ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(植物性ヨーグルト) |
臨床試験: Lactobacillus plantarum 299v (DSM 9843) は 過敏性腸症候群の症状を改善します |
Philippe Ducrotté et al., |
|
|
| 要約 |
目的: Rome III 基準を満たす過敏性腸症候群 (IBS) 患者の大規模なサブセットにおける腹部症状の軽減に対する Lactobacillus plantarum 299v (L. plantarum 299v) (DSM 9843) の対症療法効果を評価すること。 |
| 方法:この二重盲検、プラセボ対照、並行計画研究では、被験者は無作為にL. plantarum 299v(DSM 9843)1カプセルまたはプラセボのいずれかを毎日4週間摂取する群に割り付けられた。 腹痛、膨満感、直腸が完全に排出されない感覚の頻度と強度を視覚的アナログスケールで毎週評価し、同時に排便回数を計算しました。 |
| 結果: 214 人の IBS 患者が募集されました。 4週間後、痛みの重症度(0.68 + 0.53 vs 0.92 + 0.57、P < 0.05)と1日の頻度(1.01 + 0.77 vs 1.71 + 0.93、P < 0.05)の両方が、プラセボよりもL. plantarum 299v(DSM 9843)の方が低かった。 膨満感についても同様の結果が得られました。 4週目では、患者の78.1%がL. plantarum 299v (DSM 9843)の症状効果を優れまたは良好とスコア付けしたが、プラセボではわずか8.1%であった(P < 0.01)。 |
| 結論: L. plantarum 299v (DSM 9843) による 4 週間の治療は、Rome III 基準を満たす IBS 患者の症状、特に腹痛と膨満感の効果的な軽減をもたらしました。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.材料と方法 |
| 2.1.患者 |
| 2.2.研究デザイン |
| 2.3.研究製品 |
| 2.4.評価と研究のエンドポイント |
| 2.5.サンプルサイズとランダム化 |
| 2.6.統計分析 |
| 3.結果 |
| 3.1.消化器症状の頻度 |
| 3.2.消化器症状の重症度 |
| 3.3.総合評価 |
| 3.4.食生活別の効果比較 |
| 3.5.安全性 |
| 4.討議 |
本文 |
| 1.はじめに |
| 過敏性腸症候群 (IBS) は、一般開業医や消化器内科医が遭遇する最も頻繁な消化管疾患の 1 つです。 IBS は、排便習慣の変化に伴う慢性的かつ再発性の腹痛または不快感を特徴とする機能性腸疾患です。 あらゆる治療の主な目的は、患者の生活の質を著しく損なう可能性がある腹痛を軽減することです。 発行されたガイドラインによると、腹痛の主な治療選択肢には、低用量の鎮痙薬または抗うつ薬が含まれ、輸送障害を改善するために下痢止め薬または下剤が投与されます[1、2]。 しかし、多くの場合、これらすべての選択肢は腹痛の軽減には期待外れのままです。 IBSの治療効果はおそらく、腸の運動性の変化、内臓の過敏症、脳腸相互作用の異常、食物不耐症、腸の透過性の変化、感染後および/または炎症後の変化など、この病気の不均一な病因によって影響を受けると考えられます[3] |
| 最近、症状の発症時の腸内細菌叢の質的または量的変化の有害な役割が強調されています。 したがって、適切な量を摂取すると宿主に健康上の利益をもたらす生きた微生物であるプロバイオティクスの治療的使用を議論する理論的根拠が存在します[4]。 IBS症状を改善するいくつかのプロバイオティクス株の有効性に関する臨床証拠が最近明らかになりました[5,6]が、IBS症状に対するプロバイオティクスの作用機序は完全には理解されていません。 一部のプロバイオティクスは小腸および大腸の上皮に結合し、抗生物質特性を持つ物質を生成する可能性がありますが、他のプロバイオティクスは付着を巡って競合し、それによって病原菌の侵入を軽減します[7]。 プロバイオティクスはまた、サイトカインと細胞環境を炎症促進状態から抗炎症状態に変化させることによって、胃腸管腔免疫を調節します[8]。 また、未消化の炭水化物を短鎖脂肪酸に変換し、結腸細胞の栄養素として働き、腸の運動性に影響を与える可能性があります[4]。 |
| Lactobacillus plantarum 299v (L. plantarum 299v) (DSM 9843) は、マンノース接着の特異的なメカニズムにより、生体内でヒトの結腸粘膜に存在できるプロバイオティクス株です[7]。 L. plantarum 299v (DSM 9843) も、健康なボランティアの便中のカルボン酸、特に酢酸とプロピオン酸の量を増加させます[9]。 この菌株は、Listeria monocytogenes, Escherischia coli, Yersinia enterolytica, Enterobacter cloacae and Enterococcus faecalisなどのいくつかの潜在的な病原体に対して抗菌活性を示しています[10]。 L. plantarum 299v (DSM 9843) はまた、炎症を起こした結腸由来のマクロファージおよび T 細胞におけるインターロイキン 10 の合成および分泌の増加を介して有益な免疫調節活性を持っています。 そして最近、L. plantarum 299v (DSM 9843) が杯細胞におけるムチン MUC2 および MUC3 の転写と排出を増加させることが実験研究で報告されました [11,12]。 |
| 3つの単一施設研究で、IBS患者におけるL. plantarum 299v (DSM 9843)の臨床効果が試験されている[13-15]。 2 つの試験では、プラセボと比較して鼓腸スコアの改善 [13] と腹痛の軽減 [14] において有意な利点が実証されましたが、わずか 12 人の患者に基づいた 3 番目の試験の結果は決定的ではありませんでした。 現在のランダム化二重盲検プラセボ対照臨床試験の目的は、Rome III 基準を満たす IBS 患者のより大きなサブセットにおける L. plantarum 299v (DSM 9843) の対症療法の有効性を評価することでした。 |
| 2.材料と方法 |
| 2.1.患者 |
| 参加者(n = 214)は、インドの 4 つの臨床センター(ムンバイに 1 つ、チェンナイに 2 つ、バンガロールに 1 つ)の一般開業医によって募集されました。 Rome III基準に従ったIBSを有する18〜70歳の被験者が対象となる資格があった。 すべての被験者は、器質的疾患を除外するためにベースラインで結腸検査を受けましたが、この診断が疑われた患者の腸感染症は便培養によって除外されました。 結腸直腸疾患やその他の胃腸疾患を含む重度の慢性疾患を患っている被験者は除外されました。 妊娠中および授乳中の女性、研究製品の評価を妨げる可能性のある食習慣を持つ患者、または研究製品の成分に対して既知のアレルギーを持つ患者も除外されました。 研究全体を通じて、被験者は他のプロバイオティクスを摂取することを許可されず、通常の食事習慣や運動習慣を変えないよう奨励されました。 |
| 2.2.研究デザイン |
| この研究は、IBS 症状に対する L. plantarum 299v (DSM 9843) の毎日の摂取の有益な効果を評価するために、並行群による多施設二重盲検プラセボ対照研究として設計されました。 治療期間は4週間で、1週間ごとに3回のフォローアップ来院でした。 研究プロトコールはヘルシンキ宣言に従って実施され、地元の倫理委員会によって承認されました。 すべてのボランティアは、研究に参加する前に書面によるインフォームドコンセントを与えました。 |
| 2.3.研究製品 |
| 試験製品は、凍結乾燥した乳酸菌と賦形剤の混合物を含むプロバイオティクス製剤でした。 乳酸菌株はL. plantarum 299v (DSM 9843)であった。 これは、番号 DSM 9843 で DSM コレクション (Deutsche Sammlung von Mikrooorganismen und Zellkulturen GmbH) に寄託されています。試験製品には、ジャガイモデンプンとステアリン酸マグネシウムをベースとしたカプセルあたり 100 億のコロニー形成単位 (cfu) が含まれていました。 対照製品には、ジャガイモデンプン (97%) およびステアリン酸マグネシウム (3%) が含まれていました。 試験製品と対照製品はどちらも同様の外観、質感、味を持っていました。 どちらの製品も研究用に特別に調製され、ローセル・ラレマン研究所(フランス、ブラニャック)から提供されました。 |
| 2.4.評価と研究のエンドポイント |
| 主要評価項目は、腹痛エピソードの頻度の改善でした。 副次評価項目は、腹痛の重症度の変化、腹部膨満の頻度と重症度の変化、および直腸が完全に排出されない感覚の変化でした。 腹痛の頻度と直腸が完全に排出されない感覚の両方を、1 (時折のみの症状) から 4 (毎日の症状) までの範囲の 4 段階スケールを使用して毎週評価しました。 症状の重症度(腹痛、腹部膨満感、および直腸が完全に排出されない感覚)を視覚的アナログスケール(VAS 1 ~ 10)で評価し、0(痛みなし、VAS = 0)から 3(重度、VAS = 8 ~ 10 )の範囲の 4 ポイントスケールに変換しました。 |
| 1 日の排便回数と腹部膨満エピソードを計算し、来院ごとに記録しました。 4週間の治療期間の終わりに、治療の全体的な有効性に関する患者と医師の両方の意見が、「悪い」から「非常に良い」までの4段階スケールを使用して記録されました。 |
| 安全性評価に関しては、血球数、血糖、血中尿素窒素および肝機能検査の評価のために、各患者のベースラインおよび第 4 週に血液サンプルが採取されました。 診察のたびに身体検査と有害事象の確認が行われました。 |
| 2.5.サンプルサイズとランダム化 |
| サンプルサイズの計算は、主な結果である腹痛エピソードの頻度に基づいて行われました。 検出力 80%、統計的有意水準 5% で 2 つのグループ間の 20% の有意差を検出するために必要な試験サンプル サイズは、1 グループあたり少なくとも 79 人の患者であると計算されました。 途中で辞退したすべての被験者が置き換えられなかったことを考慮して、214 人の被験者がコンピューターで生成されたランダム化リストに従って 1:1 の比率でランダム化されました。 各施設について、1:1 の比率を維持するランダム化チャートが研究者に提供されました。 すべての研究者、患者、モニターは研究全体を通じて盲検化されました。 割り当ての隠蔽を確実にするために、包装とラベル貼り付けは第三者によって行われ、ランダム化コードは研究中安全な場所に保管されました。 |
| 2.6統計分析 |
| 有効性のすべての分析は、完全な分析セット (FAS) 集団を使用して実行されました。 FAS 集団は、治験薬を少なくとも 1 回投与し、ベースライン後の有効性評価を少なくとも 1 回受けた、無作為化されたすべての被験者に相当します。 症状の全体的な評価は、各期間の固定因子として、時間、治療グループ、相互作用時間×積、およびベースラインスコアを使用した反復測定分散分析 (ANOVA) を使用して分析されました。 |
| 3.結果 |
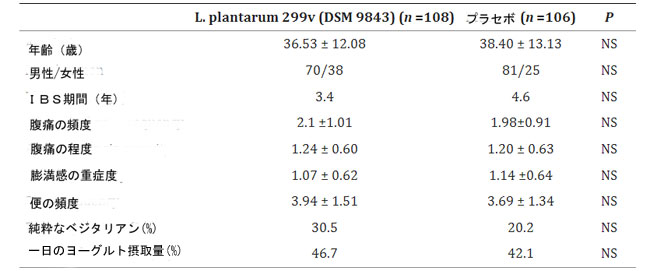
| 研究のフローチャートを図1.1に示します。 合計214人の患者が無作為化され、108人の患者がL. plantarum 299v (DSM 9843)群に割り当てられ、106人の患者がプラセボを受けるように割り当てられた。 これら 214 人の被験者のうち、10 人は、4 週間の二重盲検期間全体を完了しなかったか、治療期間に関する利用可能なデータが提供されなかったため、除外されました。 患者の大多数はIBS-D患者であり、L. plantarum 299v (DSM 9843)群では63.89%、プラセボ群では60.3%であった。 2 つのグループのベースライン特性を表 表 1 に示します。 |
| 表 1 2 つのグループ間の被験者のベースライン特性 (平均 ± SD) |
 |
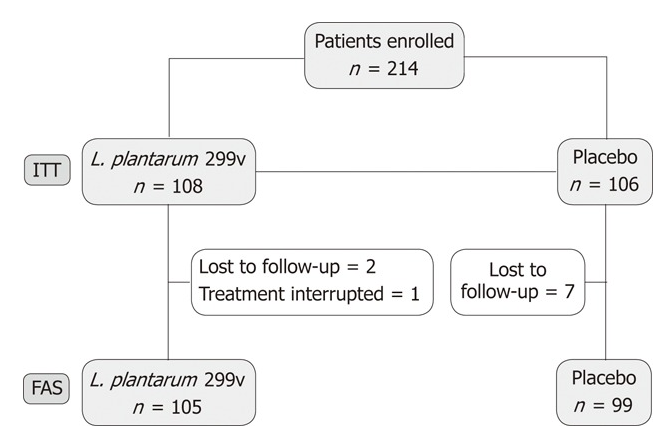 |
図 1 研究のフローチャート。 L. plantarum 299v:Lactobacillus plantarum 299v; FAS: 完全な分析セット。 ITT: 治療するつもりです。 |
| 3.1.消化器症状の頻度 |
| この 4 週間にわたる各消化器症状の頻度の平均変化を図 2. に示します。 腹痛頻度の減少は、3 週目と 4 週目では、L. plantarum 299v (DSM 9843) グループの方がプラセボ グループよりも有意に高かった。4 週目の終わりには、L. plantarum 299v (DSM 9843) グループの平均頻度は 51.9% 大幅に減少した。L. plantarum 299v グループではプラセボグループの 13.6% 減少と比較しました。 便の回数、膨満感、および不完全な排泄回数の全体的な減少も、4 週間にわたってプラセボ群と比較した場合、L. plantarum299v (DSM 9843) 群で有意に大きかった (P < 0.05)。 両方の治療の排便回数に対する効果を図 3. に示します。 L. plantarum 299v (DSM 9843) では、2 週間目の治療後に 1 日の便数の大幅な減少が観察されました。 |
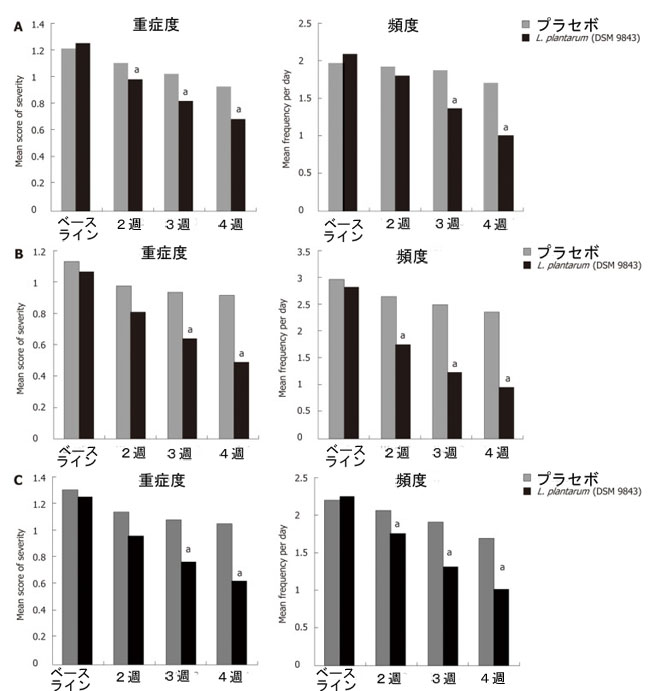 |
| 図2 両方のグループにおける症状の頻度と重症度の変化 |
A: 腹痛。 B: 膨満感。 C: 不完全な避難感。 L. plantarum (DSM 9843): Lactobacillus plantarum 299v。 aP < 0.05 対ベースライングループ。 |
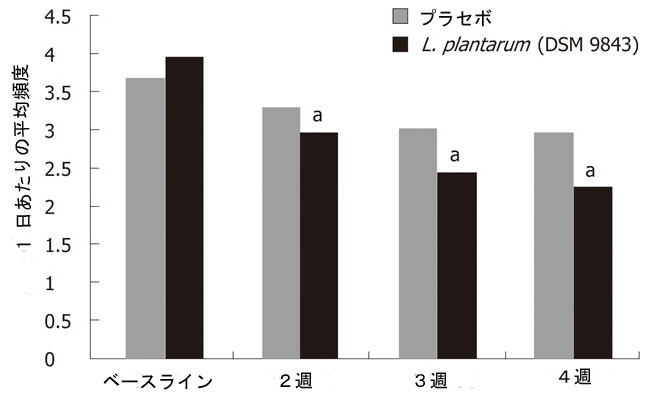 |
| 図3 両グループの排便回数の変化 |
| L. plantarum (DSM 9843): Lactobacillus plantarum 299v。 aP < 0.05 対ベースライングループ。 |
| 3.2.消化器症状の重症度 |
| 4 週間にわたる腹痛の平均重症度の変化を VAS で分析しました。 4 週目の終わりに、平均スコアは L. plantarum 299v (DSM 9843) グループで 45.2% 減少しましたが、プラセボ グループでは 23.3% だけ減少しました (図 (図 2A).2A)。 このスコアの毎週の分析では、プラセボと比較して、L. plantarum 299v (DSM 9843) 群の 2、3、および 4 週目のスコアが有意に低いことが示されました。 腹部膨満感の重症度の平均スコアの低下および不完全な排出感も、3週目および4週目でプラセボ群と比較して、L. plantarum 299v (DSM 9843)群で統計的に高かった(図2B2BおよびC)。 |
| 3.3.総合評価 |
| 受けた治療の有効性を良好または優れていると考えた患者の割合は、プラセボ群よりもL. plantarum 299v (DSM 9843)群の方が有意に高かった(78.1% vs 8.1%)(図4)。研究者によって有効性が推定された場合にも同様の結果が観察されました (82.8% 対 11.1%) (図 4)。 |
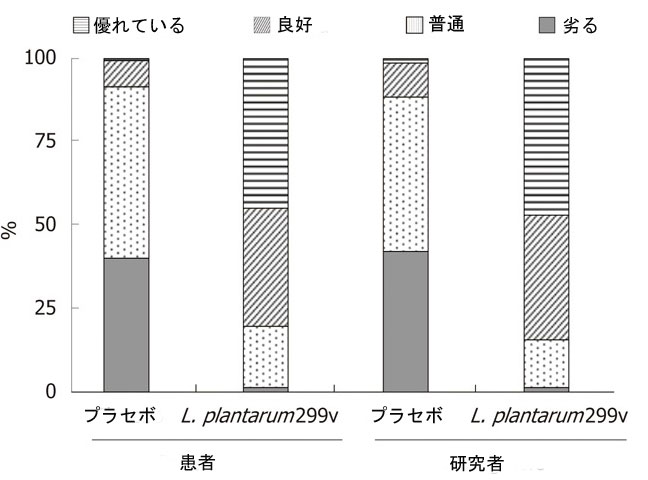 |
| 図 4 患者および研究者による治療効果の全体的な評価 |
| 3.4.食生活別の効果比較 |
| ヨーグルトの摂取は結果に影響を与えず、2 つの治療群間に差は生じませんでした (データは示されていません)。 ベジタリアンか非ベジタリアンかを考慮した場合、腹痛の頻度も両腕で差はありませんでした。 しかし、L. plantarum 299v (DSM 9843) による腹痛の重症度は、2、3、4週目ではベジタリアンの方が非ベジタリアンよりも低かった(P < 0.05)。 |
| 3.5.安全性 |
| 4週間の治療中、どのグループでも重大な副作用は報告されませんでした。 報告された唯一の有害事象は、L. plantarum 299v (DSM 9843) を投与された患者の 1 人が発症した一過性のめまいでした。 研究全体を通じて、血液パラメータの変化は検出されませんでした。 |
| 4.討議 |
| 今回のプラセボ対照試験は、インド人集団において、L. plantarum 299v (DSM 9843) が、Rome III 基準を満たす IBS 患者の IBS 症状、特に腹痛や膨満感を軽減できるプロバイオティクス株であることを実証しました。 腹痛は、IBS 患者が医師のアドバイスを求める主な症状であるため、主要評価項目として選択されました。 この試験は、中等度の IBS 症状を訴え、一般開業医によって募集された、あらゆるサブタイプの IBS 患者のグループを対象に設計されました。 プロバイオティクスを用いたいくつかの試験では、主にIBS-D患者が対象となっているが、微生物学的研究では、微生物叢の質的変化がすべてのIBSサブタイプに存在することが強調されている[16]。 したがって、サブタイプを問わず、あらゆる IBS 患者が参加資格があると考えました。 研究対象者の約3分の2が女性であった以前の試験と比較して、今回の研究では、募集された参加者の大多数は男性であった。 欧米で報告されているIBS患者における女性の優位性は、アジア人、特にインドでは観察されていない。 最近の 2 つの主要なコミュニティ研究では、男性集団における IBS の有病率が高いことが報告されています。 ムンバイでは、男性の有病率は7.9%、女性の有病率は6.9%で、全インドの研究では男性の有病率は4.3%、女性の有病率は4.0%でした[17]。 しかし、インド亜大陸の他の人口調査では、Rome I 基準を使用したIBS有病率が8.5%であると報告されており、西側諸国と同様に女性の優位性が実証されています[18]。 この研究の母集団と以前に発表された試験の母集団との間の顕著な性差は、インド亜大陸ではあるがアジアの他の地域では男性の方が医療へのアクセスが多いようであるという事実によっても説明できる[19]。 しかし、コミュニティグループの相談行動に関するデータはすべて一致しているわけではありません。 インド消化器病学会特別委員会が実施した最近の大規模調査(18センターのIBS患者3000人、地域被験者4500人)では、男性の33%、女性の38%が過去12カ月以内に医師の診察を受けたことがあった[20]。 この試験に登録された患者の食行動も、純粋なベジタリアンの割合が高く、症例のほぼ半数が毎日ヨーグルトを摂取していた西洋型IBS患者の食行動とは多少異なっていました。 栄養素と細菌の間に相互作用がある可能性があるため、たとえ 2 つのグループ間で食行動に違いがなかったとしても、このレジメンが治療結果に影響を与えた可能性を排除することはできません。 私たちは、腹痛の強さに関する L. plantarum の結果が、ベジタリアンの IBS 患者よりもベジタリアンの方が優れていることさえ観察しました。 これは、この菌株の症状効果が少なくとも部分的に管腔内容物と L. plantarum の間の相互作用に関連している可能性があること、または株が管腔内の栄養素の代謝に影響を与えていることを示唆しています。 しかし、私たちの研究のデザインでは、これが実際に当てはまると結論付けることはできません。 |
| この試験は、二重盲検プラセボ対照並行デザインと治療効果の両方を含む転帰測定によりプラセボに対する統計的優位性を実証するために、機能性消化管疾患の試験デザインに関する Rome III ガイドラインに従って実施されました[21]。 主な症状、つまり腹痛について、および適切な軽減を得るために治療効果を全体的に評価します。 IBSにおけるプロバイオティクスの対症療法的有効性を試験するいくつかの臨床試験は、この試験よりも長期間にわたって行われました。 ただし、4週間の治療期間はRome IIIガイドラインに従っているだけでなく、国際機関の推奨にも従っている[22]。 この研究の潜在的な弱点の1つは、治療効果に反応することが示されているIBS症状重症度スケールなどのスコアではなく、症状の頻度を分析するための4点リッカートスケールを選択したことであった[23]。 中等度の腹痛のある患者を登録しました。 いくつかの研究では、満足のいく軽減エンドポイントの達成は、ベースラインの症状の重症度に大きく影響されることが示唆されています[23、24]。 しかし、ベースラインの重症度が満足のいく症状の軽減などのエンドポイントの達成を損なうという懸念は、現在の臨床試験の設計には影響を与えていないようだ。 例えば、5-HT3拮抗薬[25]や低用量の抗うつ薬[26]を用いた試験、あるいは非薬理学的アプローチ[27]を用いた試験でも、試験のエンドポイントとして適切な軽減の達成に対するベースラインの重症度の影響は確認されていない [17,28]。 |
| 多くの試験でのこれまでの結果によれば、プラセボを投与された IBS 患者は時間の経過とともに大幅な改善を示しました。 しかし、この改善はL. plantarum群よりも低く、改善したと考えたプラセボ群の患者全体の数は少なかった。 さらに、今回の研究では、プラセボの結果は、プールされたプラセボ反応が 37.5% であると報告した 73 件のランダム化対照試験 (RCT) の最近のメタ分析で計算された結果よりも低かった。 しかし、プラセボ反応率に影響を与える要因の同じメタ分析では、ヨーロッパのRCTでは反応率が著しく高いことが概説されました[29]。 治療の有効性を良好または優れていると考えた患者の割合は、L. plantarum 299v (DSM 9843) 群では非常に高く (78.1%)、プラセボ群では低かった (8.1%)。 この結果は、各 IBS 症状に対する L. plantarum 299v (DSM 9843) とプラセボの効果が大きいということだけでは説明できません。 この満足度は、インドの IBS 患者に非常に頻繁にみられる上腹部の症状に対するこの緊張の有効性の可能性によっても説明できるかもしれません。 実際、インド消化器病学会の特別委員会は、インドの IBS 患者の 49% が心窩部痛を報告し、70% が痛みよりも上腹部の膨満感や膨満感を訴えていると概説しています[20]。 |
| この試験に先立って、L. plantarum 299v (DSM 9843) を使用した 3 件の研究が発表されています。 最初の研究では、Nobaekら[13]は60人のIBS患者を登録し、L. plantarum 299vとプラセボを比較して、内因性結腸細菌叢がプロバイオティクスの摂取によって変化するかどうかを判定した。 複数の二次症状ベースのエンドポイントも評価されました。 積極的な治療期間は 2 週間の観察期間の後、4 週間続きました。 プラセボと比較して、治療期間の後半に鼓腸の統計的に有意な減少が観察されましたが、この副次評価項目の分析には 60 人中 52 人の患者のみが含まれていました。 別の研究では、Niedzielinら[14]は40人のIBS患者を登録し、腹痛と全体的なIBS症状をそれぞれ一次アウトカムと二次アウトカムとして評価した。 4週間後、L. plantarum 299v群では20/20人の患者が痛みを完全に解消しましたが、対照群では11/20人でした(P = 0.0012)。 さらに、L. plantarum 299v グループの患者 20 人中 19 人では、対照グループの患者 20 人中 3 人が全体的な IBS 症状の改善を経験しました (P < 0.0001)。 どちらの試験でも、副作用は確認されませんでした。 Senら[15]が実施した最終研究では有意な改善は見られなかったが、クロスオーバーデザインで患者12名のみを対象とした擬似ランダム化研究であり、IBS症状の複合スコアの変化を評価した。 8週間の時点では、グループ間で有意差は確認されませんでした[15]。 登録された母集団、研究デザイン、結果変数、統計分析に大きな違いがあることを考えると、研究全体を比較することは困難であり、以前の 3 つの研究はすべて複数の設計上の欠陥を抱えていました。 |
| 結論として、本研究は、IBS の管理における特定の菌株 L. plantarum 299v (DSM 9843) の潜在的な利点を示しています。 プロバイオティクスの潜在的な有益な効果のメカニズムを特定するには、さらなる研究が必要です。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、World J Gastroenterol. 2012 Aug 14; 18(30): 4012–4018.に掲載されたClinical trial: Lactobacillus plantarum 299v (DSM 9843) improves symptoms of irritable bowel syndrome. を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


