ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
腸内細菌叢:高尿酸血症と痛風の潜在的な治療標的 |
Jiahui TANG et al., |
|
|
| 要約 |
近年、高尿酸血症(HUA)および痛風の罹患率は増加傾向にある。高尿酸血症/痛風に対する既存の治療法は、潜在的なリスクによって制限されることが多く、より安全で効果的な治療法の開発が求められている。近年の研究により、腸内細菌叢が尿酸(UA)恒常性の重要な調節因子であることが明らかになってきている。本レビューでは、高尿酸血症/痛風に対する腸内細菌叢を標的とした介入に関する最新の知見を、作用機序の解明と臨床応用への可能性に焦点を当ててまとめる。作用機序の解明と臨床応用を結びつけることで、高尿酸血症/痛風管理における腸内細菌叢に基づく治療法の最適化に向けたロードマップを提供することを目指す。腸内細菌叢は、尿酸およびプリン代謝の調節、炎症の軽減、免疫応答の調節、腸管バリア機能の強化など、複数のメカニズムを介して高尿酸血症/痛風を軽減することができる。腸内細菌叢を標的とした治療戦略には、プロバイオティクス、プレバイオティクス、漢方薬、糞便微生物移植などがあり、これらは複数の標的と複数の経路に作用する効果をもたらします。これらの微生物叢を標的とした治療法は、従来の薬剤に比べて多くの利点がありますが、いくつかの課題も残っています。今後の研究では、作用機序の解明、個別化された微生物叢の調節、そして高尿酸血症/痛風の治療パラダイムを最適化するための大規模臨床試験を優先的に行うべきです。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2. 高尿酸血症/痛風管理における腸内細菌叢の潜在的なメカニズム |
| 2.1.尿酸代謝の調節 |
| 2.2.炎症の緩和と免疫応答の調節 |
| 2.3.腸管バリアの完全性の保護 |
| 3.腸内細菌叢を標的とした治療アプローチ |
| 3.1.プロバイオティクス |
| 3.2.プレバイオティクス |
| 3.3.伝統中国医学(TCM) |
| 3.4.糞便微生物叢移植(FMT) |
| 3.5.その他のアプローチ |
| 4.高尿酸血症/痛風の治療アプローチ:利点と限界 |
| 5.結論と展望 |
本文 |
| 1.はじめに |
| 高尿酸血症は、プリン代謝異常および/または尿酸代謝機能障害の結果として血清尿酸値が上昇する慢性疾患です。高尿酸血症は痛風の病態生理学的基盤であり、慢性腎疾患、糖尿病、心血管疾患の独立した危険因子であるとともに、早期死亡の独立した予測因子でもあります[1]。過去30年間で、世界の痛風患者数は2,200万人から5,300万人に増加し、発生率は63.44%増加しました[2]。急性および慢性の痛風性関節炎は、四肢機能と患者の生活の質に悪影響を及ぼします。したがって、高尿酸血症/痛風の予防と治療の標準化が不可欠です。 |
| 高尿酸血症の病態生理学的メカニズムに基づくと、現在の尿酸降下療法は、尿酸産生抑制、尿酸排泄促進、尿酸分解促進の3つに分類される。これらの薬剤は臨床現場で重要な役割を果たしているものの、肝臓や腎臓の障害、心血管イベントの増加、重篤な過敏症反応を引き起こす可能性があり、一部の患者では使用が制限される。研究の進展に伴い、新たな治療標的が次々と発見されている。 |
| 腸内細菌叢はヒトの第二のゲノムであり、多くの疾患と関連しており、研究の興味深い分野となっています[3]。腸内細菌叢は、腸管上皮バリアを保護し、免疫系の発達を促進し、栄養素を獲得し、病原菌の増殖を抑制することで、恒常性を維持し、健康を促進します[4]。近年、腸内細菌叢と高尿酸血症/痛風との関連性を示す研究が数多く発表されています。痛風の発症と特定の腸内細菌叢の間には、潜在的な因果関係が存在する可能性があります[5]。そのメカニズムには、尿酸とプリン代謝への影響、および抗炎症作用と抗酸化作用が含まれます[6]。高尿酸血症/痛風は、腸内微生物の構成と代謝を変化させ、腸内微生物生態系の障害を悪化させ、悪循環を生み出すこともあります[7,8,9]。したがって、腸内細菌叢は高尿酸血症/痛風の治療の潜在的な標的となる可能性があります。本稿では、高尿酸血症/痛風の治療における腸内細菌叢の潜在的な治療戦略と可能性のあるメカニズムについて概説する。 |
| 2. 高尿酸血症/痛風管理における腸内細菌叢の潜在的なメカニズム |
| 2.1.尿酸代謝の調節 |
| 尿酸はプリン代謝の最終産物であり、図1はヒトにおける尿酸代謝過程と、腸内細菌叢が尿酸代謝に影響を与えるメカニズムを明確かつ簡潔に概説している。腸内細菌が宿主のプリン代謝恒常性に寄与していることを示す研究が増加している。山田らは、ラクトバチルス」・ガセリPA-3が腸管からのプリン吸収を減少させることを報告した[10]。笠原らは、バチルス属、フソバクテリオタ属、シュードモナス属など、プリンを炭素源およびエネルギー源として嫌気的に利用するプリン分解細菌を同定した。また、この機能に関連する遺伝子群が腸内細菌叢に広く分布していることも明らかにした[11]。ラクトバチルスなどの一部の腸内細菌は、キサンチンオキシダーゼ(XOD)の活性を阻害し、プリンから尿酸への変換を減少させる能力がある[12]。生体内での尿酸の排泄は、主に腎尿細管および腸上皮にある一連の尿酸トランスポーター、例えばATP結合カセットサブファミリーGメンバー2(ABCG2)やグルコーストランスポーター9(GLUT9)に依存している。アリステペス・インディスティンクタスの尿酸低下効果を媒介する主要な微生物エフェクターである馬尿酸は、ATP結合カセットサブファミリーGメンバー2プロモーター領域へのペルオキシソーム増殖因子活性化受容体γ(PPARγ)の結合を促進し、腸ブラシ膜へのATP結合カセットサブファミリーGメンバー2の局在を促進することによって、ATP結合カセットサブファミリーGメンバー2の発現を上方制御した[13]。メタボロミクス解析によると、腸内細菌叢の異常は、トリプトファンやフェニルアラニンなどの複数のアミノ酸の代謝経路を変化させ、間接的に溶質キャリア(SLC)ファミリー輸送体の発現を調節し、それによって尿酸代謝に影響を与えることが示されている[14]。腸内細菌叢は、短鎖脂肪酸などの特定の代謝産物を産生することにより、腸の炎症を軽減し、腸管バリアの完全性を維持し、尿酸輸送体の正常な分布と機能を確保することもできる[8, 15]。ヒトとは異なり、ヒトの腸内の緑膿菌などの共生細菌は、尿酸をより溶解性の高い化合物であるアラントインに変換する反応を触媒する尿酸オキシダーゼ(UOX)などの尿酸分解活性を持つ酵素を合成することができる[9, 16, 17]。Liuら腸内細菌の中には、尿酸を嫌気的に消費し、キサンチンまたは乳酸と短鎖脂肪酸に変換するものもあることがわかった[6]。 |
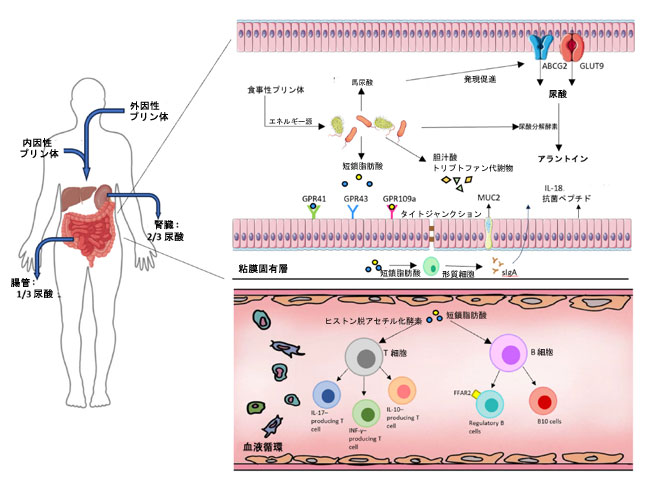 |
図1. 尿酸の代謝と、高尿酸血症/痛風の治療における腸内細菌叢の可能性のあるメカニズム。 腸内細菌叢は、プリンと尿酸の代謝を調節することで高尿酸血症を改善します。腸内細菌叢によって産生される主要な抗炎症性代謝物である短鎖脂肪酸は、腸の炎症を調節し、免疫細胞の分化を調節します。さらに、短鎖脂肪酸、胆汁酸、およびトリプトファン代謝物は、腸管バリアの完全性を維持する上で重要な役割を果たします。 |
| 2.2.炎症の緩和と免疫応答の調節 |
| 痛風の発症には、様々な炎症細胞やサイトカインが関与しています。尿酸の高値が持続しても、必ずしも急性痛風発作を引き起こすとは限りませんが、マイトジェン活性化プロテインキナーゼ/核因子κB(MAPK/NF-κB)やプロテインキナーゼB/哺乳類ラパマイシン標的タンパク質(AKT/mTOR)などのシグナル伝達経路を活性化し、慢性炎症状態を引き起こす可能性があります[18, 19]。尿酸ナトリウム(MSU)結晶は、マクロファージの特異的受容体、例えばプリン作動性2X7受容体(P2X7R)、一過性受容体電位バニロイド4(TRPV4)、およびトール様受容体2/4(TLR2/4)に作用し、NOD、LRR、およびピリン含有ドメインタンパク質3(NLRP3)インフラマソームを活性化します。これに続いてインターロイキン-1β(IL-1β)とインターロイキン-18(IL-18)が放出され、急性痛風発作を引き起こします[7, 20]。短鎖脂肪酸は、プロピオン酸、酢酸、酪酸など、食物繊維の発酵によって腸内細菌叢によって生成される代謝物であり、細胞にエネルギーを供給したり、腸管バリアを修復したりするなど、重要な生理学的効果を発揮します[21, 22]。短鎖脂肪酸は主にヒストン脱アセチル化酵素(HDAC)を阻害し、GPR41、GPR43、GPR109aなどのGタンパク質共役受容体(GPR)を活性化することによって効果を発揮します[23, 24]。 短鎖脂肪酸は腸管上皮細胞上のTLR受容体を介してNF-κB経路を活性化し、インターロイキン-8(IL-8)や腫瘍壊死因子α(TNF-α)などの炎症性サイトカインの産生を調節します[25]。短鎖脂肪酸はまた、mTORおよびシグナル伝達兼転写活性化因子(STAT3)経路を介して腸管上皮細胞における抗菌ペプチドの発現を促進します[26]。さらに、制御性T細胞(Treg)の分化を促進し、インターロイキン-10(IL-10)の分泌を増強します[27, 28]。Parkらは、短鎖脂肪酸がサイトカイン依存的にT細胞のIL-17、インターフェロン-γ、および/またはIL-10産生T細胞への分化を直接促進することを実証しました。この効果はGタンパク質共役受容体とは無関係であり、ヒストン脱アセチル化酵素の活性に依存します[29]。短鎖脂肪酸は獲得免疫にも影響を与える可能性がある[30]。関節リウマチモデルでは、短鎖脂肪酸は遊離脂肪酸受容体2(FFAR2)を介して制御性B細胞(Breg)を増加させ、炎症誘発性B細胞サブセットを減少させることで炎症を軽減する[31]。酢酸は、in vitroおよびin vivoの両方でB細胞のIL-10産生B10細胞への分化を促進する[32]。さらに、酢酸は腸管B細胞を刺激して免疫グロブリンA(IgA)を分泌させ、病原体を中和し、腸内細菌叢の恒常性を維持する[33]。リポ多糖(LPS)はグラム陰性細菌の細胞壁の成分である。血中リポ多糖の異常なレベルは、肥満やインスリン抵抗性などの代謝障害と密接に関連する多数の炎症因子の放出を誘発する[34,35,36]。 高尿酸血症/痛風患者では、腸内細菌叢の異常により血清リポ多糖レベルが上昇します。ビフィズス菌や乳酸菌などのプロバイオティクスは、病原菌の定着を阻害し、腸内エンドトキシン(リポ多糖など)の放出を減少させます[37]。 |
| 2.3.腸管バリアの完全性の保護 |
| 高尿酸血症および痛風患者は、ゾヌラオクルデンス-1(ZO-1)やオクルディンなどのタイトジャンクションタンパク質のダウンレギュレーション、および粘液層の厚さの減少を特徴とする腸管バリア機能障害を示すことが多い[38, 39]。これらの患者では、アリステペス属やパラバクテロイデス属などの炎症関連腸内細菌叢が著しく増加している。これらの細菌はTLR/NF-κB経路(訳者注:TLR/NF-κB経路は、自然免疫において病原体(細菌・ウイルスなど)を検知し、炎症性サイトカイン(IL-6, TNF-αなど)の産生を誘導するシグナル伝達系です)を活性化し、炎症を促進し、腸管上皮細胞間のタイトジャンクションを破壊する。一方、主要な酪酸産生属(例:クロストリジウム属)および保護細菌(例:ラクトバチルス属)が減少するため、短鎖脂肪酸が不足し、腸管上皮細胞へのエネルギー供給が弱まる[40]。腸内の尿酸値が高いと腸管透過性がさらに高まり、細菌エンドトキシン(リポ多糖など)が血流に移行しやすくなり、全身性炎症が悪化します[41]。全身性炎症はインスリン抵抗性の発症に寄与し、尿酸の腎臓からの排泄を阻害するため、血清尿酸値が上昇します。 |
| 微生物代謝産物は腸管バリア機能の重要な調節因子として機能します。Macia らは、短鎖脂肪酸が結腸免疫細胞上の受容体 GPR43 および GPR109A を介してシグナル伝達を行い、腸管透過性の低下に不可欠な ピリン含有ドメインタンパク質3インフラマソームを介して IL-18 の産生を促進することを実証しました [42]。in vitro 研究では、酢酸がクローディン-1 転写を促進し、細胞膜における ゾヌラオクルデンス-1およびオクルディンの再分布を誘導することが実証されました [43]。酪酸は 高尿酸血症誘導による MUC2 タンパク質(訳者注:MUC2(Mucin 2)は、主に小腸や大腸の杯細胞から分泌される主要なゲル形成性ムチン(糖タンパク質)です。腸管粘膜のバリアとして、物理的刺激や細菌、消化酵素から上皮を保護し、潰瘍性大腸炎や大腸癌などの診断マーカーとしても注目されています)のダウンレギュレーションを逆転させ、腸管粘液バリアを保護します [44]。胆汁酸と腸管バリアは双方向の相互作用を示します。腸管バリア機能の障害は、胆汁酸合成と胆汁うっ滞の障害を引き起こす可能性がある一方、胆汁酸は特定の胆汁酸受容体またはその他の下流シグナル伝達経路を活性化して腸内細菌叢の増殖を変化させ、タイトジャンクションタンパク質の発現に影響を与え、腸粘膜固有層の局所免疫系を調節する[45, 46]。Wangらは、プロバイオティクスを投与した高尿酸血書マウスでトリプトファン代謝の変化を観察し、その代謝産物であるインドール酢酸とインドールプロピオン酸のレベル上昇が特徴であり、これらは結腸のClaudin-1 mRNA(訳者注:Claudin-1 mRNA(クローディン-1 メッセンジャーRNA)は、細胞間の密着結合(タイトジャンクション)を形成する主要な膜タンパク質「クローディン-1」をコードするRNA分子です。 生体内のバリア機能維持に極めて重要な役割を果たしており、医学・生物学研究においてその発現量は健康状態や疾患の指標として頻繁に解析されます)発現と正の相関関係にあった[47]。微生物トリプトファン代謝由来のインドールとその誘導体はアリール炭化水素受容体を活性化し、タイトジャンクションタンパク質のアップレギュレーションと粘液分泌の刺激につながり、それによって物理的バリア機能を強化する[48]。さらに、腸内細菌叢は、前述のメカニズムを通じて炎症反応や免疫反応を調節することにより、間接的に腸管バリアを安定化させることができる。 |
| 3.腸内細菌叢を標的とした治療アプローチ |
| 高尿酸血症/痛風患者または動物モデルの腸内細菌叢は、健常者とは大きく異なり、その違いは、微生物多様性の低下、ビフィズス菌や酪酸菌などのプロバイオティクスおよび短鎖脂肪酸産生菌の減少、そしてプレボテラ属やフソバクテリウム属などの潜在的に病原性のある細菌の増加として現れる[49,50,51,52,53]。腸内細菌叢の異常は血清尿酸値を上昇させ、高尿酸血症/痛風の進行を促進する。プロバイオティクスは高尿酸血症/痛風の潜在的な治療選択肢となる可能性がある[8, 54, 55]。 |
| 3.1.プロバイオティクス |
| プロバイオティクスは、下痢や便秘などの消化器疾患の治療によく用いられます[56]。近年、ラクトバチルスなどのプロバイオティクスには尿酸降下作用があることが報告されています[57,58,59]。表1は、高尿酸血症(HUA)/痛風の治療におけるプロバイオティクスの使用に関する重要な研究をまとめたものです。Liらは、軽度から中等度の無症候性高尿酸血症患者にプロバイオティクス複合体を3か月投与したところ、血清尿酸値が34.77μmol/L低下したことを報告しています[60]。ラクトバチルス・ラムノサスR31およびラクトバチルス・ラムノサスR28-1は、血清および肝臓のキサンチンオキシダーゼ(XOD)活性を阻害し、腸内細菌叢の構造を改善し、腸内短鎖脂肪酸濃度を上昇させることが示されています[61]。 リモシラクトバチルス・フェルメンタム JL-3とラティカセイバチルス・パラカゼイ JS-3は、発酵食品「江水」から分離された。両菌株とも尿酸分解能力を示し、リモシラクトバチルス・フェルメンタムJS-3は24時間以内に糞便サンプル中の尿酸を最大49%分解した[62, 63]。生きたアリスティペス・インディスティンクタスを経口投与したマウスでは、腸管からの尿酸排泄が2.5倍以上に著しく増加し、血清尿酸がほぼ50%減少したことが証明された[13]。Huangらは、プロバイオティクスと従来の薬を組み合わせることで、腸の鼓腸、下痢、皮膚のかゆみなどの副作用を増加させることなく、血中尿酸値をより効果的に低下させることを発見した[64]。痛風発作を起こしたマウスでは、ビフィドバクテリウム・ロンガム51Aの投与により炎症マーカーが有意に改善し、関節の腫れと痛みが軽減された[65]。Zengらは、ラクトバチルス・パラカゼイGY-1とコルヒチンを組み合わせることで、足の腫れが軽減され、IL-1βとTNF-αのレベルが低下し、抗炎症性IL-10が上昇し、コルヒチン関連の副作用が軽減されることで治療効果が向上すると報告した[66]。WangらとKondratiukらは、プロバイオティクスと従来の薬を組み合わせることで炎症活動と急性痛風発作が軽減されることを示し、同様の結果が観察された[67, 68]。 |
| 表1. 高尿酸血症/痛風の治療におけるプロバイオティクスの研究 |
 |
 |
 |
 |
| ADA: アデノシンデアミナーゼ; AMPK: アデノシン5´-一リン酸(AMP)活性化プロテインキナーゼ; CFU: コロニー形成単位; CMC-NA: カルボキシメチルセルロースナトリウム; CRP: C反応性タンパク質; IFN-γ: インターフェロン-γ; IL-6: インターロイキン-6; NO: 一酸化窒素; NPT1: ナトリウム依存性リン酸共輸送体1; OAT1: 有機アニオントランスポーター1; OAT3: 有機アニオントランスポーター3; PDZK1: PDZドメイン含有1; PO: オキソキサントカリウム。 |
| 真菌の中には、研究上重要な意義を持つ薬用資源の宝庫となっているものがある。冬虫夏草の抽出物は、生体内および試験管内実験の両方で優れた尿酸降下作用を示した。これは、高尿酸血症マウスの腸内細菌叢の恒常性を再構築し、フィルミクテス/バクテロイデスの存在量を増加させ、高尿酸血症の変化に関連する代謝物および代謝経路を修飾した[69]。フェリヌス・イグニアリウスは、多糖類、フラボノイド、トリテルペノイドなどの生物活性成分を豊富に含む寄生性真菌である。Wangらは、キサンチンオキシダーゼの活性と発現を阻害し、結腸と腎臓におけるATP結合カセットサブファミリーGメンバー2の発現を改善し、ミトコンドリア機能を調節して高尿酸血症関連の腎障害を改善することにより、高尿酸血症を緩和したと報告している[70]。 |
| 高尿酸血症/痛風管理用に設計されたプロバイオティクスは、戦略的な遺伝子改変によって出現しました。関連する研究は主に、尿酸分解のための微生物能力の向上と消化管定着効率の最適化という2つの目標を達成することを目的としています。初期のアプローチでは、尿酸オキシダーゼを発現する遺伝子操作された細菌が開発され、ラットモデルで血清尿酸レベルが大幅に低下しました[71]。Zhaoらは、ビトレオシラ由来の細菌ヘモグロビンVhbと大腸菌由来のカタラーゼKatGを統合したエシェリヒア・コリ・ニッスル1917(EcN)(訳者注:Escherichia coli Nissle 1917(EcN)は、1917年にドイツの医師アルフレッド・ニッスルが、下痢が流行する中でも健康であった兵士の便から発見した、安全で非病原性のプロバイオティクス大腸菌株です)に酸素リサイクルシステムを実装することで、尿酸オキシダーゼの酸素依存性に対処し、低酸素条件下で酵素活性を維持し、マウスで50%以上の血清尿酸低下を達成しました[72]。Heらは、ペリプラズム尿酸オキシダーゼをエシェリヒア・コリ・ニッスル 1917に局在させることで治療効果が向上し、高プリン食によって誘発された尿酸を有するラットの酵素安定性と腸内細菌叢の調節が改善された[73]。尿酸低下効率の持続的な限界を克服するために、Zouらは、キサンチン輸送体XanQをエシェリヒア・コリ・ニッスル過剰発現させることで前駆体標的戦略を開発し、キサンチンの取り込みを8.6倍に増幅して尿酸生合成を阻害した。この革新により、マウスモデルで腎保護を伴う生理的な血清尿酸の正常化が達成され[74]、単純な酵素発現から統合的な代謝経路介入へのパラダイムシフトが示された。 |
| プリン代謝の複雑さに関して、Tong らは、嫌気性条件下でキサンチンを唯一の炭素源として利用できるように、クロストリジウム由来の嫌気性プリン分解経路を備えた エシェリヒア・コリ・ニッスルを設計した。この代謝バイパス戦略は、酸素依存性尿酸オキシダーゼ経路に頼ることなく外因性尿酸の生成を減少させる [75]。この先制的インターセプト戦略は、さまざまな食習慣を持つ患者に適している可能性がある。並行して、Gong らは、治療用タンパク質のキャリアとして外膜小胞を利用するように、設計した エシェリヒア・コリ・ニッスルのタイプゼロ分泌システム (T0SS) を改変した。この戦略は、経口投与された 尿酸オキシダーゼの安定性を大幅に向上させ、全身への送達を促進した。尿酸オキシダーゼを直接腸に分泌するように設計された設計プロバイオティクスと比較して、この タイプゼロ分泌システムベースのアプローチは優れた治療効果を示した [76]。Gencer らは、尿酸バイオレポーターと分解モジュールという二重機能を持つエシェリヒア・コリ・ニッスルを設計した。この自己制御システムは、リアルタイムの検出と応答メカニズムを通じて、in vitroモデルで頂端尿酸塩を40.35%減少させることを示した[77]。 |
| 3.2.プレバイオティクス |
| 世界消化器病学会(WGO)のプロバイオティクスとプレバイオティクス(2023年)ガイドラインでは、一般的に知られているプレバイオティクスとして、オリゴフルクトース、イヌリン、ガラクトオリゴ糖、ラクツロース、母乳オリゴ糖(ヒトミルクオリゴ糖、HMO)が挙げられています[81]。国際プロバイオティクス・プレバイオティクス科学協会(ISAP)は、プレバイオティクスを、宿主微生物によって選択的に利用され、健康上の利益をもたらす基質と定義しています[82]。この定義は、基質の種類を炭水化物から非炭水化物化合物(ポリフェノールや共役脂肪酸など)にまで広げることで、従来のプレバイオティクスの概念を拡張しています。その範囲は、消化管だけでなく、膣や皮膚など、微生物叢が存在する他の部位にも及びます。本レビューでは、より広範なプレバイオティクスについて考察します。表2は、高尿酸血症および痛風の管理における様々なプレバイオティクスの潜在的な利点をまとめたものである。 |
| 表2. 高尿酸血症/痛風の治療におけるプレバイオティクスの潜在的な利点の概要 |
 |
 |
 |
 |
 |
 |
 |
 |
| APS: Artemisia selengensis Turcz葉多糖類; DAO: ジアミンオキシダーゼ; diCQAs: ジカフェオイルキナ酸; d-LAC: d-乳酸; MDA: マロンジアルデヒド; MYD88: 骨髄分化一次応答88; OCT 1: 有機カチオントランスポーター1; OCT 2: 有機カチオントランスポーター2; OCTN2: 有機カチオン/カルニチントランスポーター |
| イヌリンは、チコリ、ショウガ、ニンニクに多く含まれる水溶性多糖類化合物である[83]。UOX遺伝子ノックアウトによって作製された高尿酸血症マウスモデルでは、7週間のイヌリン補給により、モデル群と比較して血清尿酸レベルが30%減少したが、正常対照群と比較するとレベルは依然として高かった。イヌリンはまた、オクルディンとゾヌラオクルデンス-1の発現を上方制御し、グルコーストランスポーター9またはナトリウム依存性リン酸共輸送体5(NPT5)に有意な影響を与えることなくATP結合カセットサブファミリーGメンバー2の発現を増加させることで腸管バリアの完全性を高めた。さらに、イヌリンは腸内微生物の多様性を回復させ、アッケルマンシアやルミノコッカスなどの短鎖脂肪酸産生細菌を豊富にした[84]。Bianらは、チコリが腸内微生物叢の調節によって高尿酸血症を改善すると報告したが、イヌリンの具体的な役割はそれ以上明らかにされなかった[85]。同様に、アルピニア・オキシフィラ果実由来の多糖類は、高尿酸血症マウスの血清尿酸レベルを用量依存的に有意に低下させ、200 mg/kgの用量でベンズブロマロンと同等の有効性を達成した。注目すべきことに、この治療により、プレボテラ属とルミノコッカス属の減少を逆転させ、バクテロイデス属、パラバクテロイデス属、ヘリコバクター属、フレキシスピラ属などの属の存在量を増加させることで、腸内細菌叢の構成が回復した[86]。スファセロテカ・レイリアナ多糖類も、高尿酸血症マウスの微生物構造を調節することで高尿酸血症を軽減することがわかっており、腸内細菌叢と血清代謝物、ならびにグルコース、プリン、アミノ酸代謝経路との間に相関関係が見出された[87]。 |
| クロロゲン酸は、野菜や果物に豊富に含まれるフェノール酸であり、血清尿酸値を低下させ、腎機能を保護し、炎症を軽減することが実証されている[88]。高尿酸血症マウスでは、バクテロイデス、プレボテラUGC-001、ブチリシモナスなどの短鎖脂肪酸産生細菌の存在量を増加させ、微生物のプリンおよびグルタミン酸代謝を回復させた。さらに、クロロゲン酸はタイトジャンクションタンパク質ゾヌラオクルデンス-1およびオクルディンの発現を増加させることにより、腸管バリアの完全性を強化した[89]。また、腸内細菌叢の調節によりトリメチルアミンN-オキシド(TMAO)産生を減少させることにより、高尿酸血症性腎症における腎線維症を改善し、トリメチルアミンN-オキシドを介した酸化ストレスおよび炎症反応を抑制した[90]。Hanらプニカラギンは、MAPK/NF-κB経路の阻害を介して尿中および腸管からの尿酸排泄を促進し、腸内細菌叢の構成と機能を回復させることにより、高尿酸血症マウスの尿酸レベルを用量依存的に低下させることができると最初に報告した[91]。フェルラ酸は、腸と腎臓の尿酸トランスポーターの発現を調節し、それによって血中の尿酸レベルを低下させる。また、腸内細菌叢の構成を再構築し、ラクトバチルスなどのプロバイオティクスを増加させ、バクテロイデスなどの病原菌を減少させる[92]。Lianらは、Artemisia selengensis Turcz(訳者注:タカヨモギ(Artemisia selengensis Turcz.)は、シベリアから東アジア(日本、中国、韓国)に分布するキク科ヨモギ属の多年草。別名「芦蒿(ろこう)」や「セレンゲヨモギ」とも呼ばれる。中国では若茎や葉が食用(野菜)として親しまれ、抗酸化・抗炎症作用や長寿効果がある健康・薬用ハーブとしても知られている)の葉から得られたジカフェオイルキナ酸と多糖類の組み合わせが、空腸のキサンチンオキシダーゼ活性を大幅に低下させ、バクテロイデスとフィルミクテスのバランスを回復させ、デスルフォビブリオの存在量と短鎖脂肪酸レベルを増加させることができることを発見した[93]。プーアル茶の主要なポリフェノールであるストリクチニンは、腸内細菌叢をより健康的な構成に調整することで高尿酸血症を軽減し、炎症関連の病理に対する保護をもたらす可能性があると示唆されている[94]。 |
| フラボノイドは自然界の植物に広く存在し、抗酸化作用、抗炎症作用、抗腫瘍作用、心血管保護作用がある[95]。近年、いくつかの研究で、一部のフラボノイドが尿酸値を下げる効果があることが報告されている[96,97,98,99,100]。Liらは、ケルセチンが腸内ラクトバチルス・アビアリウスCML180の量を増やすことでニワトリモデルにおける高尿酸血症を軽減することを示した。さらに遺伝子解析により、L. アビアリウスCML180には、中温および中性水素電位(pH)条件下で強いプリンヌクレオシド加水分解活性を示すヌクレオシド加水分解酵素遺伝子nhy69が含まれており、それによって尿酸産生が減少することが示された[80]。Chenらは、サフラン由来のフラボノイド抽出物が、微生物の多様性を回復させ、ローズブリア、クロストリジウム、ガストラナエロフィラレスを含む30の分類群の存在量を正常化することで、腸内細菌叢を大きく調節することが実証された。特に、この治療法は血清および腸管の尿酸レベルを効果的に低下させ、尿酸トランスポーター1(URAT1)およびグルコーストランスポーター9の発現を抑制し、ATP結合カセットサブファミリーGメンバー2の発現を亢進させた。相関分析では、差異細菌の存在量が血清代謝物のレベルと高い相関関係にあることが示され、腸内細菌叢が宿主の代謝と密接に関連していることが示唆された[101, 102]。 |
| Luらは、アポスティコプス・ジャポニクスのオリゴペプチドが腸内微生物依存的に抗高尿酸血症効果を発揮することを報告した[103]。Fanらは、アポスティコプス・ジャポニクス由来の2つの新規ヘキサペプチド、GPAGPRとGPSGRPを研究し、どちらも高プリン食によって引き起こされる腸内微生物叢の破壊を改善し、ラクトバチルスを含む15属の豊富さを回復させることができた。さらに、この研究では、グループ間で腎臓のマイクロRNA(miRNA)プロファイルの変化を特定し、短鎖脂肪酸、胆汁酸、トリプトファンの代謝に関連する属と高い相関を示したが、その根底にあるメカニズムをさらに調査する必要がある[7]。海洋魚タンパク質ペプチドは、Ildr2、Ccr7、Nr4a3を含む腸管バリアに関連する遺伝子の発現を上方制御することが報告されている[104]。 |
| レインは、ピリン含有ドメインタンパク質3インフラマソームの形成を阻害することにより、痛風性関節炎の炎症反応を弱めると考えられている[105]。Xingらは、腎障害ラットにおけるレイン-プラセオジム複合体(Rh-Pr)の腸管尿酸排泄への影響を研究した。レイン-プラセオジム複合体は、腸管におけるATP結合カセットサブファミリーGメンバー2の発現を上方制御し、グルコーストランスポーター9の発現を下方制御することで、腎臓への負担を軽減できる[106]。HUAマウスに関するいくつかの研究では、ベルベリンがキサンチンオキシダーゼ活性を低下させ、尿酸トランスポーターの発現を調節し、血中尿素窒素およびクレアチニンレベルを低下させ、炎症シグナル伝達経路の活性化を阻害することが示されている[107,108,109]。そのメカニズムは、腸内細菌叢と密接に関連している可能性がある[110]。ShanらおよびZhangらは、ベルベリンは、コプロコッカス、バクテロイデス、アッケルマンシアなどの尿酸代謝に寄与する細菌の存在量を増加させることができることがわかった[111, 112]。 |
| 3.3.伝統中国医学(TCM) |
| 近年、伝統中国医学は高尿酸血症/痛風の治療において活発な研究分野となっています。従来の解熱・解毒作用に加え、新たな研究結果から、特定の伝統中国医学の抗高尿酸血症作用は腸内細菌叢の調節を介して発揮されることが示唆されています(表3参照)[124,125,126]。四邁湯や改良百胡湯は、経口投与による高尿酸血症/痛風治療に用いられる古典的な処方であり、双柏散は外用薬として用いられます。これらの処方は、薬効を速めるために鍼治療と併用されることもあります[127]。 |
| 表3. 高尿酸血症/痛風の治療における伝統中国医学および糞便微生物移植の研究 |
 |
 |
 |
| ASC:CARDを含むアポトーシス関連斑点様タンパク質;PGE2:プロスタグランジンE2;sIgA:分泌型免疫グロブリンA;TGF-β:形質転換成長因子β。 |
| 四邁湯は痛風性関節炎の治療によく用いられる漢方薬である[128]。林らは、四邁湯が痛風性関節炎のマウスモデルにおいて、足の腫れや痛みの閾値の低下などの痛風症状を緩和し、肝毒性や腎毒性を誘発することなく血清尿酸値を低下させることを示した。さらに分析した結果、治療効果は腸内生態系を調節して炎症を軽減することによって媒介される可能性があることが示唆された。モデル群と比較して、四邁湯は腸内細菌叢の構成を変化させ、特にプレボテラNK3B31とルミノコッカスUCG-014の存在量を減少させた。また、四邁湯はIL-1β、IL-6、TNF-αなどの炎症性サイトカインの腸内レベルも低下させたが、この効果はフェブキソスタット群では観察されなかった[129]。舒卓通痺湯は血清尿酸値を大幅に低下させ、キサンチンオキシダーゼ活性を阻害することが示されている[130]。その後の研究では、これらの効果は腸内細菌叢の調節を介して発揮され、ビフィドバクテリウム属とコリンセラ属の存在量の増加とデスルフォビブリオ属とゲメラ属の存在量の減少が特徴であることが明らかになった[131]。さらに、Wenらは、この煎じ薬が酪酸産生菌を促進し、腸内ATP結合カセットサブファミリーGメンバー2発現を上方制御して痛風性関節炎を軽減することを実証した[132]。Wangらは、改良白虎湯がビフィドバクテリウム属などのプロバイオティクスの存在量を増加させ、エリシペロトリカ科の存在量を減少させることにより、痛風の急性炎症を制御できることを発見した[133]。別の研究では、李吉湯とツボへの塗布を組み合わせることで、痛風性関節炎の関節の腫れや痛みを大幅に軽減し、乳酸菌とビフィズス菌の量を増やし、腸内細菌科と腸球菌の量を減らすことができることが示されました[134]。 |
| 3.4.糞便微生物叢移植(FMT) |
| 糞便微生物叢移植は、腸内微生物叢を再構築することで疾患を治療する治療法です[135]。洗浄微生物叢移植(WMT)は、細菌溶液の生成における自動精製システムに基づいた新しい移植経路であり、従来の移植に伴う副作用を軽減し、治療効果を大幅に向上させます[136]。Xieらは、洗浄微生物叢移植治療後の痛風患者において、血中尿酸値とエンドトキシン値、および急性痛風発作の頻度と持続時間が低下したことを発見しました。その理由は、損傷した腸管バリア機能の改善に関連している可能性があります[137]。ある後ろ向き研究[138]では、高尿酸血症患者の約78%で、最初の洗浄微生物叢移植治療後3ヶ月で血清尿酸値が低下し、約30%の患者で尿酸値が正常値に戻ったことが示されました。さらに、対照群では尿酸値に有意な変化は見られず、重篤な副作用も認められませんでした。水溶性ジペプチドであるアンセリンは、尿酸合成を抑制し排泄を促進することで高尿酸血症を軽減し、同時にNLRP3インフラマソームとTLR4/NF-κBシグナル伝達経路も阻害します。Hanらは、アンセリンの抗高尿酸血症効果は腸内細菌叢を介して媒介されることをさらに実証しました。アンセリン投与マウスからの糞便微生物叢移植は、レシピエント高尿酸血症マウスに有意な尿酸低下効果をもたらしました[139]。同様に、マグロ肉オリゴペプチド(TMOP)は、腸内細菌叢を介して部分的に高尿酸血症と腎臓の炎症を軽減することがわかっており、その抗高尿酸血症効果はマグロ肉オリゴペプチド投与マウスからの糞便微生物叢の移植によって伝達可能でした[140]。 |
| 3.5.その他のアプローチ |
| 薬物療法に加え、食事療法も痛風/高尿酸血症の補助療法として徐々に普及しつつあります。Wuらは、高尿酸血症マウスにおける6種類の茶の介入効果を調査し、腸管におけるATP結合カセットサブファミリーGメンバー2発現の増強と腸内細菌叢組成の改善を示しました[142]。一部の天然植物にも尿酸値低下作用があります。腎臓茶(訳者注:「キドニーティー(腎臓茶)」は、腎臓の働きを助けたり、尿路の健康をサポートしたりするために使われるハーブティーやブレンドティーの総称です。主に、体内の余分な水分を排出する利尿作用や、炎症を抑える効果を期待して利用されます)は高尿酸血症マウスの血清尿酸値を著しく低下させ、アロプリノールと比較して肝保護効果を示しました。その理由は、腸内細菌叢構造の改善、特にローズブリア属とエンテロラブダス属の増加、およびイレイバクテリウム属とUBA1819属の減少に関連していると考えられます[143]。別の研究では、β-カロチンと緑茶粉末の補給により、痛風マウスの腸内細菌叢プロファイルが改善され、全身性炎症が軽減されました。痛風性関節炎群では、ムリバクラ、ルミノコッカスUCG-014、およびラクノスピラNK4A136群の相対存在量が減少し、血清IL-1β、IL-6、およびTNF-αと負の相関を示した。また、足関節の炎症細胞数を大幅に減少させ、関節の腫れや痛みを軽減した[144]。 |
| 4.高尿酸血症/痛風の治療アプローチ:利点と限界 |
| 臨床現場で用いられる高尿酸血症/痛風の従来の薬物療法は、大きく2つのカテゴリーに分類されます。1つ目は、コルヒチンや非ステロイド性抗炎症薬などの速効性症状緩和薬です。これらの薬剤は急性痛風発作時の疼痛を速やかに緩和しますが、多くは重大な副作用を伴います[145]。2つ目は、アロプリノール、フェブキソスタット、ベンズブロマロンなどの尿酸降下薬です。これらの薬剤は明確な尿酸降下作用を示しますが、作用機序はそれぞれ異なります。特に、アロプリノールは、HLA-B*5801アレルと強く相関する重度の過敏症反応の発生率が0.1~0.4%であり、特にアジア人集団で顕著である(RR=3.03、95% CI 1.72~5.34)[146、147]。さらに、フェブキソスタットは、心血管合併症を伴う痛風患者の死亡リスク増加と関連付けられており[148]、ベンズブロマロンは、腎尿細管および尿管の尿酸濃度を上昇させ、尿路結石症のリスクを高める[149]。 |
| 対照的に、プロバイオティクスやプレバイオティクスなどの微生物叢に基づく治療法は、複数の標的と複数の経路に効果を発揮します。これらは、全身性炎症を軽減し、免疫応答を調節し、腸管バリアの完全性を回復させながら、複数の経路を介して尿酸代謝を調節することができます[150]。これらの治療法は、従来の薬剤と併用することで、副作用を大幅に増加させることなく、尿酸低下作用と抗炎症作用を相乗的に高めることができます。しかし、重大な限界が残っています。同じプロバイオティクス種の異なる株は、異なる機能遺伝子を持っている可能性があり、尿酸代謝を調節する能力に影響を与えます。外来細菌の持続的な定着は、腸内微生物叢の競合、宿主の免疫クリアランス、食事、ライフスタイルによって影響を受ける可能性がありますが、現在、それを効果的に予測する方法はありません[151]。幸いなことに、科学者たちは最近、定着を促進するために特定の栄養素に依存するように細菌を操作したり、定着能力の高い腸内細菌株を改変したりするなど、この課題に対処するためのさまざまな戦略を開発しました。これらのアプローチは、他の疾患の治療において大きな可能性を示している[152,153,154]。しかし、外因性プロバイオティクスと腸内細菌叢との相互作用は十分に理解されておらず、菌血症、遺伝子伝達、免疫拒絶などのリスクをもたらす可能性があるため、安全性に関する懸念が残っている[155, 156]。さらに、これらの治療法は効果が現れるまでに時間がかかり、通常8~12週間を要するため、急性痛風の治療には適さない。Caiらはラットモデルで、遺伝子操作された細菌の治療効果は治療中止後2週間以内に徐々に低下し、定期的な投与レジメンの開発が必要であることを実証した[71]。さらに、現在のエビデンスは主に動物実験と小規模なヒト試験から得られたものであり、大規模なランダム化比較試験による確固たる検証が不足している。 |
| 伝統中国医学は腸内細菌叢の調節において独自の利点を示しており、痛風/高尿酸血症管理における西洋医学との統合を支持する証拠が増えつつある[157]。代表的な製剤である四邁散は、有益な腸内細菌(例:アッケルマンシア)を増強し、TLR4/NF-κB経路を抑制し、ATP結合カセットサブファミリーGメンバー2などの腸内尿酸排泄タンパク質を上方制御する[158]。しかし、その効果発現が遅いため、痛風発作時には西洋薬との併用が必要であり、持続的な尿酸低下のためには長期投与が必要となる可能性がある。さらに、伝統中国医学化合物の複雑な組成は作用機序の解釈を困難にし、弁証論治に基づく個別化治療の標準化は、臨床現場での普及において依然として問題となっている[159]。 |
| 糞便微生物叢移植は、新たな治療法として注目されており、小規模なヒト試験ではプリン代謝の再構築、尿酸値の調節、症状の緩和に効果がある可能性が示されています[137, 138, 160]。しかし、臨床応用には、ドナーのスクリーニング、移植方法の標準化、長期的な安全性に関する懸念など、いくつかの課題があります。ディスバイオシスや免疫抑制状態にある患者が糞便微生物叢移植を受けると、菌血症のリスクが高まります。DeFilippらは、2つの臨床試験で糞便微生物叢移植後に広域スペクトルβ-ラクタマーゼ産生大腸菌菌血症を発症した2例を報告しています[161]。さらに、糞便微生物叢移植の短期的な有効性は有望に見えますが、持続的な治療効果はまだ検証されておらず、宿主の遺伝的背景や基礎的な微生物構造に依存する可能性があります。 |
| 現在、高尿酸血症/痛風治療の基盤は依然として従来の薬剤療法ですが、治療パラダイムは尿酸値を下げるという単一の目標から、代謝、腸内細菌叢、免疫を統合した多標的介入へと移行しつつあります。有望な戦略の一つは、薬物療法と腸内細菌叢調節を組み合わせ、疾患の病期や個々の患者のニーズに合わせて調整することです。例えば、急性増悪の管理においては、低用量の抗炎症剤とプロバイオティクスを併用することで、尿酸分解を同時に促進することが考えられます。 |
| 5.結論と展望 |
| 腸内細菌叢と高尿酸血症/痛風との密接な関係を示唆する証拠が増えつつある。本稿では、高尿酸血症/痛風の管理に新たな知見を提供するため、腸内細菌叢が関与する可能性のあるメカニズムと潜在的な治療戦略について概説する。プロバイオティクス、プレバイオティクス、漢方薬などの標的介入は、尿酸代謝の改善、炎症反応および免疫応答の調節、腸管バリア機能の維持など、複数の経路を介して治療効果を発揮する。新たな研究では、従来の薬物療法と比較して、安全性と持続的な有効性が向上していることが示されている。しかしながら、現在のエビデンスは主に動物モデルに基づいているため、大規模コホートによる検証が必要である。ヒト腸内細菌叢の複雑な構造を考慮すると、エンテロタイプ分類は微生物群集を分類する有効なアプローチであり、微生物プロファイルと疾患病態との相関分析を強化し、標的療法に役立つ情報を提供する。しかしながら、この方法論の応用は高尿酸血症/痛風研究には見られず、緊急の調査を必要とする重要な知識のギャップとなっている。マイクロバイオーム研究が進むにつれて、高尿酸血症/痛風における腸内ウイルス叢および真菌群集の重要な役割を強調する証拠がいくつか現れている。Huangらは、痛風患者ではウイルスの多様性が低下し、ウイルス科の構成が変化しており、シフォウイルス科とミオウイルス科の存在量が減少する一方でクインビウイルス科とレトロウイルス科のレベルが上昇していることが特徴であると報告した。注目すべきことに、腸内ウイルスシグネチャーは細菌由来モデルと比較して痛風の診断性能が優れており、臨床応用における予測可能性の向上を示している[162]。腸内微生物叢は巨大な生物学的データベースである。今後の研究では、メタゲノミクス、ゲノミクス、エピゲノミクス、トランスクリプトミクス、プロテオミクス、メタボロミクスの統合に焦点を当て、高尿酸血症/痛風に関与する潜在的な分子標的と活性バイオマーカーの特定、精密な疾患治療と予後の指針に役立てることができる。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、Biosci Microbiota Food Health. 2025 Oct 17;45(2):85–99.に掲載されたGut microbiota: a potential therapeutic target for hyperuricemia and gout.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


