ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
腸内細菌叢を活用した大腸がん治療:臨床的知見から治療革新へ |
Chaofan Chen et al., |
|
|
| 要約 |
大腸がん(CRC)は依然として世界的にがん罹患率および死亡率の主要な原因であるが、従来の治療法の進歩にもかかわらず、生存率の改善は限定的である。腸内細菌叢は大腸がんの発症機序において重要な役割を果たし、臨床転帰を改善するための有望な治療標的として注目されている。大腸菌、フソバクテリウム・ヌクレアタム、バクテロイデス・フラジリスなどの特定の微生物が、DNA損傷、炎症調節、免疫抑制機構を介して腫瘍の発生と進行に関与していることを示す証拠が蓄積されている。糞便微生物叢移植、プロバイオティクス、プレバイオティクス、遺伝子操作されたバイオ医薬品など、マイクロバイオーム調節剤を研究する臨床試験では、化学療法、放射線療法、免疫療法、手術後の回復を増強する可能性が示されており、治療抵抗性の大腸がんサブタイプにおいて有望な予備的有効性が報告されている。しかしながら、マイクロバイオーム介入を標準化された臨床診療へと移行させるには、厳密なメカニズム検証、堅牢なバイオマーカー開発、そして安全性に関する懸念事項の慎重な管理が不可欠です。今後の研究では、高解像度マルチオミクス、空間マイクロバイオームマッピング、人工知能分析、そして革新的なマイクロバイオーム標的ナノテクノロジーを統合し、腸内微生物群集を正確に再構築することに注力し、それによって大腸がん治療における精密腫瘍学の新時代を切り開く必要があります。 |
| 目次(クリックして記事にアクセスできます) |
| 1.はじめに |
| 2.大腸がんにおける腸内微生物叢の役割 |
| 3.大腸がんの発症における特定の微生物の役割 |
| 3.1.大腸がんの発症における主要な細菌 |
| 3.1.1.大腸菌 |
| 3.1.2.フソバクテリウム・ヌクレアタム |
| 3.1.3.バクテロイデス・フラジリス |
| 3.2.大腸がんに関与するその他の細菌群 |
| 3.2.1.カンピロバクター属 |
| 3.2.2.クロストリジオイデス・ディフィシル |
| 3.2.3.モルガネラ・モルガニー |
| 3.2.4. ストレプトコッカス・ガロリティカス亜種ガロリティカス |
| 3.2.5.アッケルマンシア・ムシニフィラ |
| 3.2.6.クレブシエラ属菌 |
| 3.2.7.大腸がんにおける真菌とウイルスの関与 |
| 4.大腸がん臨床試験におけるマイクロバイオーム調節因子の役割 |
| 5.大腸がん治療における腸内細菌叢の役割 |
| 5.1.化学療法への治療的意義 |
| 5.2.免疫療法の治療的意義 |
| 5.3.プレバイオティクス |
| 5.4.プロバイオティクスとその生産物 |
| 5.5.遺伝子操作されたプロバイオティクス |
| 5.6.糞便微生物叢移植(FMT) |
| 5.7.放射線療法の治療的意義 |
| 5.8.放射線療法の有効性向上 |
| 5.9.放射線毒性の軽減 |
| 5.10.外科的切除における治療的意義 |
| 6.結論と今後の展望 |
本文 |
| 1.はじめに |
| 大腸がんは世界で3番目に多いがんであり、2022年には190万人以上の新規症例と90万人の死亡が報告されています(1)。米国と中国が最も高い罹患率を示し、次いで日本、ロシア、インド、ドイツ、ブラジル、英国、イタリア、フランスが続きます(2)。大腸がんの罹患率は欧米諸国で高いものの、発展途上国でも急速に増加しています。50歳以下で診断される早期発症大腸がんも、世界的に大きな懸念事項となっています(3)。 |
| 大腸がんは、その広がりに基づいて分類されます。原発腫瘍に限局している場合はステージIまたはII、局所リンパ節に及んでいる場合はステージIII、遠隔部位に転移している場合はステージIVです。ステージI~IIIの治療は通常、外科的切除を伴い、ステージIIIでは補助化学療法が必要となることがよくあります。転移性大腸がん(ステージIV)では、化学療法、分子標的療法、免疫療法、またはそれらの組み合わせを含む全身療法が一般的に用いられます(4)。腹腔鏡手術などの進歩にもかかわらず、全体的な治癒率と長期生存率はここ数十年でわずかにしか改善していません(5)。 |
| 2004年以降、ステージIII結腸がんの補助化学療法には、一般的にオキサリプラチンとフルオロピリミジンが用いられてきた(6)。しかし、このレジメンから恩恵を受ける患者はわずか20%であり、残りの80%は不必要な毒性にさらされている(7)。フルオロピリミジンはジヒドロピリミジン脱水素酵素(DPYD)によって代謝される。ジヒドロピリミジン脱水素酵素遺伝子の変異は、タンパク質の切断、薬剤曝露の長期化、および毒性の増加につながる可能性がある。ジヒドロピリミジン脱水素酵素変異のない患者では治療関連死亡率は0.1%であるが、変異のある患者では2.3%に上昇する(8)。その他の副作用には、オキサリプラチン誘発性神経障害および化学療法関連下痢がある(6)。特定の分子特性を標的とする治療が不可欠となっているが、薬剤耐性は依然として大きな課題である(9)。 |
| 免疫チェックポイント阻害(ICB)はがん治療を変革し、ペムブロリズマブは、腫瘍の変異負荷とネオアンチゲン負荷が高いことからマイクロサテライト不安定性高(MSI-H)を示す大腸がん患者のサブセットに対する第一選択治療として承認されている(10,11)。しかし、大腸がんの約85%はミスマッチ修復(pMMR)(訳者注:ミスマッチ修復(MMR)は、DNA複製時に生じる誤った塩基対(ミスマッチ)を検出し、修復する細胞の監視システムです)に優れており、マイクロサテライト不安定性低(MSI-L)またはマイクロサテライト安定(MSS)の状態を示す。これらのpMMR-MSI-L/MSS「コールド」腫瘍は、腫瘍変異負荷が低く、ネオアンチゲン提示が少なく、CD8⁺ T細胞浸潤が最小限であり、免疫抑制経路(WNT/β-カテニンおよびTGF-βなど)が活性化していることが特徴であり、PD-1/PD-L1阻害(訳者注:PD-1/PD-L1阻害剤は、がん細胞がT細胞の攻撃を逃れるために利用する「免疫ブレーキ(PD-1とPD-L1の結合)」を解除し、自己の免疫力でがんを攻撃させる免疫チェックポイント阻害薬です)に対してほとんど抵抗性を示す(12)。手術や補助化学療法の進歩にもかかわらず、長期生存率の向上はわずかであり、特にマイクロサテライト安定大腸がんにおいて、大腸がんの治療成績を改善するための効果的な補助療法が喫緊に必要とされていることが浮き彫りになっている。 |
| 現在の大腸がん治療には、化学療法抵抗性、免疫療法抵抗性、放射線毒性、術後合併症などの限界があるため、腸内細菌叢を補完的な治療標的として注目が高まっています。微生物介入は、単独で作用するのではなく、化学療法、免疫療法、放射線療法、手術の有効性を高め、毒性を軽減する可能性があります。例えば、ローズブリア・インテスティナリスなどの特定の腸内常在菌は、放射線誘発性オートファジーを促進することで大腸がん細胞の放射線感受性を高めることが示されており(13)、周術期(訳者注:周術期(しゅうじゅつき)とは、手術が決定した時点から、入院、術前準備、麻酔・手術、術後回復、退院・社会復帰に至る一連の期間を指します。術中だけでなく手術前後の管理を含め、合併症を防ぎ、安全に手術を乗り越え早期回復を目指すための包括的な医療期間です)の腸内細菌叢の構成は、大腸がん切除後の術後回復と長期合併症に関連していることが報告されています(14)。メカニズムの理解が深まるにつれて、腸内細菌叢に基づく戦略を確立された治療レジメンに統合することは、治療成績の向上につながる有望な道筋となります。本レビューでは、まず大腸がんの病因における腸内細菌叢の役割を探り、次に免疫療法、放射線療法、外科的管理における腸内細菌叢の治療的意義について検討します。 |
| 2.大腸がんにおける腸内微生物叢の役割 |
| 腸内微生物叢は、宿主の代謝、免疫、上皮の恒常性維持において基礎的な役割を担っているが、腸内微生物叢の乱れ(デイスバイオシス)が大腸がんの発症要因の一つであるという証拠が蓄積されつつある(5-17)。過去10年間、メタゲノムシーケンス技術の進歩により、大腸がん患者と健常者との大規模な比較が可能となり、がん関連腸内微生物叢と正常な腸内微生物叢を区別する微生物パターンの特定が試みられてきた。しかし、この試みは、健常者における微生物叢の固有の多様性、および食事、生活習慣、地理的要因、抗生物質曝露などによる集団レベルの異質性によって困難を極めている(18,19)。さらに、サンプル採取、保存、DNA抽出における技術的なばらつきも、研究間の比較を複雑にしている(20)。 |
| これらの限界にもかかわらず、多様なコホートと方法論にわたるデータを統合したメタ分析により、大腸がんにおける一貫した微生物の変化が明らかになった(4)。これには、フソバクテリウム、ポルフィロモナス、パルビモナス、ペプトストレプトコッカスなどの口腔由来の分類群の増加と、フェカリバクテリウムやローズブリアなどの有益な酪酸産生属の減少が含まれる(21,22)。微生物プロファイルは、腫瘍の位置と分子サブタイプによっても変化するようである(23)が、ステージ特異的な分類群の増加に関する報告は、研究間で再現性が低いことが示されている(24)。初期の証拠は、腫瘍微生物叢と大腸がんの分子サブタイプとの関連性を確立した。 CMS1 腫瘍(訳者注:CMS1(Consensus Molecular Subtype 1)大腸がんは、「免疫型」とも呼ばれ、MSI-High(マイクロサテライト不安定性高)やBRAF変異、高頻度の突然変異を特徴とする。女性の右側結腸に多く、病理組織学的に悪性度が高いが、免疫チェックポイント阻害薬が効きやすい傾向がある)(典型的には右側、MSI-H、免疫学的に活性)は、フソバクテリウム・ヌクレアタム、パルビモナス・ミクラ、ポルフィロモナス・ジンジバリス などの口腔病原菌が豊富であり、インターフェロン-γ および TNF シグナル伝達のアップレギュレーションも認められた (25)。これを基に、最近の大規模解析では、分類学的および臨床分子プロファイルが異なる 3 つの腫瘍微生物群集サブタイプ(OCS1~3)が特定された。フソバクテリウムが優勢な OCS1 は CMS1 腫瘍に対応し、CIMP 陽性、BRAF^V600E 変異、および MSI 関連の変異シグネチャと関連していた。OCS2 および OCS3 は、左側、CIN 型腫瘍(訳者注:CIN(子宮頸部上皮内腫瘍:Cervical Intraepithelial Neoplasia)は、子宮頸がんの「前がん病変(がんになる前段階の細胞の変化)」です。ヒトパピローマウイルス(HPV)の持続感染が原因で、細胞が異型(正常とは異なる形)になり、そのまま放置するとがん(浸潤がん)に進行する可能性がある状態を指します)および異なる微生物生態系と一致した。マイクロサテライト安定疾患の患者では、OCS1 および OCS3 サブタイプは予後不良と関連していた。これらのデータは、微生物組成と腫瘍表現型との一致を強調しており、大腸がんの生物学的異質性を反映している(23)。機能的には、大腸がん関連微生物叢は、アミノ酸発酵およびポリアミン生合成経路(アルギニンおよびオルニチン代謝など)の増加と、炭水化物分解能力の低下を示す(21)。これらの変化は、二次胆汁酸や短鎖脂肪酸などの微生物代謝産物の産生の変化と関連しており、これらは腫瘍促進性炎症、DNA損傷、および上皮増殖の調節に関与している。しかし、このようなディスバイオシス変化が積極的に腫瘍形成を促進するのか、あるいは単に腫瘍性微小環境への適応反応を反映しているだけなのかは依然として不明であり、原因となる微生物寄与因子を傍観者分類群から区別するために、十分に制御された実験モデルでのメカニズム研究が必要であることを強調している(4)。 |
| さらに、腸内ウイルス叢、真菌叢、古細菌叢は、腫瘍免疫や微生物の相乗効果における役割を示唆する新たな証拠があるものの、まだ十分に研究されていません(26,27)。この分野を発展させるには、記述的および相関的な研究を超えて、腫瘍内微生物が腫瘍の進行、転移、および免疫調節に果たす機能的貢献を明らかにするメカニズム研究に進むことが不可欠です。 |
| 3.大腸がんの発症における特定の微生物の役割 |
| 特定の微生物と大腸がんとの関連性は、50年以上前に、ストレプトコッカス・ガロリティカス亜種ガロリティカス (Sgg) (訳者注:Streptococcus gallolyticussubsp. gallolyticus (Sgg) はグラム陽性、D群細菌(旧ストレプトコッカス・ボヴィス バイオタイプI)で、大腸がんおよび感染性心内膜炎と強い関連がある。これは日和見病原体として働き、高齢患者において菌血症や心内膜炎を引き起こすことが多い。大腸腫瘍との相関性が高いため、ストレプトコッカス・ガロリティカス亜種ガロリティカス菌血症の場合は緊急の内視鏡検査が必要となる。)が大腸がん患者に頻繁に定着することが発見されたことで初めて明らかになりました(28)。宿主の資源利用を制御することで微生物の増殖を調節する機能の低下として定義されるようになったディスバイオシスは、大腸がんにおいて頻繁に観察されます(29,30)。このディスバイオシス状態は、特定の細菌群の過剰増殖によって特徴づけられることが多いです(31)。しかし、個々の微生物の影響は、腸内マイクロバイオームというより広範な生態学的枠組みの中で理解される必要があります。そこでは、免疫代謝シグナル、概日リズム、上皮の完全性、および細菌間の相互作用が、微生物の挙動と宿主の応答を総合的に形成しています(32)。特に、pks⁺大腸菌(訳者注:pks⁺大腸菌(pks-positive E. coli)は、遺伝毒性を持つ物質「コリバクチン」を産生する大腸菌の一種です。この菌は腸内環境においてDNA損傷を引き起こし、特異的な変異シグネチャーを誘導することで、大腸がんの発症や進行リスクを高める可能性が研究で示されています)、フソバクテリウム・ヌクレアタム、バクテロイデス・フラジリスの3つの微生物については、メカニズム研究と相関するヒトデータの両方を通じて大腸がんと一貫して関連付けられていることから、証拠は強力である(図1)(4)。これらの細菌は最もよく特徴付けられているが、他の分類群が潜在的な大腸がんドライバーであることを示唆するデータは急速に蓄積されている(表1)(33)。それにもかかわらず、広範な前臨床証拠があるにもかかわらず、腫瘍発生に先行する微生物の存在を示す縦断的研究や、微生物の根絶ががんリスクを低下させることを示す研究がないため、ヒト大腸がんの原因として明確に確立された微生物または微生物群はない(34)。 |
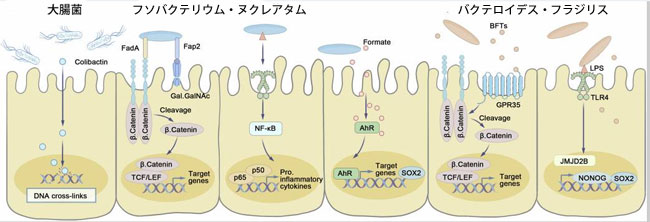 |
図1. 大腸がんの発症に関与する微生物叢関連メカニズム。 大腸菌はコリバクチンを産生し、DNA鎖間架橋と二本鎖切断を引き起こし、独特の変異シグネチャーを示す。 フソバクテリウム・ヌクレアタムのFap2はGal-GalNAc(訳者注:Gal-GalNAcは、主に大腸がんの早期段階や前がん病変で発現する特徴的な二糖類腫瘍マーカーです。正常な大腸組織では発現せず、ガラクトースオキシダーゼ-シッフ法で可視化されます。このマーカーは、がんの初期診断や病態理解に重要です)に結合し、FadAはE-カドヘリン(訳者注:E-カドヘリン(E-cadherin)は、上皮細胞の表面に存在し、細胞同士を密着させるカルシウム依存性の接着分子(糖タンパク質)です。CDH1遺伝子にコードされ、上皮組織の構造維持や組織化に不可欠な働きを持ちます。がんの転移・浸潤時に発現低下することが多く、がん抑制因子として機能します)と結合してWnt–β-カテニンとMYCを活性化し、そのリポ多糖はNF-κB駆動の増殖を誘発する。 F.ヌクレアタム由来のギ酸はAhRを活性化し、侵襲性とSOX2依存性幹細胞性を高める。 バクテロイデス・フラジリスはBFTを分泌してE-カドヘリンを切断し、タイトジャンクションを破壊し、MYCと増殖を誘導する。そのリポ多糖はTLR4を介してJMJD2B、SOX2、NANOGを上方制御し、幹細胞性を促進する。 略語: AhR (アリール炭化水素受容体)、BFT (バクテロイデス・フラジリス毒素)、E-カドヘリン (上皮カドヘリン)、FadA (フソバクテリウム接着因子 A)、Fap2 (フソバクテリウムオートトランスポータータンパク質 2)、Gal-GalNAc (ガラクトース-α1,3-N-アセチルガラクトサミン)、JMJD2B (ジュモンジドメイン含有タンパク質 2B)、LPS (リポ多糖)、MYC v-myc (鳥類骨髄腫症ウイルスがん遺伝子ホモログ)、NF-κB (活性化 B 細胞の核因子カッパ軽鎖エンハンサー)、SOX2 SRY (ボックス転写因子 2)、TLR4 (Toll 様受容体 4。) |
| 表1.大腸がんの発症要因としての微生物の証拠:主要細菌、その他の細菌、ウイルス叢、真菌 |
 |
 |
 |
マウスモデルのエビデンス欄に「限定的」と記載されている場合、その微生物は生体内で調査されているものの、エビデンスは予備的なものであり、作用機序の明確さが限られていたり、腫瘍形成の結果が一貫していなかったり、複数の大腸がんモデルにおける検証が不十分であったりすることを示しています。 略語:AOM (アゾキシメタン)、DSS (デキストラン硫酸ナトリウム)、APC^Min/+Apc^Min (ヘテロ接合マウスモデル)、Zeb2^IEC-Tg/+ (腸管上皮細胞特異的 Zeb2 トランスジェニックマウス)、BRAF^V600E Lgr5^CreMinBraf^V600E Lgr5 (プロモーター制御下の変異マウス)、Germ-free Apc^Min/+ (無菌 Apc^Min マウス)、ETBF (腸管毒素原性バクテロイデス・フラジリス)、pks+E. coli(コリバクチンをコードするpksゲノムアイランドを有する大腸菌株)、Fn(フソバクテリウム・ヌクレアタム)、IDA(インドールアクリル酸)、AHR(アリール炭化水素受容体)、ALDH1A3(アルデヒド脱水素酵素1ファミリーメンバーA3)、FSP1(フェロトーシス抑制タンパク質1)、CoQ10(コエンザイムQ10)、ROS(活性酸素種)、IL-17(インターロイキン-17)、Sgg(ストレプトコッカス・ガロリティカス亜種ガロリティカス)、Apc^+/1638NA(大腸がんマウスモデル)。 |
| 3.1.大腸がんの発症における主要な細菌 |
| 3.1.1.大腸菌 |
| pksゲノムアイランドを有する大腸菌株(pks⁺大腸菌と表記)は、コリバクチン産生に関わる生合成機構をコードしている(35)。コリバクチンはDNA二本鎖切断を引き起こし、様々な変異誘発性病変を生じさせる(36,37)。蓄積された証拠は、pks⁺大腸菌が大腸がんにおいて過剰に存在し、そのコリバクチンがマウスモデルにおける腸管腫瘍形成に寄与することを示している(38)。特に、大腸がんになりやすいマウスを用いた実験では、pks⁺大腸菌の定着が、CD3⁺およびCD8⁺腫瘍浸潤リンパ球を減少させることで免疫抑制的な腫瘍微小環境(TME)を促進し、抗PD-1療法への反応を阻害することが示されている(39)。さらに、ヨーロッパのコホート研究では、pks⁺大腸菌と腸管毒素原性バクテロイデス・フラジリス(ETBF)の両方に対する血清陽性が大腸がん発生率の上昇と関連付けられ、腫瘍発生開始における協力的な役割が示唆された(40)。最近の研究では、腸管病原性大腸菌の病原性は微生物環境によって影響を受けることも強調されている。特に、アッケルマンシア・ムシニフィラなどのムチン分解細菌は、粘液バリアを破壊して宿主由来の栄養素へのアクセスを可能にし、食事制限条件下での定着を促進することにより、大腸菌の上皮ニッチへの侵入を促進する(41)。 |
| これを基に、pks⁺大腸菌は、I型線毛上のFimHとF9線毛上のFmlHという2つのレクチン様接着因子を用いて、それぞれ異なるグリカンリガンド(末端D-マンノース抗原とT/Tn抗原)に結合し、腫瘍上皮の空間的に分離されたコロニー形成を統制することが示されています。いずれかの接着因子を欠損させると、マウスモデルにおける大腸がんの進行が著しく抑制されます(42)。同時に、コリバクチン誘導DNA損傷は、化学療法耐性のがん幹細胞を選択し、上皮間葉転換を活性化し、NANOGとOCT-3/4の発現を亢進させ、脂質滴蓄積を伴う代謝再プログラミングを促進する老化関連分泌表現型を引き起こし、CD8⁺ T細胞の浸潤をさらに阻害し、化学療法耐性と免疫回避の両方を促進します(43,44)。 |
| 3.1.2.フソバクテリウム・ヌクレアタム |
| 6つのコホートから得られた1375の糞便サンプルの包括的なメタゲノム解析により、フソバクテリウム・ヌクレアタム(Fn)がすべての大腸腫瘍部位で濃縮されていることが確認された(45)。新生児期にApcMin/+マウスにフソバクテリウム・ヌクレアタム株Fn7-1を接種すると、定着抵抗性が克服され、腫瘍発生前に大腸におけるIL-17Aの発現亢進が誘導され、腸管腫瘍形成が促進される(46)。大腸内では、フソバクテリウム・ヌクレアタムは腸管深部の陰窩に侵入し、シングルセル転写解析により、上皮細胞を再プログラムし、腫瘍開始細胞へと過剰増殖するLY6A⁺再生幹細胞を活性化することが示されている(47)。分子レベルでは、そのフソバクテリウム・ヌクレアタムがE-カドヘリンに結合してIκBαの分解とNF-κBシグナル伝達を誘発し、分泌されたADP-ヘプトースがALPK1と結合して上皮細胞からのCXCL8放出を誘導します(48,49)。生体内では、フソバクテリウム・ヌクレアタムまたはその代謝産物であるギ酸が腫瘍発生率とTh17の増殖を増加させ、CX3CR1⁺PD-L1⁺食細胞を動員して微小環境を再構築します(50,51)。 |
| 最近の研究では、大腸がんにおける免疫チェックポイント療法の結果に対するフソバクテリウム・ヌクレアタムの相反する効果が報告されている。PD-L1阻害の前臨床モデルでは、フソバクテリウム・ヌクレアタムはcGAS–STINGシグナル伝達を活性化し、IFN-γ⁺ CD8⁺ T細胞の浸潤を増加させ、それによって腫瘍を免疫療法に感作させた(52)。同様に、マイクロサテライト安定型大腸がん(MSS CRC)では、腫瘍内フソバクテリウム・ヌクレアタムはCD8⁺ T細胞におけるHDAC3/8の酪酸を介した阻害によって抗PD-1効果を高め、TBX21の発現上昇とT細胞疲弊の軽減につながった。酪酸合成を欠損した株はこの利点を失い、腫瘍内フソバクテリウム・ヌクレアタム濃度が高いほど良好な反応が予測された(10)。逆に、腸管腔におけるフソバクテリウム・ヌクレアタムの定着は免疫療法抵抗性と関連付けられています。転移性大腸がんでは、フソバクテリウム・ヌクレアタムの増加はコハク酸産生と相関しており、これはcGAS-インターフェロン-β軸を抑制し、CD8⁺ T細胞の遊走を阻害しました。メトロニダゾールを用いた抗生物質除去はこれらの効果を逆転させ、PD-1感受性を回復させました(53)。 |
| さらに、KRAS p.G12D変異大腸がん(訳者注:大腸がんの約15%に見られるKRAS p.G12D変異は、高頻度なKRAS変異サブタイプで、70歳以下の若年男性、低分化型、高度の血管・リンパ管侵襲と関連する予後不良因子。抗EGFR抗体薬が効きにくく、従来の抗がん剤への耐性や、血栓症リスク(VTE)を高める特徴がある)では、腫瘍に定着したフソバクテリウム・ヌクレアタムがDHX15依存性ERK/STAT3シグナル伝達を介して腫瘍形成を促進する一方、パラバクテロイデス・ディスタソニスの標的濃縮はフソバクテリウム・ヌクレアタムを置き換え、腫瘍の進行を弱めることができ、マイクロバイオータ調節の治療的可能性を強調している(54)。フソバクテリウム・ヌクレアタムはまた、BCL2–GSDMEおよびβ-カテニン–GPX4経路を介してパイロトーシスおよびフェロトーシスを阻害することにより、化学療法耐性を促進する(55,56)。メトホルミンはMYC/miR-361-5p抑制を介してフソバクテリウム・ヌクレアタム誘導幹細胞性および薬剤耐性を逆転させる(57)。さらに、抗菌ペプチドBr-J-Iはフソバクテリウム接着因子Aを介した接着を阻害し、5-FU(訳者注:フルオロウラシル(5-FU)は、DNA・RNAの合成を阻害してがん細胞を死滅させる、胃がんや大腸がんなどの固形がんに広く用いられる古典的な抗がん剤(代謝拮抗剤)です)の有効性を高める(58)。これらの研究結果は、フソバクテリウム・ヌクレアタムが大腸がんの進行、免疫回避、および治療抵抗性において多面的な役割を果たしていることを強調し、マイクロバイオータを標的とした治療軸としてのフソバクテリウム・ヌクレアタムの可能性を浮き彫りにしている。 |
| 3.1.3.バクテロイデス・フラジリス |
| バクテロイデス・フラジリスは、大腸内細菌叢の約0.1~0.5%を占め、その一部は亜鉛依存性メタロプロテアーゼ毒素であるバクテロイデス・フラジリス毒素(BFTまたはフラジリシン)をコードする病原性アイランドを保有している(59)。腸管毒素原性バクテロイデス・フラジリスは大腸がんで高頻度に見られ、バクテロイデス・フラジリス毒素によるE-カドヘリンの切断を介して腫瘍形成を促進する。切断されたE-カドヘリンはβ-カテニンとNF-κBまたはWntシグナル伝達経路を活性化し、上皮透過性を増加させ、粘膜免疫応答を誘発する。さらに、TLR4の活性化を介してがん幹細胞特性を促進する(60,61)。 in vitro および in vivo において、腸管毒素原性バクテロイデス・フラジリスによる大腸がん細胞株 (SW480、HCT-116) の処理は、miR-139-3p のダウンレギュレーションにより増殖、浸潤、および遊走を促進し、miR-139-3p の過剰発現によりその効果が逆転し、メカニズム的には 腸管毒素原性バクテロイデス・フラジリスは HDAC3(訳者注:HDAC3(ヒストン脱アセチル化酵素3)は、DNAのパッケージングに関わるヒストンタンパク質からアセチル基を取り除く酵素です。この作用によりクロマチン構造が凝集し、特定の遺伝子の発現が抑制されます) をアップレギュレーションし、miR-139-3p を抑制して悪性化を促進します。HDAC3 のノックダウンまたは miR-139-3p (訳者注:miR-139-3pは、ヒトの11番染色体(11q13.4)に位置するマイクロRNAの一種です。主にがん抑制因子(腫瘍抑制因子)として機能することが多くの研究で示唆されています)の回復は、腸管毒素原性バクテロイデス・フラジリスによる 大腸がんの進行を弱め、異種移植における腫瘍の増殖を減少させます (62)。腸管毒素原性バクテロイデス・フラジリスおよび バクテロイデス・フラジリス毒素は腸管バリアを破壊し、タイトジャンクションタンパク質 (MUC2、オクルディン、ZO-1) を損ない、透過性を増加させ、TEER および絨毛の完全性を低下させ、STAT3/ZEB2 軸を活性化して EMT および SW480 の悪性化を促進します。これらの効果、および AOM/DSS モデルにおける腸管毒素原性バクテロイデス・フラジリス によって悪化した腫瘍負荷とバリア損傷は、STAT3 阻害剤 ブレビリンAまたは ZEB2 ノックダウンによって軽減されます (63)。KRAS 変異型大腸がん(訳者注:KRAS変異型は、膵がん(95%以上)、大腸がん(約40%)、肺がん(約10-30%)などで高頻度に見られる、細胞増殖を制御する遺伝子の異常です)では バクテロイデス の存在量が増加し、変異型 KRAS は miR-3655 を下方制御し、それによって SURF6 を上方制御し、IRF7 の核移行と IFNβ 転写を阻害して腫瘍内腸管毒素原性バクテロイデス・フラジリスコロニー形成を促進します。miR-3655/SURF6/IRF7/IFNβ 軸を標的にすると、IFN-β を介した 腸管毒素原性バクテロイデス・フラジリスクリアランスが回復し、新しい治療経路が提供されます(64)。ヒトの研究では、健康な人と比較して大腸腫瘍患者で腸管毒素原性バクテロイデス・フラジリスの有病率が高いことが報告されていますが、濃縮に関連する腫瘍形成の特定の段階はコホートによって異なります(65)。 腸管毒素原性バクテロイデス・フラジリス処理細胞由来のエクソソームは、miR-149-3pの発現を抑制することでTh17分化と大腸がん細胞増殖を増強し、腸管毒素原性バクテロイデス・フラジリス/miR-149-3p経路が腸管毒素原性バクテロイデス・フラジリス関連腸炎および大腸がんの治療における有望な標的となる可能性を示唆している(66)。予備的な証拠は、腸管毒素原性バクテロイデス・フラジリスがIFNγ産生CD8⁺T細胞を腫瘍に動員することで抗PD-1免疫療法を強化する可能性があることを示唆しているが、このメカニズムとその治療可能性を明らかにするにはさらなる研究が必要である(67)。 |
| 3.2.大腸がんに関与するその他の細菌群 |
| 大腸菌、フソバクテリウム・ヌクレアタム、バクテロイデス・フラジリスといったよく知られた細菌以外にも、近年の研究では、あまり研究されていない細菌種も大腸がんの発症に影響を与える可能性が示唆されている。これらの知見は、大腸がんにおける腸内細菌叢の複雑かつ動的な役割を浮き彫りにし、さらなる研究への道を開くものである。 |
| 3.2.1.カンピロバクター属 |
| 主に胃腸炎と関連付けられているカンピロバクター・ジェジュニは、DNA二本鎖切断を引き起こす遺伝毒性物質である細胞致死性膨張毒素(CDT)を産生することで、腸管腫瘍形成に寄与する可能性のある菌として注目されている(68)。ApcMin/+マウスモデルを用いた実験では、細胞致死性膨張毒素活性が発がんを増幅することが示されている(69)。興味深いことに、炎症性腸疾患(IBD)に関連する口腔病原菌であるカンピロバクター・コンシサスも大腸がんとの関連が指摘されており、カンピロバクター属が消化管悪性腫瘍に広く関与している可能性が示唆されている(70)。 |
| さらに、メカニズム研究により、カンピロバクター・ジェジュニ由来の細胞致死性膨張毒素はJAK2–STAT3–MMP9経路を活性化し、肝臓および肺モデル、ヒト結腸組織片、患者由来腫瘍様組織においてマトリックス分解と腫瘍細胞の浸潤性を高めることにより大腸がん転移を促進することが明らかになった(71)。cdtBの除去または精製CdtBタンパク質による阻害はこの効果を消失させ、腫瘍内細胞致死性膨張毒素が転移拡散を促進する中心的な役割を担い、治療標的として有望であることを強調している(71)。 |
| 3.2.2.クロストリジオイデス・ディフィシル |
| 従来、抗生物質関連下痢症の原因菌として知られてきたクロストリジオイデス・ディフィシルは、大腸がんの潜在的な原因菌として特定されている(79)。ある疫学分析では、クロストリジオイデス・ディフィシルと大腸がん発生率の間に逆相関が認められたという逆説的な結果も報告されている(80)が、Searsらはマウスモデルにおいて、毒素産生性クロストリジオイデス・ディフィシルの慢性的な定着が、TcdB(クロストリジウム・ディフィシル毒素B)依存的なWntシグナル伝達の活性化、活性酸素種の産生、および骨髄系細胞の活性化とIL-17分泌性自然リンパ球の浸潤を特徴とする腫瘍促進性粘膜免疫応答を介して、大腸がんの発生を促進することを確認した(81)。 |
| これらの経路に加えて、最近の研究結果では、クロストリジウム・ディフィシル毒素Bが腸管上皮細胞でピリンインフラマソームを活性化し、ASCオリゴマー形成と強力な炎症反応を引き起こすことも示されています(82)。この活性化により、クローディンやオクルディンなどのタイトジャンクションタンパク質が破壊され、上皮バリアの完全性が損なわれ、大腸炎が促進されます(83)。これらの知見から、クロストリジウム・ディフィシル毒素Bは上皮および免疫シグナル伝達を再プログラムするだけでなく、粘膜バリアの構造も損ない、総合的に腫瘍に有利な微小環境に寄与していることが明らかになりました。 |
| 3.2.3.モルガネラ・モルガニー |
| 新たな証拠は、炎症性腸疾患(IBD)および大腸がん患者に多く見られるグラム陰性細菌であるモルガネラ・モルガニーが、遺伝毒性物質の供給源であることを示唆している。モルガネラ・モルガニーが産生するインドリミンなどの低分子化合物は、前臨床モデルにおいてDNA損傷を誘発し、腫瘍形成を促進する(84)。これらの知見は、微生物代謝産物の産生とがんの進行を結びつけ、腸内細菌叢と大腸がんの関連性に新たな複雑さを加えるものである。 |
| 3.2.4. ストレプトコッカス・ガロリティカス亜種ガロリティカス |
| ストレプトコッカス・ガロリティカス亜種ガロリティカスは結腸直腸がん組織に高頻度で存在し、疫学研究において結腸直腸腫瘍形成と強い関連性が認められています(85)。大腸がんとの関連性は認められているものの、ストレプトコッカス・ガロリティカス亜種ガロリティカスが腫瘍微小環境(TME)においてがんの進行を促進する因子なのか、あるいは単なる傍観者なのかは依然として不明です。実験モデルでは、ストレプトコッカス・ガロリティカス亜種ガロリティカスはガロシン産生などニッチ適応機構を介して大腸がんの進行を促進する可能性が示唆されています。ガロシンは競合する腸球菌を阻害します(86,87)。しかし、腫瘍発生におけるストレプトコッカス・ガロリティカス亜種ガロリティカスの役割を確立するには、より確固たる証拠が必要です。 |
| 3.2.5.アッケルマンシア・ムシニフィラ |
| ムチン分解性共生細菌であるアッケルマンシア・ムシニフィラは、大腸がんに対して多面的な効果を発揮します。大腸がん患者ではその存在量が一般的に減少しており、補充することでTLR2–NF-κB–NLRP3経路を介してM1様マクロファージを増加させ、腫瘍形成を抑制します。このメカニズムは抗腫瘍効果に不可欠です(88)。また、PD-L1の発現を抑制するAmuc_1434を含む外膜小胞、およびがん細胞におけるH3K14アセチル化とHSP70の発現亢進を誘導するアセチルトランスフェラーゼAmuc_2172を介して、CD8⁺ T細胞を介した免疫応答を促進します(89,90)。さらに、アッケルマンシア・ムシニフィラはトリプトファン–AhR–β-カテニンシグナル伝達を阻害し、化学的および遺伝的大腸がんモデルの両方において腫瘍抑制に寄与します(91)。しかし、過剰定着はムチンを分解しタイトジャンクションタンパク質を減少させることで粘膜バリアを破壊し、大腸がんの進行を悪化させる可能性がある(92)。さらに、アッケルマンシア・ムシニフィラは粘液層を薄くすることで病原性大腸菌による栄養素の貪食を促進し、食事制限下での協調的な代謝適応を強調している(41)。臨床的には、その減少は腸内細菌叢の異常と大腸がん患者の生存率の低下に関連しており、治療標的と予後バイオマーカーの両方としての可能性を強調している(93)。 |
| 3.2.6.クレブシエラ属菌 |
| クレブシエラ属菌は、多因子的なメカニズムを介して大腸がんに関与していることが示唆されている。歯周病時に増殖する口腔内のクレブシエラ属菌は、腸管に移行し、インフラマソームの活性化とTh17細胞の動員を介して大腸がんを促進する可能性がある(94)。マウスモデルでは、クレブシエラ・アエロゲネスは、粘膜バリアを破壊し、炎症反応と微生物叢の異常を誘発することで、大腸炎関連腫瘍形成を悪化させる(95)。大腸がん患者から分離されたクレブシエラ・ニューモニエの臨床分離株は、ポリケチド合成酵素遺伝子とシデロフォア遺伝子を保有していることが多く、in vitroで腫瘍細胞の増殖を促進する(96)。メンデルランダム化解析では、クレブシエラ属菌の存在量と大腸がんリスクとの関連性が、特にCD4⁺T細胞経路を介した免疫調節を介してさらに示されている(97)。これらの知見は、クレブシエラ属菌が大腸がん発生における重要な口腔腸内病原菌であることを示している。 |
| 3.2.7.大腸がんにおける真菌とウイルスの関与 |
| 腸内細菌叢は細菌が大部分を占めるが、ウイルスや真菌などの非細菌性成分も大腸がんの発症に関与している(98)。シーケンス技術とメタゲノム解析の進歩により、これまで十分に研究されてこなかったこれらの微生物群に光が当てられ、異種間相互作用やディスバイオシスを介した潜在的な関与が明らかになってきている。 |
| 大腸がん患者のウイルスゲノムの変化は、サイフォウイルス科とマイオウイルス科 の集団の変化とミクロウイルス科の増加によって特徴づけられる(27)。主にバクテリオファージによって駆動されるウイルスゲノムの動態は、腸内細菌群集を制御し、マイクロバイオームの安定性を支えている。ヘリコバクター・ピロリ感染Apc^+/1638Nマウスでは、エンテロコッカス・ファエカリスなどの大腸がん関連細菌に感染すると予測されるものを含む温和性ファージの初期段階のウイルスゲノムの拡大が観察された。共起ネットワーク解析により、腫瘍発生に先行する強いウイルスと細菌の関連性が明らかになり、ヘリコバクター・ピロリ誘導プロファージ活性化とそれに続くファージ増殖が細菌生態系を再構築することによって大腸がん発生を促進する可能性があることが示唆された(99)。細菌生態系への影響とは別に、カウドウイルス由来のファージは上皮バリアを突破して結腸細胞に入り込み、大腸がんモデルで腫瘍の増殖と浸潤性を高める炎症誘発シグナルを誘発する可能性がある100,101。機能的には、大腸がん患者のウイルスゲノムは、L-メチオニンや酢酸などのウイルス代謝産物(大腸がん細胞の増殖を阻害し、粘膜恒常性を維持することが知られている化合物)の枯渇とともに脂肪酸生合成経路の増加も示しており、ウイルスゲノムの変化が腫瘍リスクに直接影響を与える可能性があることを示している(26,102)。 |
| 真菌は、存在量が少なく個体間のばらつきが大きいにもかかわらず、大腸がんにおいて、担子菌類と子嚢菌類の比率の増加や、多様性の高い真菌の増加など、特徴的な変化を示します(103–105)。真菌は、バイオフィルム形成、マイコトキシン(アフラトキシン、カンジダリシンなど)の分泌、IL-1βやIL-17などの炎症性サイトカインの誘導、上皮バリアの完全性の破壊などを通じて腫瘍形成に寄与し、全体として腫瘍促進性で炎症を起こしやすい微小環境を育みます106。例えば、カンジダ・トロピカリスは、骨髄由来抑制細胞のNLRP3インフラマソームを活性化して過剰なIL-1β放出を促し、それがMDSC(訳者注:骨髄由来抑制細胞(MDSC)は、がんや慢性炎症下で骨髄から誘導される、T細胞などの免疫細胞の活性を強力に抑制する未熟な骨髄系細胞集団です。がんの成長・転移を促進し、化学療法抵抗性にも関与するため、新たな癌治療の標的として注目されています)を介した免疫抑制を増幅し、大腸がんの進行を促進します(107)。予備的な証拠によると、霊芝胞子と桑黄ポルス・バニニイの複合エタノール抽出物は、CYP24A1–VDRおよびTERT–Wntシグナル伝達経路を介して抗大腸がん効果を発揮する可能性がある(108)。さらに、共生細菌は抗真菌毒素や代謝産物を産生し、宿主の免疫経路に関与することで真菌の過剰増殖を抑制し、真菌と細菌の相互作用自体が独自の免疫応答を引き起こす可能性がある(109)。 |
| 4. 大腸がん臨床試験におけるマイクロバイオーム調節因子の役割 |
| 現在の標的療法や免疫療法は、免疫抑制性の腫瘍微小環境(TME)やでスバイオシスによる薬剤耐性のため、効果が限定的である。糞便微生物叢移植(FMT)、プロバイオティクス/プレバイオティクス/シンバイオティクス療法、生菌製剤(LBP)を含むマイクロバイオーム調節剤(MM)は、パラダイムシフトをもたらす補助剤として登場した(110)。これらの薬剤は腸内細菌叢の恒常性を回復させ、複数の作用機序を介して抗腫瘍免疫を増強し、あらゆるがんにおいて前例のない治療可能性を示している(111)。本研究では、大腸がん治療における重要なギャップを解明するために、進化するマイクロバイオーム調節剤臨床試験の状況を概説するとともに、新たな前臨床的知見を橋渡しして治療研究と開発を最適化する。 |
| 我々は、ClinicalTrials.gov、WHO国際臨床試験登録プラットフォーム、北米、ヨーロッパ、アジアの各国登録機関など、世界中の数十の国と地域の臨床試験データを統合する権威あるプラットフォームであるTrialtroveデータベース(https://clinicalintelligence.citeline.com)を包括的に検索した。2025年6月30日現在、関連する研究を特定するために、検索戦略「(疾患は腫瘍学:結腸直腸) AND (作用機序はマイクロバイオーム調節剤)」を適用した。分析パラメータには、試験フェーズとステータスの分布、マイクロバイオーム調節剤タイプ、スポンサー分類、疾患ステージと治療ライン、主要/副次エンドポイント、および併用戦略が含まれた。2人の独立した研究者が、非構造化情報の抽出、データギャップの解決、分類バイアスの最小化など、取得したすべての記録と分析結果を体系的にレビューおよび検証し(図2)、方法論の厳密性と厳格な品質管理を確保した。これらの手順を踏んだ後に残るいかなる制約も、本研究の全体的な解釈や観察された傾向には影響を与えない。 |
 |
 |
 |
 |
 |
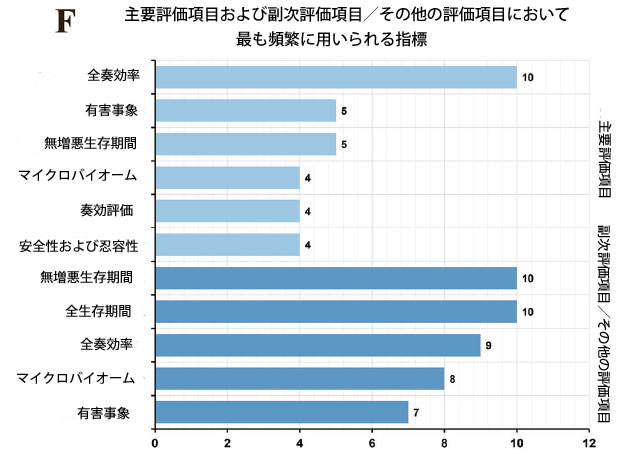 |
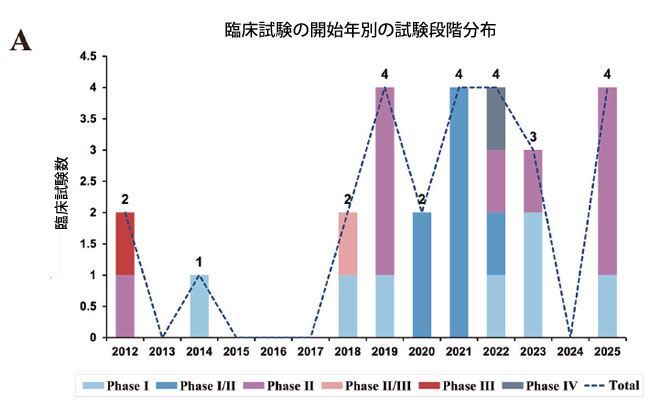
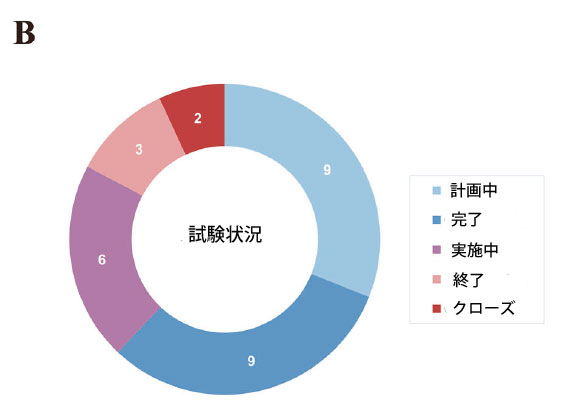
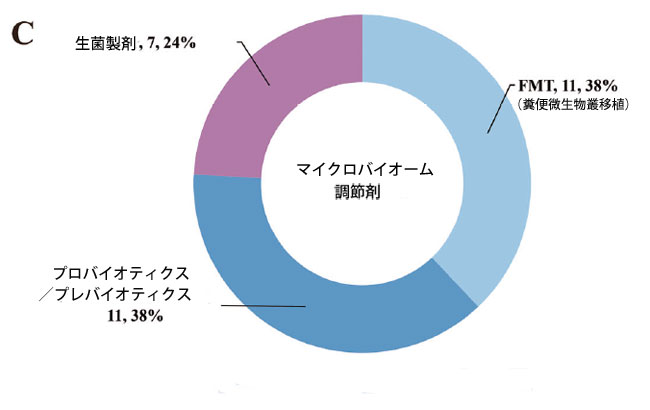
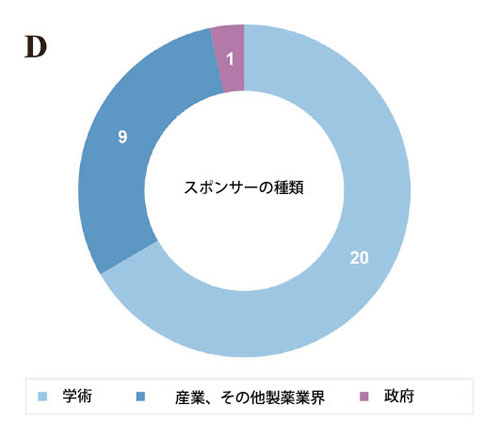
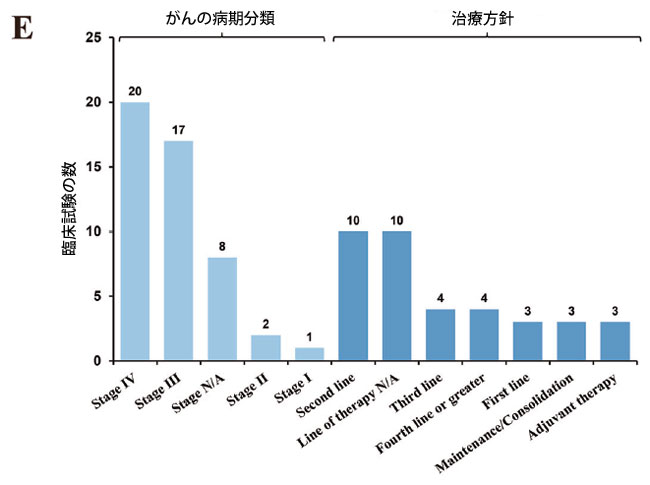
図2.大腸がん治療におけるマイクロバイオーム調節剤の臨床研究の概観。 A 臨床試験の開始年別の試験段階分布。 B 臨床試験の試験状況分布。 C 臨床試験のマイクロバイオーム調節剤タイプの分布。 D 臨床試験のスポンサータイプの分布。 E 臨床試験のがん病期と治療ラインの分布。 F 臨床試験のエンドポイント分布。 |
| 現在までに、大腸がんにおけるマイクロバイオーム調節剤を評価するために29の試験が実施されており、糞便微生物叢移植(n = 11)、プロバイオティクス/プレバイオティクス療法(n = 11)、生菌製剤(n = 7)に及んでいます(表S1/図2C)。パイプラインでは第II相試験が大部分を占め(n = 9)、次いで第I相(n = 7)、第I/II相(n = 7)となっています(図2A)。ほとんどの試験は計画段階にあり、完了した試験もかなりの割合を占めています(図2B)。この分野では学術スポンサーが大部分を占め、次いで企業主導の試験となっています(図2D)。進行大腸がん患者の後期治療が、この新しい治療法の主な適応症となっています(図2E)。そして、主要評価項目は現在、大腸がん患者におけるこの治療戦略の全奏効率(ORR)に主に焦点を当てており、いくつかの新しいマイクロバイオーム指標が革新的に適用されています(図2F)。さらに、大腸がんの標準治療(SOC)レジメンとの併用は、主流の臨床トレンドとなっている(表S1)。より重要なことに、いくつかの臨床試験では良好な結果が示されており、大腸がん治療における多様なマイクロバイオーム調節戦略の有望な治療可能性を示唆している。 |
| 大腸がんにおけるマイクロバイオーム調節剤の臨床開発パイプラインは依然として初期段階が中心ですが、一部の研究では、記述的エンドポイントを超えた生物学的に意味のあるシグナルが示され始めています。RENMIN-215試験では、難治性MSS転移性大腸がん患者(訳者注:難治性MSS(マイクロサテライト安定型)転移性大腸がんは、免疫チェックポイント阻害薬が効きにくく治療困難な病態ですが、新たな治療戦略が進行中です。主にFTD/TPI+ベバシズマブの標準治療に加え、新規血管新生阻害薬と免疫療法の併用、BRICS療法などの複合的治療が有望な結果を示しています)を対象に、健常ドナーからの糞便微生物叢移植を抗PD-1抗体ティスレリズマブおよびVEGFR阻害剤(訳者注:VEGFR阻害薬(血管内皮増殖因子受容体阻害薬)は、がん細胞に栄養を送る血管新生を抑制し、腫瘍の成長や転移を防ぐ抗がん剤)フルキンチニブと併用しました。この研究では、客観的奏効率20%、疾患制御率(DCR)95%、無増悪生存期間中央値(mPFS)9.6ヶ月、全生存期間中央値(mOS)13.7ヶ月という、この抵抗性集団ではまれにしか見られない数値が報告されました(112)。注目すべきは、奏効患者では微生物多様性の増加と持続的な微生物叢生着が見られ、腸内生態系の回復が腫瘍微小環境の調節を介して免疫療法抵抗性を克服する可能性があることを示唆している点です(113)。 |
| より広範には、固形腫瘍全体にわたるメタアナリシスでは、糞便微生物叢移植と免疫チェックポイント阻害剤(ICI)を組み合わせることで、免疫療法単独と比較して客観的奏効率が向上することが示されており、初期段階の試験では統合全奏効率が43.1%対36.9%となっています(114)。メカニズム研究では、アッカーマンシア・ムシニフィラ、フィーカリバクテリウム・ プラウスニッツィイ、バクテロイデス・ユニフォニスなどの主要な共生細菌が、抗原提示の増加、インターフェロン-γ産生、制御性T細胞の調節を通じて抗腫瘍免疫活性化を高める役割を担っていることが示唆されています(115)。 |
| これらの有望な結果にもかかわらず、これまでのマイクロバイオーム調節剤試験のほとんどは、進行した、高度な前治療を受けた患者を対象としており、微生物叢の異常と慢性的な抗原刺激がCD8⁺ T細胞の疲弊を引き起こし、マイクロバイオームに基づく介入の効果を弱める可能性がある(116)。さらに、多くのプロトコルに統合された微生物、代謝、または免疫学的バイオマーカーがないため、メカニズムの解釈と患者の層別化が制限されている。これらのギャップに対処するには、予測シグネチャを特定し、合理的な組み合わせを最適化するために、マイクロバイオームプロファイリング、機能的読み取り値(例:短鎖脂肪酸産生)、および免疫相関を組み込んだ試験設計が必要となる。 |
| 本分析は、結腸直腸がんにおけるマイクロバイオーム調節の臨床研究の急成長ぶりを包括的に示しており、糞便微生物移植、プロバイオティクス/プレバイオティクス、および生菌製剤を評価する29件の試験が行われている。これらの知見は、大腸がんにおけるパラダイムシフトをもたらす補助療法としてのマイクロバイオーム調節の臨床応用への可能性を強調するものである。今後の取り組みでは、最適なマイクロバイオーム調節剤併用療法の最適化、マイクロバイオームに基づくバイオマーカーの検証、そして臨床応用を加速させるためのより広範な患者集団への試験拡大を優先すべきである。 |
| この研究には長所がある一方で、いくつかの限界もある。治療分野に特化した専門アナリストのチームによってキュレーションされたTrialtroveデータベースは、グローバルな臨床試験情報の包括的かつ権威ある情報源として広く認識されており、数多くの査読付き論文(117~119)に貢献している。しかしながら、データ更新の遅延や分類の不一致が、試験データの網羅性に影響を与える可能性がある。これに対処するため、2名の研究者が追加で配置され、さまざまな国や地域の公式臨床試験登録簿、学会抄録、出版文献など、複数のデータソースをタイムリーに追跡することで、主要な記録を手動で検証した。これらの措置は、利用可能なリソースの制約内でデータ網羅性を向上させることを目的としていた。 |
| 5.大腸がん治療における腸内細菌叢の役割 |
| 5.1.化学療法への治療的意義 |
| 近年の研究により、腸内細菌叢は、微生物の移行、免疫調節、代謝、酵素分解、生態系多様性の低下など、様々なメカニズムを介して、5-フルオロウラシル(120)、シクロホスファミド(121)、オキサリプラチン(122)などの特定の化学療法剤の抗がん作用に影響を与える可能性が示唆されている(123)。また、腸内細菌代謝産物、特に酪酸は、腫瘍微小環境内のCD8+ T細胞の機能を調節することで、オキサリプラチンの有効性を高める可能性がある(124)。in vitro研究では、乳酸菌が酪酸(125)、γ-アミノ酪酸(126)、細胞外小胞(127)などの代謝産物を分泌することで、大腸がんにおける5-フルオロウラシルおよびイリノテカンの活性を高めたり、耐性を抑制したりすることが示されている。ビフィドバクテリウム・ブレーベDM8310、ラクトバチルス・アシドフィルスDM8302、ラクトバチルス・カゼイDM8121、およびストレプトコッカス・サーモフィルスDM8309を含むDM#1混合物は、5-フルオロウラシル治療後の腸管の完全性を回復し、炎症性サイトカインの活性化を減少させることが示されている(128)。ラクトバチルス・アシドフィルス、ラクトバチルス・パラカゼイ、ラクトバチルス・ラムノサス、およびビフィドバクテリウム・ラクティスを5-フルオロウラシルと併用してプロバイオティクスとして使用した場合にも同様の有益な効果が観察されている(129)。さらに、L.ラムノサスGGは、5-フルオロウラシル治療を受けている150人の大腸がん患者のコホートにおける下痢の重症度の軽減と関連していた(130)。また、ビフィドバクテリウム・インファンティスは、スプラーグ・ドーリーラットにおいて、Th1およびTh17の活性化を抑制しつつ細胞傷害性制御性T細胞(CD4+ CD25+ Foxp3+)の活性を高めることにより、化学療法誘発毒性(5-フルオロウラシルおよびオキサリプラチンによる)を軽減する可能性があることが研究で示唆されている(131)。最近の証拠は、腫瘍に定着するバクテロイデス・フラジリスが、SusD/RagB依存的なNotch1シグナル伝達の活性化を介して5-フルオロウラシルおよびオキサリプラチンに対する耐性を媒介し、最終的にEMTおよび幹細胞性の獲得に至ることを示している(132)。Langらは、プレバイオティクスであるキシラン-ステアリン酸複合体(SCXN)を用いてカペシタビンを搭載したナノ粒子を開発した。このキシラン-ステアリン酸複合体ナノ粒子は、抗腫瘍免疫を大幅に強化し、遊離カペシタビンと比較して腫瘍抑制率を5.29%から71.78%に増加させた(133)。 |
| 腸内細菌叢は抗腫瘍効果を高めるだけでなく、化学療法に伴う毒性にも影響を与える。がん患者の治療中に頻繁に起こる合併症の一つに、腸粘膜炎と下痢がある(134,135)。イリノテカンの活性代謝物であるSN-38は、肝臓でグルクロン酸抱合によって解毒され、胆汁を介して腸管に排泄される(136)。しかし、腸内細菌はβ-グルクロニダーゼを産生することでSN-38を再活性化し、腸管損傷や重度の下痢を引き起こす(137)。この再活性化を阻害する選択的阻害剤を使用することで、マウスにおける関連毒性を予防できる可能性があり、微生物活性を変化させて化学療法の有害な副作用を軽減する戦略となる(138)。 |
| 5.2.免疫療法の治療的意義 |
| 免疫療法はがん治療の要として確立され、様々な種類のがんに対して有効性を示しています(139)。免疫チェックポイント阻害剤(ICI)は、T細胞活性化に対する抑制シグナルを解除することで、腫瘍反応性T細胞が強力な抗腫瘍応答を誘導できるようにします(140)。しかしながら、免疫チェックポイント阻害剤は一般的に大腸がんには効果がなく、ミスマッチ修復欠損またはMSI-H腫瘍を有する患者のごく一部(約5%)にのみ有効です(141,142)。腸内細菌叢は免疫療法における効果的な免疫応答に不可欠であり、PD-1/PD-L1およびCTLA-4経路を標的とする免疫チェックポイント阻害剤の有効性に影響を与える可能性があります143-145。 アッカーマンシア・ムシニフィラ143、バクテロイデス フラジリス145、ビフィドバクテリウム属146、ユウバクテリウム・リモサム 147、フィーカリバクテリウム属148、アリスティペス・シャヒイ122などの特定の細菌は、免疫療法による治療成績の向上と関連付けられています。しかし、CTLA-4とPD-1は腫瘍浸潤制御性T細胞(Treg)にも高発現しているため、これらの阻害は逆説的に免疫調節を阻害し、自己免疫を悪化させたり、治療効果を損なったりする可能性もあります(149)。腸内細菌叢が免疫チェックポイント阻害剤に対する反応を調節する役割を考慮すると、この分野は大腸がん治療の進歩に有望なトランスレーショナル研究の機会を提供します(図3)。 |
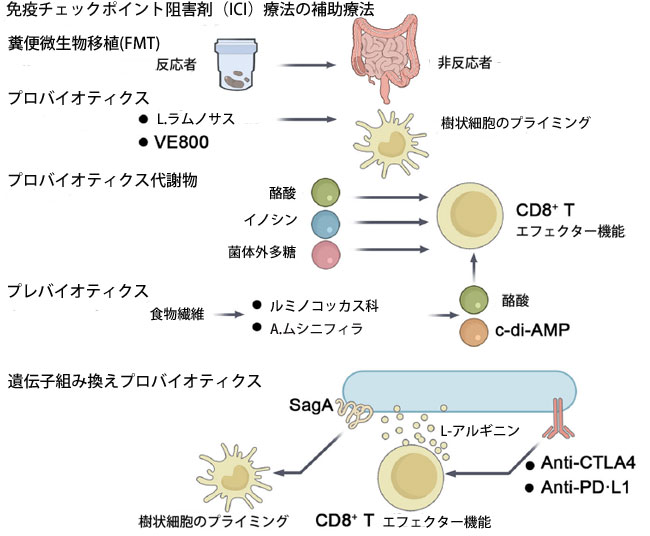 |
| 図3. 腸内細菌叢を利用して大腸がんにおける免疫チェックポイント阻害剤への反応性を高める現在の戦略。 これらの戦略には、糞便微生物移植や、プロバイオティクス、プレバイオティクス、プロバイオティクス代謝物、遺伝子組み換えプロバイオティクスといった新たなアプローチが含まれており、いずれも患者の予後改善に大きな可能性を秘めている。 |
| 興味深いことに、大腸がんを促進する病原性共生菌は、免疫チェックポイント阻害剤に対して相反する影響を与える可能性がある。例えば、フソバクテリウム・ヌクレアタムは腫瘍の増殖と化学療法耐性を促進することが知られているが、マウスモデルでは抗PD-L1抗体の有効性を高め、生存期間を延長することもできる(150)。フソバクテリウム・ヌクレアタムはSTING–NF-κBシグナル伝達を活性化し、PD-L1の発現を増強するが、PD-L1が阻害されると逆説的にCD8+ T細胞の活性化を増加させる(150)。同様に、多発性腸腫瘍(Min)マウスの腸管毒素原性バクテロイデス・フラジリスは鋸歯状腫瘍を誘発し、抗PD-L1抗体に対する感受性を高める(151)。このように、病原性細菌は免疫チェックポイント阻害剤療法に対して相反する影響を与える可能性がある。 |
| 5.3.プレバイオティクス |
| 食物繊維の摂取量が多いほど、世界各地の様々なコホートにおけるがん患者の免疫チェックポイント阻害剤(ICI)への反応性が向上し、免疫関連有害事象が減少することが示されています(152)。さらに、プレバイオティクスやイヌリン(153)、ペクチン(154)、ポリフェノール(155)、多糖類(156)などの水溶性食物繊維は、いくつかのマウスモデルにおいて抗PD-1抗体の有効性を高めることが分かっています。これらの物質は、ルミノコッカス科などの特定の細菌属、アッケルマンシア・ムシニフィラなどの個々の細菌、および短鎖脂肪酸や環状ジアデノシン一リン酸(環状ジAMP)などの代謝産物の増殖を促進することで、その作用機序が説明されます(157)。 短鎖脂肪酸は細胞傷害性CD8+ T細胞の機能を高め(153 )、一方、環状ジアデノシン一リン酸はSTING依存性I型インターフェロン産生を誘発し、自然免疫応答(単球、ナチュラルキラー細胞、樹状細胞を含む)の活性化と免疫チェックポイント阻害剤の有効性の向上につながる(158)。しかし、食物繊維欠乏下では、ムチン分解細菌(アッカーマンシア・ムシニフィラ)が宿主由来のムチンを分解し、粘液バリアを損ない、大腸炎感受性を高める可能性がある。したがって、適切な食物繊維摂取量を維持することは、有益な微生物活動を活用しつつ、過剰なムチン分解に伴う潜在的な有害作用を回避するために重要である(159,160)。大腸がんのトランスジェニックマウスモデルでは、イヌリンゲルとα-PD-1療法の組み合わせにより、CDX2-Cre NLS-APCfl/flマウスにおけるデキストラン硫酸ナトリウム(DSS)促進大腸腫瘍の増殖が抑制された(153)。プレバイオティクスは宿主の腸内細菌叢に既に存在する有益な分類群の存在に依存するため、プレバイオティクスとプロバイオティクスの両方を併用投与するシンバイオティクスは、どちらか一方だけを使用するよりも効果が高い可能性がある(161)。 |
| 5.4.プロバイオティクスとその生産物 |
| アッカーマンシア・ムシニフィラ(143)、バチルス・フラジリス(145)、ビフィドバクテリウム(146)、L.ラムノサスGG(162)、ラクティカゼイバチルス・パラカゼイ(163)、および様々なプロバイオティクス混合物(164)などの特定の腸内細菌は、マウスモデルにおいて免疫チェックポイント阻害剤の有効性を高めることが示されています。最近の研究では、C.ブチリカムを含むCBM588が転移性腎細胞がんの治療に及ぼす影響が検討されています。ある第I相試験では、ニボルマブとイピリムマブにCBM588を追加することで奏効率が改善した(58% vs. 20%、P = 0.06)ものの、統計的に有意な差は認められませんでした(165)。別の試験では、CBM588をカボザンチニブとニボルマブに併用することで奏効率が有意に増加した(74% vs. 20%、P = 0.01)ことが示されました(166)。 |
| プロバイオティクスの最適な投与量は治療効果にとって非常に重要であり、有益な細菌種が過剰に存在すると腸内細菌叢のバランスと多様性が崩れ、結果が悪化する可能性がある。免疫チェックポイント阻害療法を受けているNSCLC患者を対象とした研究では、アッカーマンシア・ムシニフィラの存在は治療効果の向上と相関していたが、アッカーマンシア・ムシニフィラの相対存在量が5%を超える患者は、アッカーマンシア・ムシニフィラが存在しない患者よりも結果が悪かったことがわかった(167)。また、特定の状況に応じた介入が効果をもたらさなかった、あるいは疾患を悪化させたという報告もある。免疫チェックポイント阻害を受けている158人のメラノーマ患者のコホートでは、市販のプロバイオティクスを自己申告で使用した場合、治療効果の低下と無増悪生存期間の短縮傾向が見られたが、統計的に有意な差は認められなかった。マウスを用いた前臨床検証では、プロバイオティクス補給が腫瘍内インターフェロンγ⁺細胞傷害性T細胞の蓄積を減少させることで抗PD-1療法の効果を損なうことが示され、これらの知見が裏付けられた(168)。また、大腸炎関連大腸がんのマウスモデル(AOM/Il10⁻/⁻)では、VSL#3プロバイオティクスカクテルによる介入治療により、腫瘍発生率、多発性、および組織学的異形成が有意に増加し、粘膜関連微生物叢における保護的なクロストリジウム属の消失が認められました(169)。これらの知見は、特に炎症やディスバイオシスが存在する場合、腫瘍治療の場面において、プロバイオティクス療法の選択を慎重かつエビデンスに基づいて行う必要性を強調しています。現在の研究では、11株からなるプロバイオティクスカクテルであるVE800などのバランスの取れた微生物コンソーシアムを、MSS (マイクロサテライト安定型)大腸がんの第I/II相試験においてニボルマブと併用する治療法を検討しています164。さらに、30種類の細菌からなるコンソーシアム(MET4)は、免疫チェックポイント阻害未治療患者の腸内細菌叢と血清代謝産物を改変する能力があり、安全であることが判明し、微生物コンソーシアムの潜在的な利点が裏付けられました170。しかし、ある研究では、4種類のクロストリジウム目菌株(CC4)の混合物がマウスの大腸がんを予防および治療できることが示され、その効果はCD8+ T細胞の活性化に依存していました。興味深いことに、ローズブリア・インテスティナリスまたはアナエロスティペス・カッカエの単独投与は、クロストリジウム目菌株混合物よりもさらに効果的でした(171)。これらの知見は、コンソーシアムは有益である可能性がある一方で、特定の個々の菌株はより優れた治療効果をもたらす可能性があることを示唆しています。 |
| 活性成分の理解に基づき、プロバイオティクス由来の治療薬のいくつかが現在、免疫チェックポイント阻害剤の補助剤として評価されている。これらには、細菌溶解物(172)、細胞外小胞(173)、および菌体外多糖(174)、ムロペプチド(175)、代謝物(124,176,177)などのより明確な成分が含まれる。これらの成分は、生きたプロバイオティクスの効果を完全に、または部分的に模倣し、免疫チェックポイント阻害剤の有効性を高める可能性を秘めている。 |
| 5.5.遺伝子操作されたプロバイオティクス |
| 機能性を向上させた遺伝子操作プロバイオティクスは、補助療法を安全かつ効率的に提供する方法として利用できる可能性がある。研究者らは、野生型、触媒活性を欠損した(C443A)、または分泌欠損型(ΔSS)のSagAを発現するラクトバチルス・ラクチス株を遺伝子操作し、野生型およびC443A変異株は分泌画分においてより高いシグナルを示した。野生型SagAを発現するラクトバチルス・ラクチスを投与した動物は、E.フェシウムを投与した動物と同等の腫瘍増殖抑制効果を示し、MC38大腸がん同種移植マウスにおいて、天然のSagA発現腸球菌株と同程度に抗PD-L1抗体の活性を効果的に増強した(175)。遺伝子操作された細菌は、腫瘍内T細胞の代謝を促進する担体として利用できる可能性がある。免疫能を有する大腸がんマウスモデル(MC38)において、研究者らは腫瘍由来のアンモニアをL-アルギニンに変換するプロバイオティクス株である大腸菌Nissle 1917(EcN)を開発した(178,179)。このL-アルギニンは、効果的な抗腫瘍応答に不可欠なT細胞の代謝能力と生存率を高める上で重要な役割を果たす(180)(図4)。 |
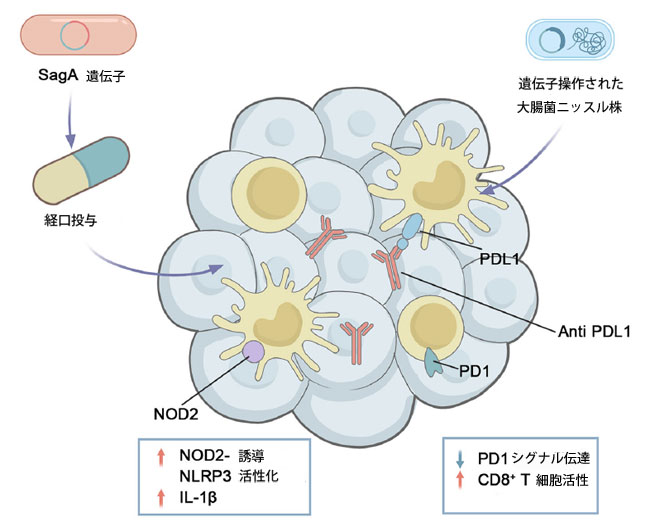 |
図4.腫瘍標的免疫療法のための遺伝子組み換えプロバイオティクス。 SagAを発現する経口投与されたラクトバチルス・プランタルムは、マクロファージNOD2と結合するムロペプチドを生成し、NLRP3インフラマソームを活性化してIL-1βを放出する。同時に、腫瘍に定着する大腸菌Nissleは、その場で抗PD-L1ナノボディを分泌し、PD-1/PD-L1相互作用を阻害してCD8⁺ T細胞活性を回復させる。 略語:NOD2(ヌクレオチド結合オリゴマー化ドメイン含有タンパク質2)、SagA(分泌抗原A)。 |
| 免疫学的に「冷たい」がんの治療におけるプロバイオティクスシステムの汎用性を評価するために、研究者らは標的療法送達用に設計された遺伝子操作プロバイオティクスを開発しました。このアプローチでは、制御された溶解放出メカニズムを利用して、腫瘍内でPD-L1とCTLA-4を直接標的とするナノボディを産生および放出するようにプロバイオティクス細菌を遺伝子操作します。MSS(マイクロサテライト安定型)大腸がんのマウスモデルでは、このシステムをプロバイオティクス産生サイトカインである顆粒球マクロファージコロニー刺激因子と組み合わせることで、抗腫瘍効果が向上し、生存率が向上しました(181)。これらの研究は、遺伝子操作プロバイオティクスが免疫チェックポイント阻害剤の効果を高める適応可能なツールとしての可能性を示しています。 |
| 5.6.糞便微生物叢移植(FMT) |
| 糞便微生物叢移植は、マイクロバイオームを調節する臨床的アプローチであり、再発性クロストリジウム・ディフィシル感染症の治療薬としてFDAの承認を受けています(182)。糞便微生物叢移植は、無菌動物に糞便微生物叢移植を投与することでヒトドナーで観察される免疫チェックポイント阻害剤の効果を再現できるというエビデンスに基づき、臨床試験において免疫チェックポイント阻害剤との併用療法としても検討されています(183,184)。しかしながら、ある研究では、炎症性腸疾患(IBD)患者由来の糞便微生物叢移植を受けたマウスは、健常ドナー由来の糞便微生物叢移植を受けたマウスと比較して、結腸のTH1細胞が有意に減少し、治療抵抗性を示したことが明らかになりました(185)。これは、免疫チェックポイント阻害剤の効果には健全なマイクロバイオームが不可欠であることを示唆しています。 |
| 初期の臨床研究では、抗PD-1抗体に反応するドナーからの糞便微生物叢移植によって、免疫チェックポイント阻害剤抵抗性の転移性黒色腫患者の一部で抗PD-1抗体に対する抵抗性を克服するなど、有望な結果が示されています(186,187)。さらに、多施設共同第I相試験では、未治療の進行期黒色腫患者において、がんのないドナーからの糞便微生物叢移植とニボルマブまたはペムブロリズマブの併用が評価されました(188)。 |
| Huangによる研究では、糞便微生物叢移植とPD-1阻害剤の併用により、大腸がん腫瘍を有するマウスにおいて、いずれかの治療単独と比較して、生存転帰と腫瘍制御が改善された。この研究では、糞便微生物叢移植によって増加したバクテロイデス・テタイオタオミクロンとバクテロイデス・フラジリス、および糞便微生物叢移植によって減少したバクテロイデス・オバタスが、大腸がんにおける免疫チェックポイント阻害剤の有効性の向上に寄与していることが強調された(184)。第II相試験では、MSS m大腸がん患者が糞便微生物叢移植とチスレリズマブおよびフルキンチニブを三次治療以降として投与され、mPFSが9.6ヵ月、全生存期間中央値(mOS)が13.7ヵ月、全奏効率が20%、疾患制御率が95%となり、治療関連死はなかった(112)。別の臨床試験では、有益な微生物叢を用いた糞便微生物叢移植が、進行性固形がん、特に消化器がんにおける抗PD-1阻害剤への耐性を克服するのに役立つ可能性が示唆されている(113)。大腸がん患者を対象とした同様のアプローチを用いた追加試験が進行中である(NCT04729322およびNCT04130763)。 |
| しかし、糞便微生物叢移植には、安全性に関する懸念や、ドナーとレシピエントの両方で有効性に必要な微生物叢プロファイルの一般化と標準化に関する課題など、注目すべき制限があり、広く使用するのに適していません。糞便微生物叢移植はドナーから生きた腸内微生物叢全体を移植することを伴うため、既知および未知の病原体を伝染させる固有のリスクがあります。報告されている合併症には、ノロウイルス腸炎、サイトメガロウイルス再活性化、真菌および寄生虫感染症、さらには肥満や代謝機能障害などの疾患関連形質の水平伝達の可能性が含まれます(189,190)。2019年には、同じドナーから糞便微生物叢移植を受けた2人の患者が広域スペクトルβ-ラクタマーゼ産生大腸菌による菌血症を発症し、1人が死亡したことが報告されました(191)。この事件を受けて、米国食品医薬品局は糞便微生物叢移植に関連する感染リスクについて安全警告を発しました。さらに、最近の後向きコホート研究では、検査されたドナーの糞便の9%に多剤耐性菌が含まれていることが判明し、別の重大な安全性の懸念が浮き彫りになりました(192)。 |
| 5.7.放射線療法の治療的意義 |
| 放射線療法(RT)は広く用いられている抗腫瘍治療法であり、固形腫瘍を有する新規がん患者の50%以上が治療過程のいずれかの段階で放射線療法を受けている(193)。しかしながら、腸は上皮細胞のターンオーバーが速いため、放射線に対して非常に感受性が高い(194)。小腸部分照射(195)や移植片対宿主病(196,197)に焦点を当てたマウスモデルを用いた研究では、放射線療法後に腸内細菌叢に顕著な変化が生じることが示されている。腸内細菌叢と放射線療法の間には双方向的な相互作用が存在する。一方では、電離放射線は腸内細菌叢の構成と機能を変化させ、微生物の多様性と豊富さを低下させ、プロテオバクテリアやフソバクテリアなどの病原性細菌の増加、そしてフェカリバクテリウムやビフィドバクテリウムなどの有益な細菌の減少を引き起こす(198)。 バクテロイデス・インファンティスとその特異抗体を予防的に投与すると、マウス肺がんモデルにおいて放射線感受性が高まり、腫瘍の増殖が抑制されることが示されている(199)。一方、16S rRNA qPCRによる絶対定量では、(化学)放射線療法後に細菌総量が約90%減少することが示されており、病原性共生菌の相対的な増加は、真の過剰増殖ではなく、優勢な共生菌の喪失を反映していることが多いことを示している(200)。その一方で、微生物叢は、治療結果を向上させ、放射線毒性を軽減することによって、放射線療法の臨床効果に影響を与える。 |
| 5.8.放射線療法の有効性向上 |
| 研究により、経口バンコマイシンは、メラノーマおよび肺がん・子宮頸がんの前臨床モデルにおいて、低分割放射線療法の直接的および遠隔的な抗腫瘍効果の両方を増強することが示されています(201)。他の研究では、常在細菌が効果的な抗腫瘍免疫応答に不可欠である一方、常在真菌は放射線療法後の免疫抑制的な微小環境を制御することが明らかになっています。これらの真菌を標的とすることで、放射線療法の成果が向上することが示されています(202)。糞便微生物移植は、消化管内のローズブリア・インテスティナリスのレベルを上昇させることが分かっており、この腸内常在細菌は、酪酸/OR51E1/RALB経路を介して放射線誘発オートファジーを促進し、大腸がん細胞死を増強します。このメカニズムは、前臨床段階において、大腸がんに対する有望な放射線増感剤となる可能性を示しています(203)。さらに、大腸がん患者に多く見られる細菌株腸管毒素原性バクテロイデス・フラジリスは、バクテロイデス・フラジリス毒素とIL-17を産生し、これらが相乗的に免疫細胞のSTAT3シグナル伝達経路を活性化し、がんの増殖を促進する可能性がある(204)。研究によると、腸管毒素原性バクテロイデス・フラジリスはバクテロイデス・フラジリス毒素を産生することで大腸がんの放射線抵抗性を高める可能性もあり、放射線抵抗性の既知のメディエーターであるJAK2/STAT3/CCND2軸を活性化する可能性がある(205)。 |
| 5.9.放射線毒性の軽減 |
| 放射線療法の有害な副作用を軽減するためのいくつかの戦略が特定されています。無作為化臨床試験では、プロバイオティクスであるストレプトコッカス・サリバリウス K12(SsK12)が、放射線療法患者における重度の口腔粘膜炎の発生率、発症時期、および持続期間を有意に減少させ、良好な安全性プロファイルを示すことが実証されました(206)。さらに、実験的研究では、糞便微生物移植が急性放射線症候群(ARS)を軽減し、放射線照射を受けたマウスの末梢白血球数を改善し、消化管機能と腸管上皮の完全性を維持することが示されています(207)。さらに、糞便微生物移植は放射線照射を受けたマウスにおいてインドール-3-プロピオン酸(IPA)のレベルを上昇させることが明らかになりました。インドール-3-プロピオン酸は、腫瘍の増殖を促進することなく、腹部全体照射後の消化管毒性を軽減する化合物です(208)。 |
| 5.10.外科的切除における治療的意義 |
| げっ歯類を用いた研究から得られた説得力のある実験データは、腸内細菌叢が腸粘膜の血管新生と創傷治癒において重要な役割を果たしていることを示している(209)。腸内細菌叢の特定の構成要素、特に酪酸産生菌は、上皮修復に不可欠である(210)。さらに、研究により、バクテロイデス・テタイオタオミクロンがパネート細胞の活性化を介して小腸の毛細血管網を効果的に倍増させることで血管新生を促進することが示されている(211)。 |
| 微生物群集内における細菌間の競争と協力のダイナミクスは、創傷治癒を促進することも阻害することもある。例えば、ラクトバチルス・ファーメンタムRC-14は、外科的インプラントのラットモデルにおいて、黄色ブドウ球菌による感染症を阻害することがわかっている(212)。逆に、緑膿菌のようなシデロフォア産生細菌間の協力は、鉄捕捉化合物を他の細菌と共有することを可能にすることで、病原性を高める可能性がある(213)。 |
| 1997年の画期的な研究で、Schardeyらは緑膿菌と吻合部漏出との潜在的な関連性を示唆し、ヒトの吻合合併症における微生物の関与を確認した最初の無作為化二重盲検試験につながった(214)。その後の研究では、新しい病原性抑制化合物であるPEG/Pi(高分子量PEG)が緑膿菌の組織破壊表現型の獲得を阻止し、ラットモデルにおける吻合部漏出を軽減することがわかった(215)。Shoganらの研究では、16S rRNA遺伝子配列決定を用いてげっ歯類モデルの吻合部位における微生物叢の変化を調べた。注目すべきは、彼らの研究では抗生物質や腸管前処置の使用を避け、これらの部位の組織関連微生物叢に大きな変化が見られる一方で、腸管内微生物叢(糞便)は比較的安定していたことである(216)。 |
| 腸内細菌叢の比較分析により、手術後の大腸がん患者(A1)は、手術前の患者(A0)および健康な人(H)と比較して、微生物の多様性に有意な差があることが明らかになった。具体的には、手術後の大腸がん患者ではシャノン指数とシンプソン指数の両方の多様性指数が著しく低く(P < 0.05)、腸内細菌叢が手術後の転帰に果たす役割が強調された(217)。さらに、最近の研究では、フソバクテリウム、グラヌリカテラ、ゲメラなどの病原性共生菌属を含む特定の微生物群の増加が、原発切除後の転帰の改善と相関することが特定され、大腸がんの予後における腸内細菌叢の役割に関する従来の見解に疑問を投げかけている(218)。 |
| 臨床研究において、Komen らは、RT-PCR を用いて排液中の大腸菌および エンテロコッカス・フェカリス を検出することに基づく、大腸吻合部漏出の早期発見のための迅速スクリーニング法を開発した。彼らの結果は、エンテロコッカス・フェカリスのレベルが高いほど早期発見の信頼できる指標となり得る一方、陰性結果は吻合部漏出がないことを強く示唆していることを示している(219)。大腸がん患者の周術期ケアにおけるプロバイオティクスの使用に関するレビューでは、プロバイオティクスは細菌の移行を減らし、腸粘膜の完全性を高め、有益な微生物と有害な微生物の間の好ましいバランスを促進することができることが示されている(220)。さらに、プロバイオティクスとシンバイオティクスの両方が、大腸がん手術における術後合併症を予防するための効果的な戦略として注目されている(221)。 |
| 6.結論と今後の展望 |
| 比較的静的なヒトゲノムとは異なり、マイクロバイオームは環境、食事、ライフスタイル要因に応じて絶えず進化する、驚くべき可塑性を示します(222)。宿主ゲノムは主に親のDNAから受け継がれますが、マイクロバイオームは個人差が大きく、個人間および時間経過とともに大きく変動するという特徴があります(223,224)。この複雑さの要因を理解することで、予防、診断、治療戦略を改善し、より正確で個別化されたヘルスケアソリューションへの道を開くという、他に類を見ない機会が得られます(225)。 |
| 大腸がんでは、腫瘍関連微生物群集の特徴付けにメタゲノムシーケンスがますます利用されるようになっている(45,226)。しかし、研究間の顕著な不一致が臨床応用を制限しており、多くの場合、技術的な違い(サンプル処理やシーケンス方法など)や、地理、食事、性別、サンプリング時間などの交絡因子から生じている(227,228)。これらの問題に対処するため、マイクロバイオーム研究の一貫性と透明性を促進するために設計された17項目のチェックリストを提供する「マイクロバイオーム研究の組織と報告の強化」ガイドラインが導入された(229)。さらに、妥当な仮説検定と堅牢で一般化可能な結論を保証するために、マイクロバイオームデータの構成性、疎性、高次元性を考慮した厳密な事前検出力とサンプルサイズ計算が不可欠である(230)。これらの取り組みを補完するものとして、患者由来組織および実験モデルにおいて、メタゲノミクスとメタボロミクス、トランスクリプトミクス、エピゲノミクス、プロテオミクスをバルクおよび単一細胞解像度で組み合わせた統合的なマルチオミクスフレームワークが、宿主と微生物のクロストークの複雑さを解明するために展開されている(231–233)。標的核酸ハイブリダイゼーションプローブを使用して腫瘍微小環境内の微生物分類群の分布を解明する空間メタオミクスプロファイリングの最近の進展により、腫瘍内マイクロバイオームの構造と隣接する細胞表現型に対するその調節効果が明らかになり始めている(234,235)。しかし、これらのアプローチでは、微生物の空間マッピングと同時in situ機能アッセイ(例えば、微生物毒素またはサイトカインの発現)を統合することはまだできない。微生物バイオマスの低さとRNAの急速な分解によって課される制約に対処することが、真のインタラクトーム再構築と高解像度空間コミュニティプロファイリングにとって極めて重要となるだろう(222)。 |
| さらに、バイオマス量の少ない臨床検体の限界に対処するため、最適化された分類学的プロファイリング(Kraken 2/Bracken)と機能アノテーション(HUMAnN 3)を統合した、カスタマイズされたメタトランスクリプトミクスワークフローが開発され、宿主RNAバックグラウンドが高い胃組織でも微生物種とその発現経路を正確に検出できるようになりました(236)。これに加えて、ロングリードシーケンスプラットフォームの登場により、メタゲノムアセンブリゲノムの完全性、株レベルの識別、およびバリアントコールが大幅に向上し、ショートリードアプローチに固有のアセンブリとプロファイリングのバイアスを克服しました(237)。 |
| メタゲノムおよびメタトランスクリプトームデータセットの深度と規模の増大は、意図せずアーティファクトを増幅する可能性があり、乳がん腫瘍における極限環境微生物の分類群に関するParidaらの報告がその例である。そのため、汚染制御、バッチ効果補正、検証パイプラインの厳密な改訂が求められている(238,239)。これに対応して、機械学習および人工知能パイプラインは、より厳密な交差検証、より大きなホールドアウトコホート、および複雑なマイクロバイオームデータから真のシグナルを抽出するためのカスタマイズされた特徴エンジニアリングによって改良されてきた(240)。ランダムフォレストとSHAPを組み合わせた説明可能なAIを統合すると、大腸がん分類において約0.73の精度と約0.67の精度-再現率AUCが得られ、フソバクテリウム、ペプトストレプトコッカス、およびパルビモナスが最も予測力の高い分類群であることが示された(241)。 |
| しかし、多くのAIモデルは、報告されている優位性にもかかわらず、がん研究において中程度または不安定な予測力しか示さないことが多く、これは主に小規模コホートへの過学習、質の低いまたは限られたマイクロバイオームデータセット、不十分な検証によるものです(242,243)。マイクロバイオームベースの大腸がんアプリケーションにおける一般化可能性と精度を高めるために、マルチモーダルデータ統合(臨床、微生物、縦断的)(244)、免疫療法反応予測のためのマイクロバイオームシグネチャの活用、高解像度シングルセルおよび空間マルチオミクスの組み込みなどの戦略が提案されており(245,246)、精密腫瘍学のための複雑な腸内微生物生態系の解読におけるAIの重要な役割が強調されています。 |
| これらの進歩に基づいて、大腸がん病変に選択的に定着し、微生物生態系を再構築するために、バイオエンジニアリングされたプロバイオティクスとプレバイオティクスナノ粒子複合体が開発されました(133)。治療用タンパク質を発現する腫瘍標的型大腸菌Nissleとペディオコッカス・ペントサセウスは大腸がん細胞の増殖を阻害し、腺腫を退縮させます(250,251)。一方、プレバイオティクスでカプセル化された胞子とキシラン-ステアリン酸ナノ粒子は短鎖脂肪酸の産生を促進し、CD8⁺ T細胞の活性を高め、抗腫瘍効果をin vivoで5%から70%以上に高めます(133,252)。これらの有望な戦略にもかかわらず、大腸がん管理における精密な微生物叢編集を実現するには、腸管浸潤、プロバイオティクスの生着、腫瘍内標的化、免疫調節といった重要な課題に取り組む必要があります。 |
| 将来的には、厳密な研究デザイン、標準化されたマルチオミクスフレームワーク、そして空間オミクス、人工知能、マイクロバイオームを標的としたナノテクノロジーの革新的な統合が、大腸がんの根底にある微生物学的メカニズムを解明し、マイクロバイオームに関する知見を精密腫瘍学へと迅速に応用するために不可欠となるだろう。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、NPJ Biofilms Microbiomes. 2025 Sep 30;11:190.に掲載されたHarnessing gut microbiota for colorectal cancer therapy: from clinical insights to therapeutic innovations.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


