ケフィアライフをお勧めする中垣技術士事務所

| 文献調査(発酵乳、腸内細菌の科学:研究の最前線) |
腸内細菌叢:あらゆる病気の起源か、それとも万能薬か?免疫 ・代謝疾患、栄養、そして腸内細菌叢に基づく介入 |
Carmela Colica, Immacolata Vecchio |
|
|
| 要約 |
肥満、2型糖尿病、アレルギー、自己免疫疾患などの慢性非感染性疾患(CNCD)は、遺伝的要因と環境要因(食事など)および腸内細菌叢の相互作用によって悪化し、世界的に大きな健康負担となっています。 |
| 腸内細菌叢は、出生から成人期まで宿主の免疫系および代謝系に影響を与える、複雑かつ動的な微生物群集です。腸内細菌叢の組成の不均衡であるディスバイオシスは、軽度の炎症、インスリン抵抗性、代謝・免疫疾患の発症に関与していることが示唆されています。 |
| 本論文では、慢性非感染性疾患における腸内細菌叢の重要な役割を概説し、特に制御性T細胞の誘導やTh1/Th2バランスを含む免疫系との相互作用に重点を置いています。さらに、出産様式、食事、および異物による腸内細菌叢の構成と機能への影響についても考察しています。最後に、本研究は、プレバイオティクス、プロバイオティクス、シンバイオティクス、糞便細菌叢移植といった腸内細菌叢を標的とした介入が、腸内生態系を調節し、疾患リスクを軽減する可能性を強調しています。 |
| 文献の改訂により、微生物叢を健康と病気の重要な役割とみなし、病気の予防と管理における統合的なアプローチの必要性が浮かび上がってきました。 |
| ハイライト |
| •慢性非感染性疾患は、遺伝的要因と、食事や腸内細菌叢などの環境要因の相互作用によって発生します。 |
| •出産様式、食事、異物への曝露などの要因は、腸内細菌叢の構成と機能に重大な影響を及ぼします。 |
| •腸内細菌叢の乱れは、軽度の炎症、インスリン抵抗性、そして様々な代謝・免疫疾患と関連しています。 |
| •腸内細菌叢と健康を回復させるための潜在的な介入としては、バイオモジュレーターや糞便細菌叢移植などが挙げられます。 |
| •今後の研究では、効果的な介入策を開発するために、食事、腸内細菌叢、そして宿主の健康状態との相互作用に焦点を当てるべきです。 |
| 目次(クリックして記事にアクセスできます) |
| 1. はじめに |
| 2. 腸内細菌叢と免疫 |
| 2.1. 腸内細菌叢、腸管上皮細胞、および腸管関連リンパ組織シグナル伝達 |
| 2.2. リンパ球集団間の洗練されたバランス |
| 2.3. 腸内細菌叢と出産方法 |
| 3. 腸内細菌叢とアレルギー |
| 3.1. エクスポソームの役割 |
| 3.2. 微生物叢と喘息の免疫学的要素 |
| 3.3. 微生物叢とアトピー性皮膚炎 |
| 3.4. 腸内細菌叢の乱れとアレルギー |
| 4. 腸内細菌叢と肥満 |
| 4.1. 肥満の腸内細菌叢異常のメカニズム |
| 4.2. 肥満と糖尿病の関連性 |
| 5. 腸内細菌叢と糖尿病 |
| 5.1. 腸内細菌による代謝調節 |
| 5.2. 腸内細菌叢の乱れと糖尿病 |
| 6. 腸内細菌叢とバイオモジュレーター |
| 6.1. 腸内細菌叢とプレバイオティクス |
| 6.2. 腸内細菌叢とプロバイオティクス |
| 6.3. 腸内細菌叢とシンバイオティクス |
| 6.4. 腸内細菌叢とパラプロバイオティクス |
| 6.5. 腸内細菌叢とメタバイオティクス |
| 6.6. 腸内細菌叢とポストバイオティクス |
| 6.7. 糞便微生物移植 |
| 7. 腸内細菌叢と栄養 |
| 7.1. 微生物叢とファイトケミカル |
| 7.2. 微生物叢の代謝物 |
| 8. 腸内細菌叢と外因性物質 |
| 8.1. 抗生物質による腸内細菌叢の乱れ |
| 8.2. 農薬による腸内細菌叢の乱れ |
| 8.3. 重金属による腸内細菌叢の乱れ |
| 8.4. マイクロプラスチックおよびナノプラスチックによる腸内細菌叢の乱れ |
| 9. 結論 |
本文 |
| 1.はじめに |
| 慢性非感染性疾患には、心血管疾患、慢性呼吸器疾患、神経変性疾患、リウマチ性疾患に加え、がん、肥満、2型糖尿病、様々な腎臓疾患や精神疾患など、幅広い疾患が含まれます。 |
| これらの疾患は、2011年の第66回国連総会で正式に承認されました。世界保健機関(WHO)の推定によると、慢性非感染性疾患による死亡者数は年間4,100万人に達し、世界の死亡率の約74%を占めています。ヨーロッパは慢性非感染性疾患の世界的な負担が最も大きい地域です(図1)。 |
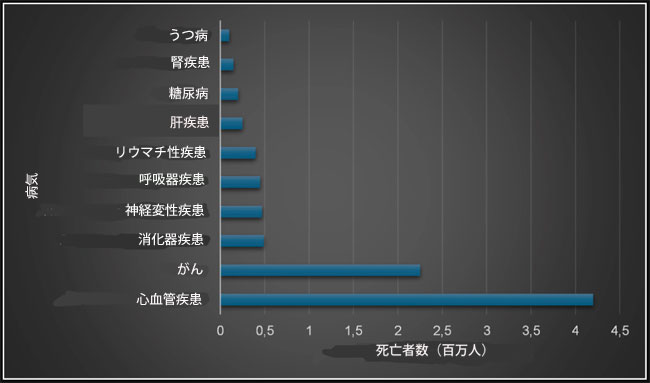 |
| 図1. ヨーロッパにおける10大死亡原因。世界疾病負担共同ネットワーク、「世界疾病負担研究2019(GBD 2019)」結果(2020年、保健指標評価研究所(IHME))のデータより. |
| 慢性非感染性疾患の有病率の急激な上昇は、21世紀における最も差し迫った保健・社会経済上の課題の一つとなっています[1,2]。このため、WHOは2025年までに慢性非感染性疾患による早期死亡率を25%削減するための戦略を策定しました。これらの対策は、慢性非感染性疾患の主要なリスク要因(または決定要因)に対処しながら、医薬品、医療技術、カウンセリングへのアクセスを確保することに重点を置いています。 |
| 慢性非感染性疾患の特徴的な点は、免疫系の活性化によって引き起こされる低度の炎症の持続的な状態である[3]。 |
| 慢性非感染性疾患の領域では、肥満、2型糖尿病、アレルギーといった疾患が、特に欧米諸国において、世界的に重大な健康問題となっています。遺伝的素因がこれらの疾患の発症に影響を及ぼす一方で、蓄積されたエビデンスから、食事などの環境要因が腸内細菌叢に及ぼす影響が、全身性炎症の形成や代謝異常の誘発において重要であることが明らかになっています。食事、免疫系、腸内細菌叢の相互関連性は、全身性炎症に大きな影響を与え、インスリン抵抗性、肥満、心血管リスク、免疫機能障害といった問題の発現に寄与しています[4,5]。マイクロバイオータとマイクロバイオームを区別することが重要です。前者はヒトなどの生物に関連する微生物群を指し、後者はそれらの微生物、その遺伝物質[6,7]、そしてそれらに関連する生物学的環境(構造要素(タンパク質、ペプチド、脂質、多糖類)、核酸(構造DNA/RNA)、可動性遺伝成分(ウイルスやファージ)、微生物代謝物(シグナル分子、毒素、有機化合物および無機化合物)[8]を含む)を包含する。哺乳類の微生物叢は、細菌、真菌、ウイルスなど、体内および体表に生息する多様な微生物から構成されている(表1)。 |
| 表1. 主な哺乳類の微生物叢の分類 |
 |
 |
| (訳者注:正確を期するために菌名をカタカナ表記していません) |
| この微生物群は、消化、免疫、代謝といった生理学的プロセスに大きな影響を与えます。これらの微生物のほとんどは腸内に生息し、中でも細菌種は最も広く研究されています[9]。歴史的には消化器官としてのみ考えられてきましたが、現在では、ヒトの消化管は局所的および全身的な影響を及ぼす高度な調節能力を有する多機能システムとして認識されています。実際、消化管は代謝、免疫、炎症プロセス、行動、そして気分に大きな影響を与えています[10]。 |
| 慢性非感染性疾患の多因子的原因は、出生後の腸内細菌叢の定着パターンの乱れと微生物多様性の低下と関連しており、これらはいずれも多くの慢性非感染性疾患に特徴的な免疫代謝の不均衡と慢性の低度炎症の一因となっている可能性がある[[11], [12], [13]]。明確な「健康な」微生物叢の構成は未だ解明されていないものの[14]、観察研究では一貫して、微生物の多様性と存在量の不均衡であるディスバイオシス(腸内細菌叢の乱れ)が様々な慢性非感染性疾患と関連付けられている[15]。 |
| さらに、新たなエビデンスは、ディスバイオティックな微生物叢が疾患の進行に寄与する可能性があることを示唆しています[16]。微生物叢移植研究では、罹患個体から健康な動物へのディスバイオティックな微生物叢の移植が疾患の発症を誘発すること、また微生物叢の構成が他者との密接な接触によって影響を受けることが示唆されています。2020年、フィンレイは、特定の慢性非感染性疾患には微生物由来の成分が含まれている可能性があり、微生物叢を介して感染する可能性があると提唱しました[9]。 |
| 腸内細菌叢は、非常に動的でありながらも強固に自己調節する微生物生態系であり、生涯を通じて免疫系および代謝系の発達と機能に極めて重要な役割を果たしています。宿主との相互作用は、代謝経路、免疫関連経路、そして構造経路を介して起こります。最終的に、微生物ファミリーのディスバイオシスは、多くの慢性非感染性疾患の特徴的な兆候であることが判明しました。 |
| 個体間で分類学的構成に大きなばらつきがあるにもかかわらず、機能的冗長性により、異なる微生物分類群が同一の代謝的役割を果たすことができ、それによって多様なマイクロバイオーム間で中核的な生理機能が維持されています[17]。実際、腸内細菌叢の構成は、個体間だけでなく、同一個体内でもライフステージの異なる段階で大きく異なります。健康な成人では、フィルミクテス門(例:エンテロコッカス、ラクトバチルス、クロストリジウム、バチルス、ルミノコッカス)とバクテロイデス門(例:バクテロイデス、プレボテラ)が優勢であり、アクチノバクテリア門(ビフィズス菌)、フソバクテリア門、プロテオバクテリア門(大腸菌)、ヴェルコミクロビア門などの優勢な菌は少ないです[18]。 |
| 腸内細菌叢の発達は子宮内で始まり、出生後に急速に定着する[19]。個人の初期の微生物構成は母親のそれ(出産方法の影響を含む)を反映しているが、成人期には社会的交流などの要因によって変化する。例えば、同居人や配偶者は、遺伝的には関連しているものの地理的に離れた兄弟姉妹間に見られるものよりも、微生物叢の類似性を示すことが多い。微生物叢は家族内および社会的ネットワーク内で伝染性があり、夫婦関係は腸内細菌の分析に基づいて判定することができる[20]。 |
| 人類は長い進化の歴史を通じて、「古くからの友人」である細菌と切っても切れない関係を築いてきました。実際、人類は長い時間をかけて微生物と共進化し、相互依存と相互利益を特徴とする関係を築いてきました。ヘンダーソンとウィルソンによって提唱された「ホモ・バクテリエンス」という用語は、この共生関係を的確に捉えています[21]。この長年にわたる関係は、微生物が人間の生理機能と健康の形成において果たす不可欠な役割を強調しています。 |
| アメリカの遺伝学者リン・マーギュリスによって提唱された「細胞内共生説」は、ミトコンドリアが祖先細菌から進化したことを示唆しています[22]。これらの細菌はヒト細胞に組み込まれると、その有益な酸化代謝のおかげで、潜在的な脅威から共生パートナーへと変化しました[23]。 |
| 人体は広く「超個体」あるいはホロバイオント(完全共生体)とみなされており、自身の真核細胞と、主に細菌を主体とする広範な微生物群(総称してマイクロバイオータ)から構成されています。出生時から、様々な細菌種が皮膚、口腔、呼吸器系、泌尿生殖器系、そして特に消化管といった体の特定の部位に定着します。腸内マイクロバイオータは徐々に発達し、生後2年以内に完全な構成に達します[24]。 |
| 腸内細菌叢は主に結腸に集中しており、膨大な細菌バイオマスを代表しており、その細胞数は人体の真核細胞の10倍にも上ります[25,26]。 |
| 微生物叢の構成は、時間の経過とともに比較的安定しているものの、生理学的または病理学的要因によって変化する可能性があります[27]。この複雑な生態系は、その集合的な遺伝物質(マイクロバイオーム)とともに、共生関係において宿主と密接に相互作用します。この細菌群集の構成は、宿主生物との動的な共生バランスを反映しています。 |
| 個体差は大きいものの、研究者たちは、必須の代謝機能と栄養機能を担う共通の「コア微生物叢」とそれに関連する「コアマイクロバイオーム」の存在を仮説として提唱している[28]。この「微生物制御室」は、生物全体の恒常性維持にとって重要な媒介因子として浮上している[29]。健全な微生物叢は、その生態学的安定性と回復力によって定義され、これは、ストレス下でも混乱に抵抗したり、構成を回復したりする能力を指す。また、健康と有益な機能プロファイルに関連する特定の細菌パターンの存在も特徴としており、これらは常在微生物によって促進される栄養、代謝、免疫、保護といった役割である[30]。 |
| 最近、ヒト微生物叢における普遍的な核という概念が再検討され、基本的な栄養機能と代謝機能に不可欠であり、「機能的安定性」と表現されています。この再考は、環境の影響、解剖学的領域、栄養、民族、地理的要因を考慮しています[31]。 |
| メタオミクス技術(訳者注:「メタオミクス(Meta-omics)」とは、土壌、海水、あるいはヒトの腸内環境といった特定の環境サンプル中に存在する「微生物群集(コミュニティ)」全体を対象に、遺伝情報、タンパク質、代謝産物などを網羅的に解析する手法です)の進歩は、腸内細菌叢とそのヒトの健康と疾患における役割についての理解を深めてきました。これらの科学的手法は、DNA(メタゲノミクス)、RNA(メタトランスクリプトミクス)、タンパク質(メタプロテオミクス)、代謝物(メタボロミクス)、脂質(メタリピドミクス)、そして炭水化物とタンパク質の相互作用(メタグライコミクス)といった様々な生物学的構成要素を分析します[32,33]。 |
| 共生微生物の70~80%は従来の方法では培養できないため、これらの培養非依存型技術はヒト微生物叢の研究に革命をもたらしました。また、慢性炎症性疾患や免疫介在性疾患の予防と発症における微生物叢の関与に関する理論を強化しました[34]。 |
| 現在までに、ヒトの消化管では、バクテロイデス門、フィルミクテス門(例:乳酸菌、クロストリジウム、腸球菌)、放線菌(例:ビフィズス菌)、プロテオバクテリア(例:腸内細菌科、大腸菌)など、様々な門に属する1000種以上の細菌種が確認されています。腸内微生物ゲノムは約300万個の遺伝子で構成されていると推定されており、これはヒトゲノムの約150倍に相当します。この推定値には、ウイルスの存在を示す用語である「ビローム」も含まれています。ビロームとは、細菌の数を1:1から10:1の比率で上回ることが多いウイルスの存在を指します[35]。 |
| 歴史的には消化のみに焦点を当てていると考えられてきた消化管ですが、現在でははるかに包括的な役割を果たしていると理解されています。腸内細菌叢の存在は、広範な全身的影響を及ぼす多くの調節プロセスを促進し、局所および全身の炎症[25]、代謝[36]、さらには行動[37]にも影響を与えています。したがって、腸内細菌叢とその代謝産物との相互作用は、宿主の健康維持に不可欠です[[38]、[39]、[40]]。 |
| 腸内細菌叢は、多様な保護、栄養代謝、解毒、構造、免疫調節の役割を果たすため、宿主生物にとって非常に重要です[41]。 |
| その防御機能は、病原細菌の定着と血流への侵入を防ぐのに役立ちます。この耐性を支えるメカニズムには、競合的阻害(例えば、栄養素の競合や受容体部位の阻害)、腸管上皮受容体または粘液層からの病原体の物理的排除、抗菌物質の産生(アメンサリズム)などがあります[42]。 |
| ヒトの体は数十種類の消化管酵素しか産生しませんが、微生物バイオマスは数百種類もの、相補的なものも独自のものも提供しています。これらの微生物酵素は、数多くの代謝プロセスの基礎となっています[43]。この連携を通して、腸内マイクロバイオームはヒトゲノムを補完する広範な酵素レパートリーを提供することで、ヒトの生化学的柔軟性を高めています。この進化的パートナーシップは、細菌を共生関係へと形作った選択圧の結果であると考えられています[44]。 |
| 微生物叢の栄養代謝的役割には、多糖類[46]の消化によって得られるポリフェノール[45]や、ビオチン、葉酸、ビタミンK、ビタミンB群などの必須ビタミンの合成、イオン吸収の促進(Mg++、Ca++、Fe++)などが含まれます。また、短鎖脂肪酸、アミノ酸、ポリアミン、成長因子など、腸管上皮細胞の成長に必要な化合物の産生にも重要な役割を果たし、オリゴ糖、多糖類、上皮粘液などの消化されない食物成分を発酵させます。さらに、微生物発酵による食物繊維からのエネルギー回収は、ヒトが単独では行えないプロセスを補います。特定の常在細菌群によるこのプロセスの調節は、微生物叢の構成と肥満の多因子的病因との複雑な関係を浮き彫りにします[4] |
| 微生物叢の質的構成の変化は、遺伝的要因、環境要因、そしてライフスタイル要因の相互作用によって影響を受ける重要な要因であることが現在では理解されています。微生物叢の解毒能力は、薬物(特に抗生物質)、環境毒素、農業残留物などの異物を処理・中和する酵素合成能力に起因すると考えられており、その重要な生理機能のさらなる証拠となっています[49]。 |
| 最近の研究では、微生物由来の代謝物(短鎖脂肪酸、二次胆汁酸、トリプトファン分解産物など)が、宿主の代謝、免疫調節、炎症、遺伝子発現に影響を及ぼす重要なシグナル伝達分子として機能していることが明らかにされています。この研究は、腸内細菌叢を単なる受動的な常在菌群としてではなく、全身の健康に積極的に貢献する存在として位置付けています。腸内細菌叢の乱れは、腸管バリアの完全性を損ない、エンドトキシン血症を引き起こし、代謝性疾患や炎症性疾患にしばしば関与する全身性免疫応答を誘発する可能性があります[50]。 |
| 腸内微生物の変化と免疫代謝疾患の間には強い関連性があることが新たなエビデンスによって示されており(表2)、疾患の病因、予防、治療へのアプローチにおけるパラダイムシフトが求められています。腸内微生物叢の調節は、代謝の健康増進、全身性炎症の軽減、免疫調節の改善といった、変革をもたらす可能性のある戦略として認識されつつあります。こうした変化の激しい状況において、食事療法、微生物叢を標的とした治療法(糞便微生物叢移植(FMT)など)、そして個別化医療は、トランスレーショナルリサーチと臨床的意義において有望な分野となっています[51]。(訳者注:トランスレーショナルとは、本来"基礎から臨床への橋渡し(Bench to Bedside)"をいいます。) |
表2. 代謝性疾患における微生物叢の変化。 略語:SCFA(短鎖脂肪酸)、TLR(Toll様受容体)、Treg(制御性T細胞)、GPR(Gタンパク質共役受容体)。 |
 |
 |
 |
| 2. 腸内細菌叢と免疫 |
| ヒトの消化管は、地球上で最も複雑な生態系の一つであり、多様な生態学的ニッチにまたがる広範な微生物群集を特徴としています。この相互に連結したシステムは、複雑かつ繊細な制御ダイナミクスの下で、数千年にわたりヒト宿主と共進化してきました。この共生関係において、人体はもはや孤立した存在ではなく、むしろ統合された超個体、つまり「非自己」と特定される微生物宇宙との融合体、すなわち「メタ個体」とみなされます[52]。 |
| 腸内細菌叢の注目すべき役割の一つは、幼少期における免疫系の発達と分極化への影響です[53,54]。腸内微生物群集は、非アトピー性免疫プロファイルの確立と経口免疫寛容の促進に極めて重要な調節機構を活性化する重要な抗原負荷を提供します[55]。 |
| 2.1. 腸内細菌叢、腸管上皮細胞、および腸管関連リンパ組織シグナル伝達 |
| 腸管内容物と腸管関連リンパ組織(GALT)との間の動的な境界として機能する単層の腸管上皮細胞は、恒常性維持に重要な役割を果たしている。この界面は洗練された防御バリアであり、抗原輸送を媒介し、自己と非自己の識別を促進することで粘膜の完全性を確保する[56]。腸内細菌叢、腸管上皮細胞、および腸管関連リンパ組織間の恒常的な交換は、免疫調節機能につながり、粘膜バリアを強化しながら免疫恒常性を維持する[57]。この緻密に調整された相互作用が破綻すると、腸管透過性の亢進、経口耐性の喪失、炎症、そしてそれに続く組織損傷など、一連の病因的イベントが引き起こされる可能性がある[58]。これらの破壊はアレルギーや自己免疫疾患などの免疫介在性疾患の発症に関与していると考えられている[59]。 |
| 宿主生物は、miRNA(マイクロRNA)などの特異的因子や、抗菌ペプチド、粘液、IgAなどの非特異的因子を介して腸内細菌叢に影響を与えます。これらの因子は、特定の細菌属の増殖を促進し、他の細菌属の増殖を抑制します[60]。miRNAの発現制御は、腸管恒常性の維持と病態の予防に特に重要です。非コードmiRNAである内因性および外因性(食物由来)miRNAは、細菌遺伝子発現の調節、上皮バリアの完全性の維持、アポトーシスの制御、腸管上皮細胞の増殖と分化の制御において重要な役割を果たします[61,62]。(訳者注:マイクロRNA(miRNA)は、約21〜25塩基の長さを持つ一本鎖の機能性RNA(ノンコーディングRNA)です。タンパク質には翻訳されず、メッセンジャーRNA(mRNA)に結合してその翻訳を抑制することで、遺伝子の発現を微調整する役割を担っています。がんや分化、発生など多様な生物学的プロセスに関与しており、血液や体液中に安定して存在することから、新しい診断法や治療薬の標的として研究が進められています。) |
| この統合システムの変化は、全身の免疫バランスを維持する上でのその極めて重要な役割を強調しています。ヘルパーT細胞(CD4 Th細胞)は、他の免疫細胞の活動を制御するサイトカインを産生することにより、獲得免疫において中心的な役割を果たしています。Th1またはTh2サブタイプへの分化は、環境からの刺激と抗原提示細胞(APC)の影響を受けます。インターフェロン-γ(IFN-γ)やインターロイキン-12(IL-12)などのサイトカインはTh1細胞への分化を促進し、IL-4、IL-2、IL-13などのインターロイキンはTh2細胞への分化を促進します。健康な個人では、特定の環境抗原に対してTh1指向の免疫応答が優勢であるのに対し、アレルギー表現型の個人ではTh2サイトカインパターンが優勢です[63]。 |
| 2.2. リンパ球集団間の洗練されたバランス |
| 子宮内では、母体の免疫系は、部分的に父方の遺伝的要素に由来する胎児抗原の存在に直面する。この非自己抗原性プロファイルは、胎児をTh1サイトカイン応答を介した免疫拒絶の潜在的なリスクにさらす。しかし、妊娠中の胎児のTh2分化により、このリスクは回避される。出生後、この免疫指向はウイルスや細胞内病原体と闘うには不十分となり、幼少期にTh2優位プロファイルからTh1優位プロファイルへの免疫移行が必要となる。アトピー性傾向のある人は、このプロセスを推進するために必要なIFN-γやIL-12などのサイトカインの量が不十分なため、免疫移行が不完全または不完全となる可能性がある[64]。 |
| 1989年にストラチャンによって提唱された「衛生仮説」は、幼少期の感染性因子や抗原への曝露がTh2からTh1への免疫転換プロセスを触媒する上で重要であると仮定している[65]。 |
| 先進国におけるアレルギー疾患の劇的な疫学的増加は、感染症、特に糞口感染による感染症への曝露の減少が一因とされている。衛生習慣の改善、ワクチン接種プログラムの普及、そして抗生物質の広範な使用は、こうした曝露を総合的に減少させてきた。ジェラードは、アレルギー疾患の有病率の上昇を、小児感染症や寄生虫感染からの解放のために社会が支払う代償であると、挑発的に表現している[66]。 |
| しかしながら、免疫応答の基盤となる生物学的メカニズムは、当初「衛生仮説」によって提唱されたTh1/Th2パラダイムよりも複雑です。抗原刺激はTh1応答またはTh2応答のいずれか一方のみを誘発するわけではなく、免疫システムの多面的な性質を浮き彫りにしています。さらに、Th2応答を主因とするアレルギー疾患の急増に伴い、1型糖尿病(T1D)、セリアック病、慢性炎症性腸疾患など、Th1の過剰活性化に関連する疾患も同時に、そして顕著に増加しています。これらの観察結果に対処するため、衛生仮説は改訂・拡張され、「再考された衛生仮説」[67]と呼ばれています。 |
| 出生後の微生物コロニー形成の枠組みの中で、腸内細菌叢と腸管関連リンパ組織(GALT)樹状細胞との早期相互作用は、寛容と免疫活性化を制御するメカニズムを誘発します。このダイナミクスには、様々なリンパ球集団間の高度な均衡が関与しています[68]。このような恒常性維持の枠組みにおいて、制御性Tリンパ球(Treg)が中心的な役割を担い、IL-10やTGF-βなどの主要な免疫調節性サイトカインの産生によって支えられています[69,70]。 |
| 制御性Tリンパ球はTヘルパー細胞サブセットの中で重要な役割を果たします。実際、制御性Tリンパ球は明確なサイトカイン発現プロファイルによって定義され、胸腺由来の天然型制御性Tリンパ球(nTreg)と末梢組織由来の誘導型制御性Tリンパ球(iTreg)に分類されます。これらの誘導型制御性Tリンパ球は、炎症を抑制し免疫抑制効果を発揮するために不可欠なサイトカインであるTGF-βとIL-10の分泌を主に担っています[71]。 |
| 腸内には、広範かつ多様な細菌細胞集団が定着しており、そのゲノム全体はヒトゲノムの150倍にも達します。この細菌細胞集団は、有益な抗原レパートリーを提供します。この微生物叢とその遺伝子内容(マイクロバイオームと呼ばれる)は、制御性Tリンパ球細胞によって制御される制御ネットワークを活性化し、Th2優位(アレルギー性)またはTh1優位(自己免疫性)のいずれかへの免疫分極化を防ぐ役割を果たします[72]。微生物叢のこの制御機能は、感染症の制御機能を凌駕しています。感染症は、歴史的に衛生仮説において、まだ慣らし段階にある免疫システムの成熟を促進する触媒として強調されてきました[73,74]。 |
| 2.3. 腸内細菌叢と出産方法 |
| 腸内細菌叢は免疫学的に活性な「細菌器官」として機能し、発達初期の自然免疫と獲得免疫の両方のプログラミングに寄与する[75]。幼少期には、多くの内因性および外因性因子が腸内細菌叢の構成を大きく左右する。これらの因子には、遺伝、分娩方法(経膣分娩または帝王切開)、周産期の抗菌薬使用、妊娠週数、アプガースコア、分娩場所(病院または自宅)、乳児の栄養方法(母乳、人工乳、混合)、代替栄養の期間と質、母乳オリゴ糖残留量、妊娠中の体重増加、アトピーレベル、BMI、そして最後にペットとの接触などが含まれる[76]。 |
| 経膣分娩の過程を通じて、母親は新生児に「微生物遺伝」を伝え、口腔、呼吸器、泌尿生殖器、消化管などの皮膚や粘膜表面における母体微生物と環境微生物の定着を促進する。そのため、経膣分娩で生まれた満期新生児の微生物叢は、バクテロイデス属(バクテロイデス門)、ビフィドバクテリア属(放線菌門)、乳酸菌属(フィルミクテス門)、腸内細菌科(プロテオバクテリア門)などの属が優勢な好ましい種の多様性を示し、これらの属はユービオシスと呼ばれる均衡のとれた共生状態を維持している。対照的に、帝王切開で生まれた新生児は、微生物叢の組成に著しい乱れ(ディスバイオシス)を示し、これは機能的転帰に影響を及ぼす質的および量的変化を特徴とする [77,78]。 |
| 帝王切開、長期入院、早期または長期の抗生物質使用などによって引き起こされる出生後の不十分なコロニー形成は、様々な免疫介在性疾患および代謝性疾患の病因となるディスバイオシス状態の決定因子として作用します[79,80]。ディスバイオシス状態においては、腸管バリア成熟の遅延(「腸閉塞」)、細菌および食物抗原の転座、免疫調節異常、局所炎症など、一連の有害事象が発生します[81](図2)。 |
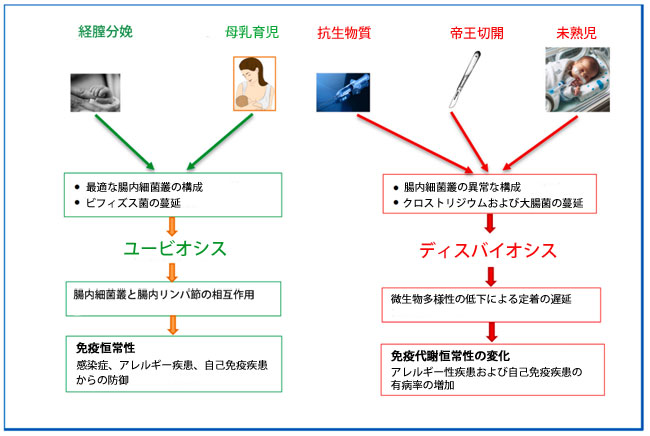 |
| 図2. ユービオシスとディスバイオシス |
| ユーバイオシス(真正腸管機能維持)の間、寛容原性樹状細胞はTGF-βと呼ばれるサイトカインを分泌する。このサイトカインは制御性Tリンパ球細胞集団を誘導し、Th2を介したアレルギー経路とTh1を介した自己免疫反応の過剰活性化を抑制する[82]。対照的に、帝王切開に伴う腸内細菌叢異常(ディスバイオシス)では、クロストリジウムと大腸菌の過剰増殖が頻繁にみられ、これらはIL-1β、IL-6、TNF-αなどの炎症性サイトカインの産生を促進する。これらのサイトカインはさらにTh17リンパ球の増殖を促進し、タイトジャンクションの完全性を破壊し、腸管透過性を高める[83]。新たなエビデンスにより、微生物叢は免疫調節だけでなく、体重管理、エネルギー恒常性、全身性炎症などの重要な生理学的プロセスにも関与していることが示唆されており、肥満の病態生理学と深い関連がある[84,85]。 |
| 3. 腸内細菌叢とアレルギー |
| 免疫システム(IS)自体は、化学的メディエーター、細胞要素、生物学的構造、そして進化の過程で発達した動的プロセスからなる複雑に統合されたネットワークであり、物理的、化学的、生物学的な外的脅威から生体を防御します。免疫システムは、自然免疫と獲得免疫、あるいは体液性免疫と細胞性免疫といったサブシステムに細分化できます。その中核機能は、自己分子と非自己実体を区別することであり、非自己実体には、ウイルス、細菌、真菌、蠕虫由来の病原性代謝物など、多様な因子が含まれます[86]。 |
| 免疫システムは宿主の恒常性維持に不可欠な調節因子として機能し、微生物や環境因子に遭遇した際に組織の機能を維持・回復することを可能にする[87]。獲得免疫に関連する免疫システムサブシステムの出現は、複雑な微生物叢の発達と並行しており、このシステムの大部分が多様な微生物群との共生的相互作用を維持するために進化したという考えを強めている。これらの微生物群は、免疫システムの様々な側面に影響を与え、制御している[88]。 |
| 免疫システムは、必要に応じてその活動を調整しながら、細かく調整された動的なバランスとして機能します。このバランスが崩れると免疫不全に陥り、再発性で生命を脅かす可能性のある感染症を引き起こします。この状態は、遺伝的要因、エイズなどの疾患、あるいは免疫抑制療法の使用に起因する可能性があります。逆に、バランスが上昇すると免疫の過剰活性化が引き起こされ、自己免疫として現れ、自身の組織が免疫攻撃の標的となります。一般的な自己免疫疾患には、1型糖尿病(T1D)、関節リウマチ、アレルギーなどがあります[89]。 |
| アレルギーは広く蔓延する健康問題です。先進国では、約15~25%の人がアレルギー性鼻炎を経験しています[90]。約6%の人が少なくとも1つの食物アレルギーを有しています[91]。また、約20%の人がアトピー性皮膚炎を患っています[92]。その他、地域によって異なりますが、人口の1~18%[93]が喘息に、0.05~2%がアナフィラキシーに罹患しています[94]。 |
| 3.1. エクスポソームの役割 |
| ここ数十年、疫学研究により、特に先進国においてアレルギーの有病率が増加していることが示されている[95]。遺伝的素因に加えて、エクスポソームと総称される環境因子が決定的な役割を果たしている。エクスポソームは、子宮内早期から遭遇するあらゆる環境的影響を包含し[96]、3つの重複する領域に分類できる。すなわち、一般的な外部環境(例:都市化、社会状況、ストレス、騒音、人工光)、特定の外部環境(例:化学物質汚染物質、食事、身体活動、タバコへの曝露、感染症)、そして内部環境(例:代謝プロセス、腸内細菌叢の構成、炎症、酸化ストレス)[97]である(フローチャート参照)。これらの領域は非常に動的であり、生涯を通じて進化し続ける[98]。これらの要因の中で、腸内細菌叢は、わずか数十年の間に生物多様性が大きく変化することから、支配的な役割を果たしていると思われます[99]。これは、何百万年にも及ぶ進化と比較すると、ほんの一瞬のことです。 |
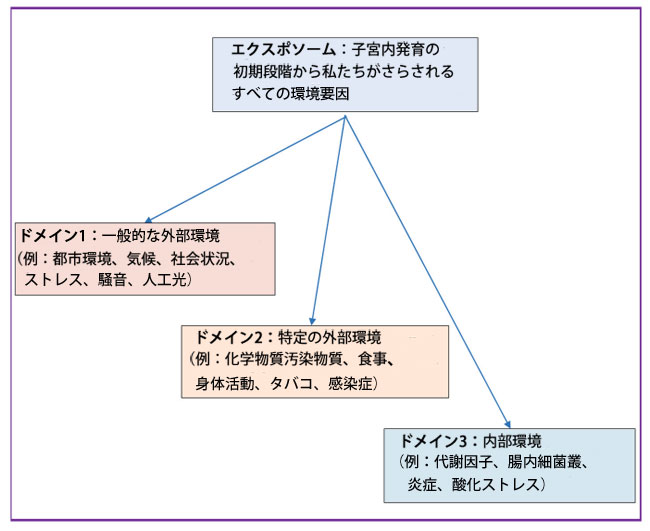 |
| エクスポソームの代表的なフローチャート |
| 代謝効率を促進する選択圧は、宿主と微生物叢の共進化を形作ってきたと考えられます。この長期にわたる統合により、微生物群集(消化管外を含む)と宿主との間に、代謝を超えて複雑な生理学的つながりが形成されました。これらの相互関係は、微生物叢と免疫系の相互作用において特に顕著です。この相互作用は、複雑な界間シグナル伝達プロセスと代謝調節を介して、免疫応答、代謝活動、内分泌経路に影響を及ぼします。腸内微生物叢は、その構成と食事および環境要因に応じた機能的ダイナミクスに応じて、宿主を保護することも、害を及ぼすこともできます。 |
| 胎児期から幼少期にかけて腸内細菌叢を確立することは、宿主の免疫系が外部刺激に対処し、適切に反応するために不可欠です。胎児の腸内細菌叢の変化は、生活習慣、食事、薬剤使用(特に抗生物質[100])といった母体要因によって子宮内で始まり、出産方法(経膣分娩 vs. 帝王切開)[101]や授乳方法(母乳育児 vs. 哺乳瓶授乳)[102]に応じて出生後にも変化が続きます。3歳までに微生物組成は急速に変化し、1歳までに成人の組成に近づき、3歳までに成熟した微生物群集へと安定します[103,104]。このように、この周産期は健康な微生物叢と回復力のある免疫系を育むために不可欠です。腸内細菌叢のディスバイオーシス(不均衡)は、乳児や小児の代謝および免疫機能に悪影響を及ぼす可能性があります。これらの混乱は、肥満[105]、1型糖尿病[106]、アレルギー[107]、自閉症スペクトラム障害[108]、非特異的炎症性腸疾患(IBD)[109]、発育不全[110]などのアレルギーおよび自己免疫疾患だけでなく、代謝の問題にも寄与します。 |
| 腸内細菌叢の乱れと、腸管、全身循環、他の臓器、末梢組織における免疫応答との関連性は確立されている[56]。特に、腸内細菌叢の乱れとアレルギー発症との間には高い相関関係があることは注目に値する。例えば、アトピー性皮膚炎と診断された乳幼児の約80%が、後にアレルギー性鼻炎または喘息を発症する[111]。この進行は、いわゆる「アレルギーマーチ」と一致しており、これは小児期におけるアトピー性皮膚炎や食物アレルギーから始まり、喘息やアレルギー性鼻炎へと進行する、アレルギー疾患の連続的な発症を詳述している[112]。 |
| 3.2. 微生物叢と喘息の免疫学的要素 |
| 喘息は、呼吸器系の慢性炎症性疾患であり、息切れ、咳嗽、喘鳴などの反復症状を特徴とする[113]。喘息に関与する免疫応答機構は完全には解明されていないが[114]、炎症とアレルゲン感受性が喘息の病態生理において重要な役割を果たしていることは明らかである[115]。研究では、微生物代謝物(主に乳酸菌が産生する短鎖脂肪酸)が保護作用および免疫調節作用を有する可能性が示唆されている。短鎖脂肪酸は、CD4前駆細胞および樹状T細胞から制御性T細胞の産生を刺激し、Gタンパク質共役受容体(GPR)を活性化し、ヒストン脱アセチル化酵素を阻害することで、重要な影響を及ぼす[116]。微生物叢は、喘息に関連する炎症反応において中心的な役割を果たしている[117]。妊娠中の母親の喫煙[118]、母親の喘息の既往[119]、妊娠中の抗生物質の使用[120]、食事[121]、出生前のストレス[122]などの要因は、喘息のリスク増加に関連しています。 |
| さらに、研究では微生物多様性の低下(ディスバイオシス)と呼吸器疾患との関連が実証されている [123]。胃腸系と呼吸器系の両方におけるディスバイオシスは、免疫システムの反応を変化させることで喘息の病態生理に大きく寄与している [124]。研究では、母親の膣微生物叢から移行した細菌、新生児の IgE レベル、アレルギー性免疫調節との間に関連があることが示されている [125]。胎便中の ラクトバチルス・ジェンセニなどの特定の抗原の存在は、子宮内で特定の免疫機能を抑制し、幼少期にアレルゲンに対する免疫寛容を促進する可能性があることを示唆している [126]。興味深いことに、膣微生物叢におけるラクトバチルス 属の優位性は、乳児の生後 1 年目に IgE 産生を誘発する可能性があるため、喘息の発症感受性と関連している [127]。さらに、遺伝的要因も腸内細菌叢の形成とそれに続く喘息の発症に影響を与えているようだ[128]。 |
| 3.3. 微生物叢とアトピー性皮膚炎 |
| 科学的根拠によれば、アトピー性皮膚炎の60%は生後1年以内に発症し、多くの場合乳児湿疹として現れることが示されています[129]。腸内細菌叢の乱れは、免疫プロセスに対する調節作用と相まって、アトピー性皮膚炎の発症に大きな役割を果たしています。微生物叢の有益な特性には、炎症関連のアレルギー性疾患や自己免疫疾患から保護する制御性T細胞の産生を促進することが含まれます[130]。アレルギー性鼻炎や感作においては、細菌の多様性がしばしば減少しますが、この現象はアトピー性皮膚炎と密接に関連しているようには見えません。 |
| 3.4. 腸内細菌叢の乱れとアレルギー |
| 健康な膣内細菌叢は、小児のアレルギー発症率の低下と相関関係にある[131]。一方、L.フォルニカリスやG. ヴァギナリスといった菌種の蔓延は、膣内の腸内細菌叢の乱れや炎症と関連しており、リポ多糖類の産生を通じてアレルギー発症を促進する[132]。生活習慣などの出産後の要因は、消化管微生物環境を大きく左右し、腸内細菌叢の乱れを促し、時間の経過とともにアレルギー感受性を高める[133]。寄生虫やその他の微生物への曝露も、免疫系の反応性やアレルゲン産生に影響を与える[134]。研究では、出産方法などの様々な要因に応じて、母親の腸内細菌叢が乳児の腸内細菌叢に密接に影響を与えることが強調されている[135]。さらに、栄養[136]、プロバイオティクスの使用[137]、抗生物質の投与[138]は、微生物叢の発達と早期定着に大きな影響を与えます。これらは免疫反応の形成を助け、最終的には健康結果に影響を与える要因です[51]。 |
| 食物アレルギーの増加は、公衆衛生および経済的に大きな懸念を引き起こしている [91]。腸内細菌叢は、免疫応答を調節することで、保護バリアとして機能することも、食物アレルギーの引き金となることもあるという証拠がある [139]。何度も述べたように、腸内細菌叢は数百種に及ぶ数兆個の細菌で構成されており、個人間で大きく異なる [140]。健康な腸の免疫系は通常、常在微生物に対する寛容性を維持しているが、その破綻は食物アレルギーの一因となる炎症誘発状態につながる可能性があり、これは腸の免疫環境の恒常性バランスを崩す炎症誘発性変化に関連している [141]。保護細菌とアレルギー誘発細菌の両方が、Th1ヘルパーリンパ球の刺激とTh2媒介経路の抑制を介して免疫応答を調節する能力があることが特定されている [142]。微生物叢特異的制御性T細胞などの微生物叢を介したメカニズムは、アレルギー性炎症の抑制に重要な役割を果たしている[143]。しかし、免疫細胞が食物抗原特異的制御性T細胞の形成をどのように調整するか、そして微生物叢がその機能にどのように寄与するかについては、まだ十分に解明されていない[144]。 |
| 腸内細菌叢は、新生児の腸管免疫系の形成と成熟において重要な役割を果たします。特定の糞便微生物プロファイルは、乳幼児のアレルギー素因と関連付けられています[[145], [146], [147]]。観察研究では、食物アレルギーのある小児における細菌叢の経時的変化が、年齢層別に調査され、アレルギー発症との相関関係を示唆する可能性のある細菌門の違いが明らかになっています[148]。例えば、母親のホルデマニア属細菌の濃度と、子孫の食物アレルギーリスクの低下との関連が示唆されており、その潜在的な保護的役割が示唆されています[149]。さらに、クロストリジウム属、特定のビフィドバクテリウム属の増加[150]、大腸菌の増加[151]といった微生物組成の不均衡、ならびに食事、分娩方法、環境曝露、細菌の定着時期に関連した短鎖脂肪酸産生の変化が、アレルギー疾患と関連付けられている[152]。これらのエビデンスは、バランスと多様性(ユーバイオシス)を特徴とする母体微生物叢が、胎児および新生児の適切な免疫発達を確保し、アレルギーリスクを軽減する上で不可欠であるという前提を強く支持している[153]。 |
| 4. 腸内細菌叢と肥満 |
| 腸内細菌叢の異常なパターンは、肥満やその他の非感染性疾患の特徴である低レベルの炎症と関連していることが報告されている[154]。腸内細菌叢の異常と肥満の間には、ヒトと動物の両方の研究によって裏付けられた、十分に裏付けられた関連性がある[155]。例えば、西洋式の食事を与えられた実験動物では、優勢な細菌門に顕著な変化が見られる。具体的には、フィルミクテス門(例えばクロストリジウム)が増加し、バクテロイデス門が減少する[156]。これは肥満者にも同様のパターンが観察される[157]。 |
| 前向き研究によるエビデンスによると、小児期の腸内細菌叢の構成変化は、しばしば過体重や肥満の発生に先行する[158,159]。特定の細菌属の蔓延は重要であるように思われる。例えば、母乳育児や経膣分娩児に多くみられるビフィズス菌の菌数増加は過体重リスクの低下と関連している一方、バクテロイデス・フラギリスの優勢は肥満リスクの上昇と相関している[160]。 |
| 高脂肪食は、ビフィズス菌と乳酸菌の減少と、フィルミクテス菌とプロテオバクテリアの増加を促し、ディスバイオシスをさらに悪化させます[161]。肥満児および成人のディスバイオシスパターンは、バクテロイデス菌の減少、フィルミクテス菌の増加、放線菌門などの細菌門の頻度の変化を特徴とします[162,163]。 |
| 4.1. 肥満の腸内細菌叢異常のメカニズム |
| 腸内細菌叢異常と肥満を結びつける複雑なメカニズムが徐々に解明されつつある[164,165]。 |
| 腸内細菌叢の乱れは、腸管透過性の変化、グラム陰性細菌の細胞壁の構成成分であるリポ多糖(LPS)の血漿中濃度の上昇、インターロイキン(IL-1β、IL-6)や腫瘍壊死因子α(TNF-α)などの全身性炎症性サイトカインの増加を引き起こします。これらの因子は、持続的な低レベルの炎症とエンドカンナビノイドシステム(ECS)の調節不全に寄与し、これらが相まってエネルギー恒常性と肥満に影響を与えます[166,167]。 |
| リポ多糖は、活性化B細胞核因子κ軽鎖エンハンサー(NF-κB)の活性化を介して、ゾヌリン-1やオクルディンなどのタイトジャンクションタンパク質のダウンレギュレーションによって腸管透過性を媒介しますが、その一方で、インターロイキン(IL-1β、IL-6)や腫瘍壊死因子α(TNF-α)などの炎症性サイトカインは、局所および全身性炎症の原因です[168]。結果として生じる炎症性環境は、ディスバイオシスによって引き起こされる炎症が、脂肪組織の炎症を含む全身的影響を伝播するという「代謝感染」仮説を支持しています[169]。メタボリックシンドローム(MS)の患者は重篤なエンドトキシン血症を発症します[170]。エンドカンナビノイドシステムの過剰活性化は、ディスバイオシスに関連して、腸管透過性を高め、リポ多糖媒介炎症を増幅させることで脂肪生成を刺激します[171](図3a)。 |
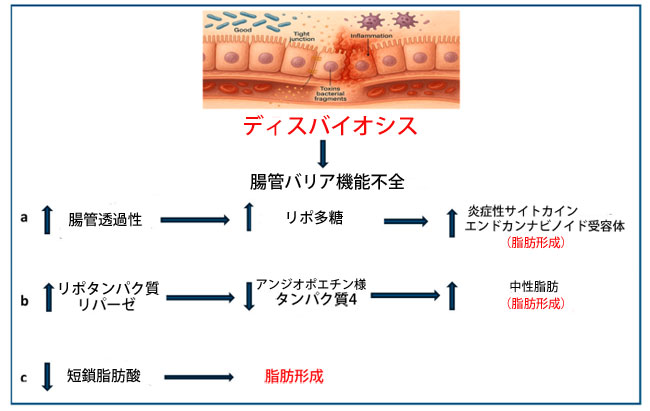 |
| 図3. 腸内細菌叢の異常と肥満のメカニズム |
| 4.2. 肥満と糖尿病の関連性 |
| マウスモデルを用いた研究では、腸内マイクロバイオームがエネルギー管理および体重調節に関与していることが示唆されている[172]。これらのプロセスには、腸管上皮におけるアンジオポエチン様タンパク質4(ANGPTL4)の発現調節が関与していると考えられる。アンジオポエチン様タンパク質4は、断食誘発性脂肪因子(FIAF)としても知られ、脂質およびグルコースの恒常性の調節や血管新生の促進など、様々な役割を果たしている[173]。アンジオポエチン様タンパク質4はリポタンパク質リパーゼ(LPL)活性を阻害することで、組織、特に脂肪組織におけるトリグリセリドの取り込みと蓄積を抑制し、脂肪分解を促進する[174](図3b)。糖尿病[175]および肥満[176]の患者では、血清中のアンジオポエチン様タンパク質4濃度が低いことが観察されている。動物実験や試験管内実験では、腸内細菌叢が腸内アンジオポエチン様タンパク質4の発現に大きく影響し、それによって脂質の蓄積や体重に影響を与えることが示唆されている[177]。 |
| 短鎖脂肪酸は、消化されない食物炭水化物の細菌発酵によって生成される代謝物である[178]。メタボローム解析により、短鎖脂肪酸のプロファイルは腸内生態系における様々な細菌属間の相乗効果を反映していることが明らかになった。間接栄養素として、短鎖脂肪酸(酢酸、プロピオン酸、酪酸を含む)はエネルギー代謝と脂肪組織の拡張に重要な役割を果たし、代謝調節因子として機能する[179](図3c)。 |
| メタゲノム研究では、特定の腸内細菌、その遺伝子、および腸内代謝物と2型糖尿病(T2D)との強い相関関係が強調されています。特に、ローズブリア・インテスティナリスやフェカリバクテリウム・プラウスニッツィ、などの酪酸産生細菌の値が2型糖尿病患者で低いことが検出されており、短鎖脂肪酸産生の低下が肥満、糖尿病、および関連する代謝障害の一因となる可能性が示唆されています[179]。 |
| 5. 腸内細菌叢と糖尿病 |
| 2型糖尿病は、世界中で早期死亡の80%を占めています。薬物療法が利用可能であるにもかかわらず、2045年までに約7億人が2型糖尿病に罹患すると予測されています[180]。この疾患は、膵臓のインスリン産生不全またはインスリン感受性の低下による血糖値の上昇を特徴とします[181]。糖尿病およびそれに関連する代謝機能障害(高血圧、脂質代謝障害、酸化ストレスなど)の管理が不十分だと、様々な大血管合併症(例:冠動脈疾患、脳卒中、末梢血管疾患)や微小血管合併症(例:腎症、神経障害、糖尿病網膜症)[182]を引き起こす可能性があり、さらに相互に関連する代謝経路の破綻も引き起こします[183]。 |
| 2型糖尿病患者は健常者と比較して腸内微生物叢が変化しており[184]、共生細菌の多様性の低下と日和見病原体のレベルの増加がみられます[185]。これらの微生物叢の変化は、グルコース代謝、インスリン抵抗性、慢性炎症などの重要なメカニズムに影響を及ぼすことで、糖尿病の発症と進行を促進します[186]。また、特定の腸内細菌は短鎖脂肪酸の産生を調節することでインスリン感受性に直接影響を与えます[187]。さらに、腸内微生物叢は様々な食事成分の分解を通じて、宿主の食事に対する代謝反応を調節します[181]。 |
| 5.1. 腸内細菌による代謝調節 |
| 腸内細菌叢は、食物の消化以外にも、腸管上皮細胞の約1%を占める、小規模ながらも多様な腸内分泌細胞(EEC)と相互作用しています。消化管に沿って分布する腸内分泌細胞は、宿主の代謝、消化、腸管運動、胃内容排出、そして腸管全体の健康状態を調節する最大20種類のホルモンを産生・放出します[188]。これらの細胞は、腸内細菌叢とその代謝産物(タンパク質、炭水化物、胆汁酸の発酵または酵素分解によって生成されるもの)と密接に相互作用します。これらの代謝産物には、短鎖脂肪酸、分岐鎖脂肪酸、二次胆汁酸、そして腸管運動に影響を与えるインドールなどのトリプトファン由来の異化産物が含まれます[189]。腸内細菌叢、腸内分泌細胞、そして代謝の相互作用は非常に複雑であり、これらの構成要素は相互に影響を与え合っています。この動的な関係は、胃内容排出、腸管運動、食習慣、エネルギー代謝など、多くの生理学的プロセスを支配しています。そのため、腸内細菌叢と腸管上皮細胞(EEC)間のコミュニケーションの破綻は、糖尿病の前兆となるインスリン抵抗性などの代謝変化につながる可能性があります[190]。 |
| 5.2. 腸内細菌叢の乱れと糖尿病 |
| 多くの研究により、腸内細菌叢の変化と糖尿病の発症機序との間には重要な関連性が認められています。特に、バクテロイデス門とフィルミクテス門の比率の変化は、腸管透過性亢進と関連付けられています[191]。このバランスの崩れは、腸管バリアの損傷を介した微生物副産物の移行を促進し、糖尿病に特徴的な炎症プロセスを引き起こします。短鎖脂肪酸産生細菌、特に酪酸産生細菌の顕著な減少も2型糖尿病と相関しており、これらの代謝物はインスリン感受性の調節に重要であるためです[192]。 |
| 特定の細菌株は、炎症誘発マーカーを減少させ、腸管バリアの完全性を維持することで糖尿病に対する保護効果を示すことが示されています。これらの有益な微生物には、ラクトバチルス・ファーメンタム、プランタラム、カゼイ、ロゼブリア・インテスティナリス、バクテロイデス・フラギリス、アッカーマンシア・ムシニフィラなどがあります。これらの種は、グルコース代謝を促進し、インスリン感受性を改善し、炎症誘発性サイトカインの産生を緩和する可能性を示しています[182]。さらに、腸内マイクロバイオームは、肝臓でのグルコース産生を抑制し、インスリン感受性を改善し、筋肉および肝臓組織におけるグルコースの取り込みを促進する抗糖尿病薬であるメトホルミンの有効性と消化管耐性の両方を調節する上で不可欠です[193]。動物およびヒトの研究では、メトホルミンの補給は、ブラウティア、ブチリシコッカス、アッカーマンシア・ムシニフィラなどのいくつかの短鎖脂肪酸産生分類群の増加と関連しており、回腸杯細胞の増殖を促進し、腸管透過性を低下させ、内毒素血症を低下させ、Toll様受容体シグナル伝達経路を強化することが示唆されています[194]。 |
| 糖尿病性腎症に関しては、最近の知見から腸内細菌叢の乱れ、特にプレボテラ属、ルミノコッカス科、ロゼブリア属、フェカリバクテリウム属などの善玉菌の減少が腸内細菌叢の乱れの影響を強く示唆しています。同時に、パラバクテロイデス属、エンテロコッカス属、腸内細菌科、クレブシエラ属など、潜在的に病原性のある細菌群の増加も報告されています[195]。 |
| 同様に、糖尿病網膜症患者では腸内細菌叢の変化が観察されており、バクテロイデス門と放線菌の減少と、アシダアミノコッカス、大腸菌、エンテロバクターの増加が特徴的である[196]。 |
| 糖尿病性神経障害は、フィルミクテス門、放線菌、大腸菌・赤痢菌、ラクノクロストリジウム、ブラウティア、メガスファエラ、ルミノコッカスなどの細菌叢の異常増加と、バクテロイデス門およびフェカリバクテリウムの減少という明確な微生物叢異常とも関連している[197]。 |
| 6. 腸内細菌叢とバイオモジュレーター |
| 周産期は、発達中の免疫系が環境の影響に対して感受性が高まる重要な時期です。この時期の免疫系調節のための一般的な戦略は、アレルゲン除去(抑制的アプローチ)から、腸内細菌叢を標的としたより積極的な介入(促進的アプローチ)へと移行し、ナイーブな免疫応答を形成しています[77,78]。腸内細菌叢と免疫系の複雑な相互作用に関する理解の進歩により、プレバイオティクスとプロバイオティクスを含む栄養介入を通じて、妊娠中の母体の免疫と乳児期初期の新生児の免疫発達を最適化するための取り組みが推進されています[198]。 |
| 腸内細菌叢の構成を「操作する」という概念の科学的起源は、20世紀初頭に生きた乳酸菌を含む発酵食品に治療効果を認めたウクライナのノーベル賞受賞者、イリヤ・メチニコフに遡ります。メチニコフの先駆的な洞察は、プレバイオティクス、プロバイオティクス(サイコバイオティクスを含む)、シンバイオティクス、パラプロバイオティクス、メタバイオティクス、ポストバイオティクスなど、微生物叢を標的とした治療法(総称して「バイオモジュレーター」)を活用するための現代的な枠組みの基盤となっています[199](表3)。 |
| 表 3. 腸内細菌叢バイオモジュレーターのさまざまなタイプ |
 |
| これらの各カテゴリーには、腸内微生物のバランスを維持または回復するためのさまざまな戦略が含まれており、最終的な目標は、腸内細菌叢の異常に関連する慢性疾患を予防または治療することです。 |
| 糞便微生物移植(FMT)は、厳格なスクリーニングを受けた健康なドナーから腸内細菌叢をディスバイオティックな状態のレシピエントに移植する技術であり、腸内微生物叢を改善するための有望な戦略の一つです。糞便微生物移植は、健全な生態系を回復させ、ひいては臨床的回復を促進することを目的としています。その有効性の正確なメカニズムはまだ部分的にしか解明されていませんが、再発性クロストリディオイデス・ディフィシル感染症[200,201]だけでなく、様々な慢性非感染性疾患 [202,203]に対する治療の可能性を裏付けるエビデンスが増えています。 |
| 6.1. 腸内細菌叢とプレバイオティクス |
| 国際プロバイオティクス・プレバイオティクス科学協会(ISAPP)は、プレバイオティクスを「宿主微生物によって選択的に利用され、健康効果をもたらす物質」と定義しています[204]。プレバイオティクスは、消化管での消化吸収に抵抗性があり、腸内細菌によって発酵されるため、宿主の健康に良い影響を与えます[205]。この発酵プロセスによって、腸内環境のpHを下げ、ラクトバチルス属、ビフィドバクテリウム属、バクテロイデス属などの小腸の善玉菌の増殖を促進する化合物が生成されます[206]。多くの植物性食品や蜂蜜、牛乳などの特定の動物性食品に自然に含まれるプレバイオティクスは、乳酸菌が産生する抗菌物質とともに、腸内細菌叢の構成と代謝機能を整え、健康をサポートし、病気を予防します[207]。プレバイオティクスの一般的な例としては、イヌリン、ガラクトオリゴ糖(GOS)、フラクトオリゴ糖(FOS)、ヒトミルクオリゴ糖(HMO)、キシロオリゴ糖(XOS)、マンナンオリゴ糖(MOS)、ラクツロース、ガラクトース誘導体、β-グルカンなどがあります[208]。さらに、フラボノイド[209]、多価不飽和脂肪酸(PUFA)[210]、グルコオリゴ糖[211]などのポリフェノールもプレバイオティクスの候補と考えられています。 |
| プレバイオティクスの臨床的意義は腸内環境だけにとどまりません。短鎖脂肪酸産生をサポートし、ユーバイオシスを促進することで、プレバイオティクスは免疫寛容、腸内バリア機能の改善、そして代謝調節に貢献します。近年のエビデンスでは、プレバイオティクスの摂取が、肥満、2型糖尿病、炎症性腸疾患、アレルギー疾患など、いくつかの慢性疾患のリスク低減または緩和につながることが示唆されています[206]。さらに、ヒトミルクオリゴ糖などの特定のプレバイオティクスは、乳児期の腸内細菌叢の形成に重要な役割を果たしており、将来の免疫介在性疾患への感受性に影響を与える可能性があります[212]。 |
| 予防と治療の観点から、プレバイオティクスは、標的を絞った食事戦略がいかにして腸内細菌叢の健康を維持し、疾患リスクを低減するかを示しています。しかしながら、臨床研究では、プレバイオティクスの種類、投与量、治療期間、そして患者特性の違いにより、結果にばらつきがあることが示されています。これらの方法論的課題に対処することは、プレバイオティクスを腸内細菌叢を中心とした予防と治療のための信頼できるツールとして確立するために不可欠です。 |
| 6.2. 腸内細菌叢とプロバイオティクス |
| プロバイオティクスは、適切な量を摂取することで宿主に健康上の利益をもたらす生きた微生物と定義されています[213]。これらの微生物は、抗菌物質を産生し、免疫応答を増強し、有害な細菌が上皮に付着するのを防ぎ、粘膜IgA産生を刺激し、細菌毒素の産生を阻害します[214]。乳酸菌は、糖類を発酵させて乳酸を産生するため、消化管細菌の中でも特に重要です。プロバイオティクスは、短鎖脂肪酸、ビタミン、バクテリシジンの産生にも寄与し、胆汁酸代謝にも関与しています。ケフィア、ヨーグルト、漬物、味噌、キムチなどの発酵食品に豊富に含まれています[215]。 |
| 臨床的には、プロバイオティクスは慢性の非感染性疾患の広範な領域で研究されてきました。抗生物質関連下痢症や過敏性腸症候群などの消化器疾患、ならびにアトピー性皮膚炎やアレルギー性鼻炎などの免疫介在性疾患におけるその役割を裏付けるエビデンスも存在します。腸-脳軸を調節するプロバイオティクスの能力は精神医学の関心も集めており、サイコバイオティクスと呼ばれる特定の菌株[216]が不安[217]や抑うつ症状[218]を軽減することが示されています。さらに、予備試験では、プロバイオティクスの補給が代謝調節、心血管リスクプロファイルの改善、さらには免疫調節[219]と抗炎症経路を介したがん予防戦略の改善につながることが示されています。これらの有望な知見にもかかわらず、プロバイオティクスの治療的使用は、臨床結果の大きなばらつきによって課題となっています。有効性は、菌株特異的な特性、投与量、介入期間、そしてベースラインの微生物叢構成や免疫状態といった宿主関連因子に依存するようです。さらに、脆弱な集団(例:免疫不全患者、早産児)では、プロバイオティクスはリスクを伴う可能性があり、慎重な菌株選択と安全性評価の重要性が浮き彫りになっています[220]。 |
| プロバイオティクスは、標的微生物の補充がユーバイオシスを維持または回復させることで、疾患の予防と治療にどのように活用できるかを示す好例です。しかし、その可能性を一貫した臨床実践に活かすには、最適な菌株、治療レジメン、そして患者選択基準を明らかにするための大規模かつ標準化された試験が必要です。 |
| 6.3. 腸内細菌叢とシンバイオティクス |
| シンバイオティクスは、プロバイオティクスとプレバイオティクスを組み合わせることで、宿主の健康に相乗効果をもたらします[215]。国際プロバイオティクス・プレバイオティクス科学協会の見解に一致して、シンバイオティクスは、宿主微生物に摂取されると有益な効果をもたらす生きた微生物と基質の組み合わせを指します[221]。この二重のアプローチは、有益な微生物に供給すると同時に、それらの生存、定着、および代謝活性を高める基質を提供することを目的としています。 |
| プロバイオティクスの機能的役割には、腸内細菌叢のアンバランス調整、免疫機能の強化、肥満予防などが含まれます[222]。プロバイオティクスとプレバイオティクスの組み合わせは有望な研究分野ですが、栄養補助食品におけるその有効性を裏付ける科学文献は依然として限られています。一般的なシンバイオティクス製剤には、ラクトバチルスGGおよび/またはビフィズス菌と、オメガ3脂肪酸、フラクトオリゴ糖、またはイヌリンを組み合わせたものがあります[223]。 |
| 臨床的には、シンバイオティクスはアレルギー予防、代謝障害、消化器疾患など、様々な分野で研究されています。予備研究では、2型糖尿病における血糖コントロールの改善、アレルギー疾患における免疫寛容の増強、肥満における体重管理のサポートといった効果が示唆されています。また、シンバイオティクスの潜在的可能性は、全身性抗炎症作用が特に重要な腫瘍学や心血管代謝疾患にも及びます[224]。 |
| しかし、シンバイオティクスは理論的には魅力的であるにもかかわらず、プロバイオティクスやプレバイオティクス単独の場合と比較すると、科学的エビデンスは依然として限られています。臨床転帰は、研究対象となる菌株、プレバイオティクス基質、そして患者集団によって大きく異なります。したがって、シンバイオティクスの有効性を明らかにし、プロバイオティクスやプレバイオティクス単独投与と比較してシンバイオティクスが明確な利点を示す状況を特定するには、処方の標準化と厳格な臨床試験が不可欠です。 |
| トランスレーショナルな視点から見ると、シンバイオティクスは、微生物叢を標的とした戦略を個別に組み合わせることで、治療および予防介入をいかに強化できるかを示しています。しかし、その成功は、方法論の多様性を克服し、食事、微生物、そして宿主因子を統合する精密医療アプローチへと前進することにかかっています。 |
| 6.4. 腸内細菌叢とパラプロバイオティクス |
| パラプロバイオティクスという用語は、2011年に造語され、非生菌性のプロバイオティクス微生物またはその細胞成分を指します[225]。パラプロバイオティクスは、未熟児、免疫不全患者、敗血症または腸管バリア機能低下患者など、生菌によるプロバイオティクス投与がリスクとなる可能性のある状況において特に有用です[226]。このような場合、細菌の断片または代謝物を投与することで、生菌細胞に伴うリスクなしに、同様の治療効果が得られます[227]。パラプロバイオティクスは非生物性であるため、プロバイオティクスに比べて製造および保管が容易です[228]。また、細菌の転座や抗生物質耐性遺伝子の伝播のリスクがなく[229]、より正確な投与量設定が可能で、再現性の高い治療効果が得られます[225,230]。 |
| 製造工程では、特定の微生物株を培養し、その後、電離放射線、紫外線、高圧乾燥、pH調整などの方法を用いて不活性化します。健康増進効果のあるパラプロバイオティクス菌種には、ビフィドバクテリウム・ラクティスBb12、ビフィドバクテリウム・ロンガム、ラクトバチルス・ガセリOLL2716、サッカロミセス・セレビシエ、ラクトバチルス・ブレビスSBC8803、ラクトバチルス・デルブルエッキ亜種ブルガリカスOLL1073R-1などがあります。 |
| これらの菌株は、タンパク質、ペプチド、ペプチドグリカン、リポテイコ酸、多糖類(グルカンなど)、あるいはAT-リッチDNAなどの遺伝物質断片を介して、免疫調節作用[231]を発揮します。パラプロバイオティクス由来のタンパク質の中には、腸粘膜の再生を促進し、腸管バリアを修復するものもあります[230]。酵母細胞壁の成分であるβ-(1,3)-D-グルカン、β-(1,6)-D-グルカン、キチン、マンノプロテインなどは、消化を促進します[232]。 (訳者注:核酸の GC含量は生物により、また細胞の核と核以外由来によっても異なるが、GC含量が少ないも のを AT リッチ、GC 含量が多いものを GC リッチという。) |
| パラプロバイオティクスは、まだ発展途上の分野ではありますが、従来のプロバイオティクスが禁忌となっている集団への応用が期待されています。初期の研究では、炎症の抑制、感染症の減少、代謝調節の補助といった潜在的な効果が示唆されています。しかしながら、様々な慢性疾患における有効性を確立するには、より堅牢な臨床試験が必要です。 |
| 6.5. 腸内細菌叢とメタバイオティクス |
| メタバイオティクスは、プロバイオティクスの構造要素、その代謝物、あるいは宿主特異的な生理機能を最適化し、常在細菌叢の活性に関連する代謝、調節、および/または行動反応に影響を与える特定のシグナル伝達分子から構成される[233]。これらの化合物は、ケフィア、キムチ、ザワークラウト、テンペ、ヨーグルト、特定のピクルスなどの発酵食品や人体内に存在する[234]。メタバイオティクスは、生きたプロバイオティクスの副作用を軽減するためのバイオテクノロジーの進歩として注目を集めており、健康治療や機能性食品の開発に応用されている[235]。メタバイオティクスには、宿主に多くの利点をもたらす幅広い生理活性化合物が含まれている。メタバイオティクスは、酸化ストレスを軽減し、血圧を調節し、免疫調節作用をもたらし、抗炎症作用や抗癌作用を示す[235,236]。代謝産物の主要成分には、シグナル伝達分子、代謝後の死細胞または細胞断片、短鎖脂肪酸、多価不飽和脂肪酸、バクテリオシン、ポリアミン、表面分子、多糖類、ペプチドグリカン、タンパク質、ペプチドなどがある[237]。 |
| 腸内細菌叢に関する研究は、バイオモジュレーターが健康全般の維持に果たす役割を強調しています。バイオモジュレーターは、神経系、炎症反応、腫瘍学、消化管、内分泌系、尿路、呼吸器系、心血管系、免疫系など、様々なシステムに影響を与えます。最近の研究では、抗生物質の乱用によって引き起こされる耐性菌の抑制におけるバイオモジュレーターの可能性も強調されています。抗菌薬とプロバイオティクスを併用することで、薬剤投与量を減らすことで治癒が促進されます。この併用アプローチは、病原体の除去効果を高め、副作用を軽減します。このような相乗効果は、口腔カンジダ症、膣カンジダ症、歯周炎、ヘリコバクター・ピロリ感染症の治療に有効であることが証明されています[238]。 |
| アレルギー性疾患の予防におけるプロバイオティクス・バイオモジュレーターの効果を評価する臨床研究およびメタアナリシスでは、相反する結果が得られている[239]。プロバイオティクス株の多様性、治療期間、研究方法、評価対象となる主要評価項目および副次評価項目、対象となるアレルギー性表現型、患者特性(例:年齢、アトピー)といった要因のばらつきが、データの解釈を複雑にしている。 |
| 臨床的には、メタバイオティクスは肥満[240,241]、2型糖尿病、心血管疾患、神経変性疾患[237]などの慢性疾患の治療薬として研究されています。例えば、酪酸[242]は腸の炎症を軽減し、腸管バリアの完全性を高める効果が期待されており、プロピオン酸はインスリン感受性の改善と関連付けられています[243]。さらに、ラクトバチルス属およびビフィドバクテリウム属由来の生理活性代謝物は、消化管[244]および全身の健康に関連する免疫調節作用および抗酸化作用を示すことが示されています。 |
| こうした進歩にもかかわらず、メタバイオティクスの臨床応用は依然として限られています。課題としては、活性代謝物の同定の複雑さ、微生物代謝における個人差、そして有効性を検証するための対照試験の必要性などが挙げられます。しかしながら、メタバイオティクスは、慢性疾患の病因に関与する特定の経路を標的とするプレシジョンセラピューティクスとして大きな可能性を秘めています。 |
| 6.6. 腸内細菌叢とポストバイオティクス |
| ポストバイオティクスは、プロバイオティクスの有益な代謝副産物または分泌物質の複雑な混合物であり、無細胞培養上清中に存在します[245]。これらには、酵素、分泌タンパク質、短鎖脂肪酸、ビタミン、アミノ酸、ペプチド、有機酸などが含まれます[246]。「ポストバイオティクス」という用語は、「生命の終焉」を意味し、生きた微生物の代謝から得られる物質を指します。ポストバイオティクスは安定しており、輸送が容易で、包装を簡素化しながら長期保存が可能です。その有効成分は腸管に到達してもそのままの状態を保ち、そこで生理学的効果を発揮します[247]。ポストバイオティクスに関する研究では、炎症を調節し、消化管における病原体の付着を減少させ、肥満[222]、高血圧、冠動脈疾患、がん、酸化ストレス[248]などの症状に対処する能力が明らかにされています。さらに、ポストバイオティクスは強力な免疫調節作用と抗腫瘍作用を示します。その作用の具体的なメカニズムは未だ解明されていません。いくつかの実験的研究が行われています。現在、ポストバイオティクスは、乳製品、野菜、パン、肉、魚などの食品派生物に機能性成分として添加されることが多くなっています。 |
| さらに、ポストバイオティクスはプロバイオティクスの代謝副産物(短鎖脂肪酸など)を保存することが多く、代謝や免疫のメリットにさらに貢献します。 |
| 臨床的には、ポストバイオティクスは呼吸器系および消化器系の感染症の予防、アレルギーの抑制、慢性炎症性疾患の管理において研究されてきました。非生菌性であるため、乳児、高齢者、免疫不全患者など、プロバイオティクスでは安全性に懸念がある脆弱な集団に特に適しています。メタボリックシンドローム、肥満、神経炎症性疾患への応用の可能性を示唆する研究もありますが、より大規模で標準化された試験が必要です。 |
| これらの利点にもかかわらず、限界は依然として存在します。観察された効果をもたらす正確な生理活性成分は必ずしも明確に特定されておらず、反応には個人差が依然として存在します。さらに、これまでの研究のほとんどは短期的なものであり、長期的な疾患エンドポイントではなく、代替アウトカムに焦点を当てています。 |
| 6.7. 糞便微生物移植 |
| 糞弁微生物移植(FMT)は、健康なドナーから採取した処理済みの糞便を、腸内細菌叢の乱れに悩むレシピエントに移植し、健康な微生物バランスを再構築する治療法です。この治療法は、主に、乱れた微生物叢によって引き起こされる、または悪化する症状に対処します[249](図4)。 |
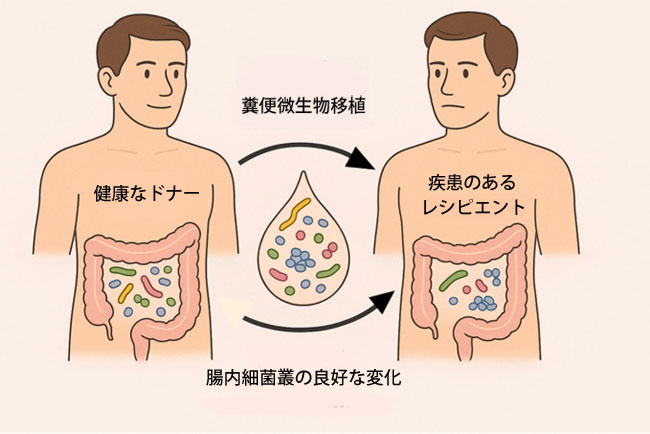 |
| 図4. 糞便微生物移植により腸内細菌叢が回復する |
| 糞便微生物移植は、特に抗菌薬耐性患者における再発性または難治性のクロストリディオイデス・ディフィシル感染症(rCDI)の治療におけるゴールドスタンダードとなっています。クロストリディオイデス・ディフィシル感染症治療以外にも、他の腸内細菌叢異常関連疾患への糞便微生物移植の実験的応用が検討されています[201,250]。 |
| 糞便微生物移植には、様々な投与方法を用いた様々なプロトコルが開発されている[251]。これらには、胃または小腸(十二指腸または空腸)を標的としたカプセルや経鼻腸チューブなどの上部消化管経路、浣腸などの下部消化管経路、あるいはフレキシブルS状結腸鏡検査や大腸内視鏡検査などの処置が含まれる。 |
| ドナースクリーニングは、糞便微生物移植の安全性を確保する上で重要なステップです。このプロセスでは、病原体伝播リスクを最小限に抑えることを目的とした広範な臨床検査に加え、包括的な臨床歴の調査が行われます[252]。経膣分娩、母乳育児、地中海式ダイエットの遵守など、健康なマイクロバイオームに関連するドナーの特徴も、慢性非感染性疾患に対する糞便微生物移植の有効性を高めるために提案されています[253]。 |
| 現在、糞便微生物移植の主な臨床応用はクロストリディオイデス・ディフィシル感染症の治療であり[254,255]、その有効性は最大90%に達する可能性があります。この治療法は、患者の腸内細菌叢を迅速に回復させるだけでなく、クロストリジウム・ディフィシルの発芽および栄養成長を阻害します[256,257]。長年にわたり、多くの研究によって糞便微生物移植の可能性は拡大し、他の慢性疾患の管理における有効性が実証されています。これらの知見は、感染症、代謝、炎症性疾患における腸内細菌叢の複雑な役割を浮き彫りにしており、糞便微生物移植は免疫代謝メカニズムに関わる経路を通じて細菌叢と宿主の相互作用に影響を与える可能性を示しています[258]。 |
| 糞便微生物移植の有効性に関する注目すべき知見は、糞便微生物移植懸濁液を0.2mmまで徐々に細かいフィルターに通すことで作製した滅菌便濾液を用いたパイロットスタディから得られました。この濾液をクロストリディオイデス・ディフィシル感染症患者5名に投与したところ、従来の糞便微生物移植と同等の結果が得られました[259]。この知見は、糞便微生物移植の成功は生菌だけでなく、濾液中に存在する可溶性因子、すなわちウイルス、真菌、代謝物、マイクロRNA(miRNA)、免疫シグナル伝達分子にも依存している可能性を示唆しています。 |
| バクテリオファージ(細菌や古細菌に感染するウイルス)に関する研究により、様々な疾患において糞便微生物移植後のウイロームの変化が明らかになっている[260]。特に、レシピエントの腸管ウイロームはドナーのウイロームに類似するように変化し、この変化は1年以上持続することが示された[261]。 |
| ニッチ競争の理論は、クロストリディオイデス・ディフィシル感染症治療における糞便微生物移植の有効性にも影響を与えている。糞便微生物移植によって再導入された腸内常在菌は、必須栄養源やコハク酸、インターロイキン、プロリンなどの特定のアミノ酸をめぐってC. ディフィシルと競合する。さらに、糞便微生物移植後の細菌の中にはこれらの栄養素を積極的に異化して、C. ディフィシルによる利用を妨げるものもある。糞便微生物移植の成功は短鎖脂肪酸レベルの回復とも関連付けられており、特に吉草酸はC. ディフィシルの増殖に対して用量依存的な阻害効果を示した[262]。さらに、糞便微生物移植は胆汁代謝細菌を回復させ、C. ディフィシルの発芽の引き金となるタウロコール酸の分解などのプロセスや、栄養成長を阻害するデオキシコール酸などの二次胆汁酸の産生を増加させることで、C. ディフィシルの病原性を抑制するのに役立つ。 |
| クロストリディオイデス・ディフィシル感染症の文脈以外では、短鎖脂肪酸、胆汁酸、その他の微生物代謝物が、潰瘍性大腸炎などの疾患における糞便微生物移植の成功に重要であることが証明されています[263]。食事療法も治療効果をさらに高めており、治療中に抗炎症食を遵守することで、標準的な医療プロトコルと比較して寛解率が大幅に向上することが研究で示されています[264]。 |
| 糞便微生物移植の有効性は、カテリシジンなどのドナー細菌からの抗菌化合物の移行や、宿主マイクロRNAの変化の誘導など、他の要因にも左右される可能性があります。これらのマイクロRNAは、炎症性遺伝子の発現に影響を与えたり、オートファジーの改善や腸管バリア機能不全の改善によって腸管透過性を低下させたりする可能性があります。腸管バリアの回復は、非アルコール性脂肪性肝疾患[265]やエイズ感染症[266]など、様々な症例で報告されています。さらに、クロストリディオイデス・ディフィシル感染症、多剤耐性菌、重症アルコール性肝炎の場合、糞便微生物移植は有害な腸内細菌の全身循環への移行を制限することで、侵襲性感染症や菌血症の減少と関連付けられています[267]。 |
| 最後に、糞便微生物移植は腸内細菌叢と免疫システムの間の動的かつ相互的な関係を強調し[83,268]、多様な健康状態にわたるその広範な治療可能性を強調しています。 |
| 糞便微生物移植を受けたクロストリディオイデス・ディフィシル感染症患者では、分泌型免疫グロブリンAの標的化が健常ドナーのプロファイルとより一致していた[269,270]。さらに、自然免疫系および獲得免疫系における免疫老化マーカーは逆転し、血清N-グリカン構造の複雑さ(免疫機能の変化に関連する可能性がある)が減少した。 |
| 糞便微生物移植の免疫学的効果はクロストリディオイデス・ディフィシル感染症以外の状況でも評価されています。例えば、大腸炎症はIL-10を介して調節されます[270]、非特異的炎症性腸疾患は制御性Tリンパ球細胞を介して調節されます[144]、細菌性敗血症はインターフェロン調節因子3の変異を介して調節されます[271]。 |
| 動物実験では、糞便微生物移植のドナーとしてプレバイオティクスを摂取することで腸内細菌叢を再構築することで、メタボリックシンドロームを改善できることが実証されています。メタボリックシンドロームの青年における糞便微生物移植の有効性を評価し、インスリン感受性とグルコース代謝の向上が示された臨床試験では、インスリン感受性とグルコース代謝が改善したことが明らかになりました[272]。さらに、洗浄微生物移植(WMT)[273]と呼ばれる新しいアプローチが、機能性腸疾患患者237名(メタボリックシンドローム患者42名、非メタボリックシンドローム患者195名)のコホートで実施されました。このアプローチは、メタボリックシンドローム患者の転帰を有意に改善しました[274]。 |
| 1型糖尿病における腸内細菌叢と糞便微生物移植の役割を調査した複数の研究のエビデンスによると、1型糖尿病の進行は停止したか、または有意に遅くなることが示されている[275,276]。小腸のプレボテラ菌のレベルも残存β細胞機能と逆相関しているようだった[275]。2型糖尿病を有する肥満患者61名を対象とした12週間のランダム化試験では、糞便微生物移植と生活習慣介入(LSI)、糞便微生物移植単独、および生活習慣介入を伴う偽手術の3つのグループが調査された。最初のマイルストーンは、糞便微生物移植 + 生活習慣介入群で100%、糞便微生物移植のみのグループで88.2%、生活習慣介入のみのグループで22%で達成された。さらに、糞便微生物移植はすべての症例で酪酸産生細菌を増加させたが、糞便微生物移植 + 生活習慣介入の組み合わせは、糞便微生物移植単独と比較してビフィズス菌と乳酸菌の増殖も刺激した。脂質プロファイルと肝機能の改善も観察された。糞便微生物移植の反復実施は、2型糖尿病患者の代謝転帰に対する持続的かつ強化された影響を実証した[277]。糞便微生物移植を受けた17名の2型糖尿病患者を対象とした別の研究では、11名の参加者で有意な改善が報告された。グリコヘモグロビン、空腹時血糖値、食後血糖値、尿酸値の顕著な減少と、食後Cペプチド(インスリン分泌の指標)の上昇が認められた。インスリン抵抗性と関連する嫌気性細菌の存在量が多い参加者は、より強力な臨床反応を示した[278]。さらに、糞便微生物移植または洗浄微生物移植は、腸内細菌叢の調節を介して遠位対称性多発神経炎[279]と血糖変動[280]を改善し、糖尿病患者を助けた。 |
| 経膣分娩された新生児では、母親の腸内細菌叢が新生児に効果的に定着する[77]のに対し、帝王切開で生まれた赤ちゃん[54]は、腸内細菌叢の構成が異なっている[281]。これらの違いは、帝王切開で生まれた新生児、特に母乳ではなく人工乳で育った赤ちゃんのアレルギー疾患に対する感受性の高さに寄与している[282]。帝王切開で生まれた新生児に母親の糞便移植を行ったある研究では、その腸内細菌叢が経膣分娩児のものと非常によく似ていることがわかった[283]。これは、糞便微生物移植が乳児のアレルギーを予防できる可能性があり、小児アレルギー疾患の治療に有望な治療戦略となることを示唆している[284]。 |
| 糞便微生物移植の有効性を確認する研究と臨床実践からの肯定的な結果にもかかわらず、重要な疑問は依然として解明されていません。糞便微生物移植に対する疾患特異的な反応、理想的な投与レジメン、治療頻度、再現性、持続的な有効性といった要因については、さらなる検討が必要です。入手可能なエビデンスのほとんどはサンプル数が少ない研究から得られたものであり、より大規模で質の高い試験が必要となります。糞便微生物移植が日常臨床ケアに広く導入されるには、作用機序、有効な治療濃度、潜在的な副作用、費用対効果、そして長期的な影響をより深く理解するための包括的な調査が不可欠です。 |
| 本章で検討した戦略(様々なバイオモジュレーターから糞便微生物移植まで)は、腸内細菌叢調節による治療領域の拡大を示しています。これらの戦略は、症状中心のアプローチから腸内生態系のバランス回復を目的とした介入へのパラダイムシフトを反映しています。 |
| バイオモジュレーターに関しては、プレバイオティクス、プロバイオティクス、シンバイオティクスが、食事やサプリメントが微生物群集をどのように形成し、レジリエンス(回復力)、免疫寛容性、そして代謝の健康を促進するかを明らかにしています。パラバイオティクスとポストバイオティクスは、安全で標準化された代替手段を提供し、微生物叢由来の恩恵を脆弱な集団にも広げます。メタバイオティクスは、特定の生理活性分子に焦点を当てることで、微生物叢科学を精密薬理学に近づけています。 |
| 糞便微生物移植に関する限り、この技術は最も包括的なアプローチであり、胃腸疾患と腸管外疾患の両方に対して変革の可能性を秘めた微生物生態系全体を再構築します。 |
| しかし、これらの戦略すべてに共通する課題として、臨床アウトカムの不均一性、標準化の欠如、そして長期にわたる高品質な試験の必要性が挙げられます。さらに、その有効性は食事、ライフスタイル、宿主の遺伝子、そしてベースラインの微生物叢構成に左右されるため、個別化アプローチが求められます。 |
| しかし、これらの戦略すべてに共通する課題として、臨床アウトカムの不均一性、標準化の欠如、そして長期にわたる高品質な試験の必要性が挙げられます。さらに、その有効性は食事、ライフスタイル、宿主の遺伝子、そしてベースラインの微生物叢構成に左右されるため、個別化アプローチが求められます。 |
| 最終的には、健康な腸内細菌叢の維持は、治療目標としてだけでなく、疾患予防の基盤としても重要になります。腸内細菌叢に基づく介入をより広範な健康戦略に統合することで、慢性非感染性疾患の負担を軽減し、精密医療と予防医療の新たな道を切り開くことができる可能性があります。 |
| 7. 腸内細菌叢と栄養 |
| 歴史的に、結腸は主に体液と消化されない物質の貯蔵器官と考えられてきました[285]。しかし、現在では、結腸は体の他のどの部分よりも多くの生理活性細胞を含む、完全に機能する代謝器官としての役割が強調されています[286]。1970年代の最初の画期的な研究により、便塊は未消化物ではなく主に細菌で構成されていることが明らかになりました。これに続く重要な発見は、結腸上皮細胞の主なエネルギー源がグルコースではなく短鎖脂肪酸であるという認識であり、その代謝における役割の理解に大きな転換をもたらしました[287]。粘膜上皮の特徴的な特性は、血液循環に依存せずに、食事摂取や消化プロセスから栄養素を直接抽出し、利用できることにあります。しかし、乳び(訳者注:乳び(Chyle)は、食事の消化中、特に小腸で形成される脂肪とリンパ液が混ざった乳白色の液体です)が結腸に到達するまでに、タンパク質と炭水化物の90%以上が既に吸収されており、食物繊維、デンプン、そして「難消化性」タンパク質といった未消化成分が残されています。結腸自体はこれらの残留物を分解できる酵素を生成しません。ここで腸内細菌叢が重要となり、宿主-微生物共生の重要な例として機能します。腸内細菌叢はこれらの消化されない残留物を発酵させ、短鎖脂肪酸や水素、メタンなどのガスを産生します。これらは主に呼吸によって吸収または排泄されます[288]。短鎖脂肪酸は結腸の健康に大きく貢献します。例えば、酪酸という特定の短鎖脂肪酸が腫瘍形成を抑制できることは、多くの実験的証拠によって実証されています[289]。さらに、食事と腸内細菌叢の相互作用は、ビタミンを含む様々な有益な効果を持つ代謝物の合成につながります[290]。それにもかかわらず、腸内の微生物代謝によって粘膜に有害な化合物が生成される可能性もあることに注意することが重要です[291]。 |
| 動物モデルおよびヒト研究から得られた新たなエビデンスは、腸内細菌叢がエネルギー代謝の調節と肥満傾向への影響において重要な役割を果たしていることを強調している。痩せ型と肥満型の人の間での大腸内細菌叢の構成の違い、特にバクテロイデス門およびフィルミクテス門の相対的存在量の変化は、宿主が食事からエネルギーを摂取する能力の決定要因であることが明らかにされている[292] [293]。大腸の代謝機能は、粘膜の健康維持における役割に加え、重度の腸管吸収不良症例において重要な生存メカニズムとして機能する可能性がある。このような状況では、腸内細菌叢を介した発酵によって、吸収されなかった食事性残留物から最大1000キロカロリーのエネルギーを回収することができる。さらに、この代謝活動は、葉酸、ビオチン、ビタミンKなどの必須ビタミンを合成することで、栄養不足の状態でも生存をサポートします[294,295]。 |
| 食生活パターンが結腸疾患に及ぼす保護効果に関する初期の研究の一つでは、自家粉砕穀物由来の食物繊維を豊富に含む「伝統的な」食事を摂取するアフリカ人において、非感染性結腸疾患が認められないことが明らかになった[296]。この研究では、食物繊維の摂取量増加によって腸管通過が促進され、毒素や発がん物質への曝露が減少するとともに便の量が増加し、便秘が軽減され、憩室症などの疾患リスクが低下すると提唱されている[297]。 |
| 食事は複数のメカニズムを介して慢性非感染性疾患のリスクに影響を与える。まず、食品加工や環境汚染物質に由来する非吸収性の炎症誘発性分子を体内に取り込む可能性がある。さらに、特定の栄養素は健康と細胞代謝に重要である。西洋型の食事は、常在細菌に対する異常な粘膜免疫応答を促進し、腸管バリアの完全性を破壊し、それによって腸内で炎症を誘発することに関与していることが示唆されている[298]。対照的に、地中海式ダイエットの遵守は、腸管粘膜機能の促進、腸管バリア機能の強化、免疫機能のサポートを通じて、腸管生理機能に有益な結果をもたらすことが実証されている。食事介入による腸管の健康の回復は、しばしば長期的な食事遵守を改善する正のフィードバックループを生み出す[298]。 |
| 体内の組織の中で腸粘膜は独特な特徴を持ち、食事中の栄養素を直接利用して構造的完全性と機能性を維持することができます [299]。さらに栄養素は、感染症や炎症を防ぐ強力な免疫システムを維持するために不可欠な代謝プロセスを調節します。これを裏付ける証拠は、地中海式ダイエット(ポリフェノールの含有量が多いことで特徴付けられる)[300]や伝統的な日本食[301]などの食物繊維と抗酸化物質が豊富な食事を摂っている人々の健康と長寿に見ることができます。これらの食事モデルは、腸内微生物叢の組成に大きな影響を与えることで、全体的な健康を維持するための最も実践的な戦略の1つを例示しています [302]。健康的な食事は、慢性非感染性疾患の減少だけでなく、多様でバランスの取れた腸内微生物叢の集団を促進することで老化の減速にも関連しています [303]。このような食事では、通常、超加工食品、精製炭水化物、飽和脂肪が豊富な動物性食品を最小限に抑え、豆類、全粒穀物、ナッツ、果物、野菜、ハーブなどの植物性食品(生物学的に活性な植物化学物質が豊富な供給源)を重視します[304]。 |
| 7.1. 微生物叢とファイトケミカル |
| ファイトケミカルは、植物によって合成される多様な生理活性非栄養化合物群であり、植物の色素、風味、芳香特性に関与しています。現在までに、ポリフェノール、カロテノイド、イソチオシアネート、アルカロイド、フィトステロール、サポニンなど、10万種類以上のファイトケミカルが同定されています[305]。これらの化合物のヒトの食事における生物学的利用能は、分子サイズ、親油性、化学的安定性、食品マトリックス内での相互作用、腸内細菌叢による代謝変換など、いくつかの要因によって異なります[306]。ファイトケミカル、特にポリフェノール[307]は、消化器系で吸収されにくいため、大腸に無傷で到達します。そこで、ファイトケミカルは腸内細菌叢と相互作用し、代謝を受けて新たな生理活性微生物代謝物を形成します[308]。食物中の植物化学物質とこれらの代謝物は、腸管組織に良い影響を与えることで腸の健康維持に有益な役割を果たします[309]。微生物代謝物は全身循環に入ると、宿主-微生物叢相互作用を媒介するシグナル伝達分子として働き、様々な組織や臓器の免疫機能、代謝機能、神経機能に影響を与えます[310]。局所粘膜免疫系と腸内微生物叢のバランスは、病原体を制御し、有益な微生物を活性化し、細菌の過剰増殖を防ぐ上で非常に重要です。腸内の持続的な炎症は、局所および全身の活動を破壊することが知られています[311]。植物化学物質を含む食品やサプリメントは、抗炎症作用、抗酸化作用、免疫調節作用を有するため、炎症の抑制に不可欠です。これらの化合物は、体の自然防御力を高め、間接的に腸内微生物叢の構成に影響を与えることで効果を発揮します。 |
| 7.2. 微生物叢の代謝物 |
| 細菌の代謝によって産生される食物成分のうち、短鎖脂肪酸[312]とアミノ酸(AA)[313]は宿主の生理機能の重要な調節因子として機能している。 |
| 短鎖脂肪酸受容体であるGPR43(訳者注:GPR43は、腸内細菌が産生する短鎖脂肪酸(酢酸、プロピオン酸など)をリガンドとするGタンパク質共役型受容体です。主に脂肪組織や免疫細胞に発現し、脂肪蓄積の抑制、エネルギー代謝の制御、炎症の調節、免疫機能の恒常性維持(制御性T細胞分化誘導など)において重要な役割を果たす)は、細菌の代謝活性と宿主のエネルギー恒常性を結び付けることが示されています[314]。酢酸、プロピオン酸、酪酸などの短鎖脂肪酸(嫌気性腸内細菌による食物繊維の発酵中に、H2やCO2などのガスとともに生成されます)[315]は、多くの健康効果を示しています。これには、免疫バランスの維持、代謝機能のサポート、血糖値の安定化、腸管バリアの完全性の強化、食欲の調節などが含まれます[316]。短鎖脂肪酸は慢性非感染性疾患の予防と管理にもプラスの影響を与え[186]、実際、疾患に関連する腸内細菌叢の乱れにより短鎖脂肪酸レベルが低下することが知られています[317]。 |
| 上で報告されているように、アミノ酸は消化吸収中の腸内細菌叢の成長と活性を維持する上で重要な役割を果たしています。細菌叢は、消化管内のアミノ酸の総量(アミノ酸プール)と構造特性(アミノ酸プロファイル)の両方の調節に寄与しています[318]。さらに、腸内細菌叢とアミノ酸を含む食事性窒素成分との相互作用は、宿主の健康と栄養にとって重要です。これらの相互作用は、アミノ酸の食事性補給の有効性に影響を及ぼします[319]。腸内細菌は、グルタチオン代謝を変化させるなど、アミノ酸代謝に影響を与えます[320]。最近の研究では、タンパク質とアミノ酸の発酵に関与する特定の細菌種がヒトの大腸で活動していることが特定されています。たとえば、クロストリジウム属はプロリンとリジンを代謝し、ペプトストレプトコッカス属はトリプトファンとグルタミン酸を処理します。バクテロイデス属、フソバクテリウム属、ベイヨネラ属などの他の属も、大腸におけるアミノ酸の分解において重要な役割を果たしている[321]。高度な分子生物学的研究により、腸内細菌叢とアミノ酸代謝の相互作用が、宿主の栄養状態や全体的な健康状態に有益な影響、あるいは有害な影響を与えることが明らかになっている[322]。 |
| 個人の腸内細菌叢の構成は、食物由来の植物化学物質の代謝と薬物動態に大きな影響を与えます[304]。したがって、機能性食品から有益な微生物代謝産物を産生する能力は、腸内に存在する特定の微生物群集に依存します[306]。腸管透過性、年齢、病状、薬物使用(例:抗生物質)、遺伝、環境要因など、いくつかの要因がこのプロセスにさらに影響を与える可能性があります。 |
| 微生物代謝物は、慢性非感染性疾患の発症を予防または遅らせることができる新しい化合物の発見が期待される、急速に進歩している研究分野です |
| 8. 腸内細菌叢と外因性物質 |
| ヒトは、生物系にとって異物である外因性物質(ヒトの活動によって環境中に放出される物質)に頻繁に曝露されています。これには、薬剤(抗生物質を含む)、農薬、重金属、マイクロプラスチックおよびナノプラスチックなどが含まれます(表4)。 |
表4. 異物による腸内細菌叢異常。 略語:PCB(ポリ塩化ビフェニル)、CNCD(慢性非感染性疾患)、SCFA(短鎖脂肪酸)、Aas(アミノ酸)、TPA(テレフタル酸、ポリエチレンテレフタレート(PET)モノマー)、BPA(ビスフェノールA、ポリカーボネート(PC)モノマー)。 |
 |
 |
| 薬物を除く環境汚染物質は、主に食物を通じてヒトに侵入する。生体はこれらの汚染物質を吸収する速度が、排泄または代謝する速度よりも速い傾向がある[323]。宿主の遺伝的要因は、環境要因と比較して微生物叢の構成に最小限(2%未満)しか影響を及ぼさない[324]ため、環境要因が腸内細菌叢の異常を引き起こす上で重要な役割を果たしていることがわかる。異物による腸内細菌叢の変化は免疫系の発達に影響を与え、それによって炎症性腸疾患(IBD)などの慢性疾患のリスクを高める可能性がある[325]。腸内細菌叢の主要な機能の1つは、異物化合物および食事性分子を生理活性代謝物に変換することである[326]。これらの化合物への曝露は、微生物とヒトの代謝物との相互作用に影響を与え、多くの場合、微生物の生理機能および多様性の変化につながる[327]。 |
| 8.1. 抗生物質による腸内細菌叢の乱れ |
| 抗生物質が腸内細菌叢に及ぼす影響に関する研究は、ペニシリンの発見直後から始まりました[328]。分子生物学的手法、特に培養に依存せず16S rRNA遺伝子解析に基づく手法の進歩は、腸内細菌叢に関する理解を大きく深めました。16S rRNA配列には、保存領域(すべての細菌に共通)、半保存領域(同じ門の細菌内で類似)、そして細菌種の同定に用いられる可変領域が含まれています[329]。これらの領域の16S rDNA配列決定により、抗生物質誘発性ディスバイオシスが明らかになり、細菌叢構成の質的および量的変化が明らかになりました[330]。ヒトマイクロバイオームプロジェクト[331]やヒト腸管メタゲノミクス[332]といった主要プロジェクトは、微生物界への理解を深める膨大なデータセットを生み出してきましたが、これらのデータの多くは依然として解釈が複雑です。メタゲノム解析によるアプローチは、腸内脂質プロファイルと血漿メタボロームの変化と腸内細菌叢の異常との関連を実証しています[333]。抗生物質は腸内細菌叢に大きな影響を与え、細菌多様性の急激な減少と相対的な存在量の変化を引き起こします。 |
| 大腸のpHが高いほど、微生物の多様性と密度が豊かである[334]。健康な人では、とフィルミクテス門とバクテロイデス門が優勢(90%以上を占める)で、ウェルコミクロビウムと放線菌がそれに続く[335]。健康な腸内細菌叢は、ビタミン産生、栄養代謝、免疫調節、病原体の定着を防ぐことによる感染防御など、重要な役割を果たしている[336]。異なる国の集団間の比較研究では、食事、地理、幼少期の曝露、遺伝の違いに関連して微生物叢の構成にばらつきがあることが明らかになった[337]。年齢、食事、抗生物質、プロバイオティクス、プレバイオティクスなどの要因はすべて、生涯を通じて動的かつ進化する微生物叢の形成に寄与している[335]。 |
| しかし、抗生物質は、ディスバイオシスを引き起こすことでこのバランスを崩す可能性があり、こうした乱れが免疫機能の変化や感染抵抗力の低下につながるという証拠が増えています[338]。抗生物質の使用に起因するディスバイオシスは、神経変性疾患[339]、神経障害[340]、肥満および糖尿病[341]、炎症性腸疾患[342]、クローン病[343]、セリアック病[344]、アレルギー、若年性特発性関節炎、喘息などの自己免疫疾患[345]など、多くの健康問題に関連しています。これらの影響は、生後2年以内に抗生物質を服用した場合に特に顕著であり、累積的な影響が生じる可能性があります[346]。微生物叢にはある程度の回復力(抗生物質治療後に元の状態に近い構成に戻る能力)が見られますが[347]、この回復プロセスには数か月から数年かかる場合があり、まだ完全には解明されていません[348]。 |
| 8.2. 農薬による腸内細菌叢の乱れ |
| 農業における農薬の広範な使用には長い歴史があるが、その使用量は工業化農業の進展とともに急増した。国連食糧農業機関(FAO)のデータによると、年間400万トン以上の農薬が使用されており、中国、米国、ブラジルが最大の消費国となっている。数十年にわたる集中的な農薬使用により、土壌、堆積物、水質サンプルに残留物が残っている。ジクロロジフェニルトリクロロエタン(DDT)のような内分泌かく乱性農薬は、その有害性の証拠が蓄積された後、ほとんどの国で禁止されている。しかし、すべての国がこれらの有害物質を完全に廃止したわけではない[349]。農薬曝露に関連する職業上の危険性については多くの研究が行われてきたが、残留農薬で汚染された農産物や水の日常的な摂取による健康リスクに注目が集まるようになったのはごく最近のことである。様々な研究から、農薬は特に腸内細菌叢のバランスを崩すことで消費者の健康を危険にさらす可能性があることが示されています[350]。 |
| 最近の研究では、腸内細菌叢が農薬などの環境化学物質への曝露のバイオマーカーとして機能する可能性が示唆されている[351]。特に、2,4-ジクロロフェノキシ酢酸(2,4-D)やグリホサートなどの一般的な除草剤は、遺伝子組み換え作物によって耐性が発達したためにしばしば併用されており、重大な影響を及ぼす[352]。研究によると、グリホサートはヒトの腸内細菌叢内の細菌種の54%に影響を及ぼす可能性があると示されている[353]。ポリ塩化ビフェニル(PCB)は1977年にその毒性のために禁止されたにもかかわらず、環境中に広く残留し、引き続きリスクをもたらしている。主に経口摂取によるポリ塩化ビフェニルへのヒトの曝露は、胃腸障害、腸内細菌叢異常、および自閉症スペクトラム障害などの神経発達障害に対する感受性の高まりに関連している[354]。妊娠中の曝露は胎児の腸内細菌叢を長年にわたり変化させ、バチルス属、プロピオニバクテリア属、プロピオニバクテリア科などの特定の細菌群を増加させることが示されています[355]。 |
| 出生時に腸内細菌叢が定着しているにもかかわらず、マウスを用いた多くの研究では、母体の腸内細菌叢が胎盤通過によって胎児の神経細胞の発達に影響を与える可能性があることが示唆されている[356]。さらに、母乳育児は最も初期の腸内細菌叢に影響を与え、母乳は農薬残留物に移行する可能性がある[357]。最近の研究では、DDTの代謝物やDDT自体が、推奨される1日摂取量の上限値よりも高い濃度で存在することが明らかになっている[358]。 |
| 8.3. 重金属による腸内細菌叢の乱れ |
| ヒ素(As)、カドミウム(Cd)、鉛(Pb)、水銀(Hg)などの重金属(HM)による汚染は、腸内細菌叢のバランスを崩すことが知られており、広範囲かつ永続的な脅威となっている[359]。ヒトへの曝露は、環境汚染、汚染食品、歯科処置、産業活動または農業活動を通じて起こる[360]。重金属によって引き起こされる腸内細菌叢の乱れは、生理機能および代謝機能を損ない、炎症を誘発し、慢性非感染性疾患(慢性閉塞性肺疾患)の一因となる可能性がある[361]。重金属は強力な神経毒として作用し、特に妊娠初期などの重要な時期に有害である[362]。フタル酸エステル、ビスフェノールA、粒子状物質、重金属などの外因性物質は、腸内細菌叢-腸管-脳系に干渉することが知られており[323]、精神的および神経学的健康に影響を及ぼす可能性がある[363]。調査結果は時折変化するものの、重金属への曝露が腸内細菌叢の多様性と構造を変化させることを研究では一貫して示している[364]。さらに、重金属などの環境汚染物質への曝露は腸管上皮バリアを損傷し、免疫と微生物のバランスを崩す[365]一方で、代謝活動を阻害し、炎症反応と細胞損傷を引き起こす[366]。動物実験では、重金属が腸内細菌の組成と機能を変化させることで毒性効果を発揮することが実証されている。これらの変化は代謝物に影響を及ぼし、病理学的状態につながる[367]。重金属に関連する腸内細菌叢の乱れは腸の内壁を損傷し、酸化ストレスと炎症を高めるとともに、慢性非感染性疾患に寄与する細胞毒性、遺伝毒性、発がん性効果を引き起こす可能性がある[367]。最近の研究では、腸内細菌と宿主シグナル伝達系が微生物代謝物を介して免疫を調節し、腸管バリア防御を強化する能力が強調されている[368]。腸内細菌叢は、重金属の毒性を軽減し、恒常性を維持する上で重要な役割を果たしている[369]。したがって、腸内バイオモジュレーターの利用は、異物によって引き起こされる腸管バリア機能障害の治療に有望な可能性を提供している[370]。特に、高重金属レベル(Cdを除く)への曝露は、病原体として知られるコリオバクテリア科の炎症性細菌属であるコリンセラの増加と関連している[371]。この属は、腸内でのコレステロール吸収を変化させ、肝臓でのグリコーゲン生成を減少させ、トリグリセリド合成を増加させることで、代謝経路に影響を及ぼす[372]。食物繊維の摂取は血中の重金属濃度を低下させることが示されており[373]、食物繊維の低摂取はコリンセラの増加と相関している[374]。さらに、コリンセラは腸管細胞におけるタイトジャンクションタンパク質の発現を減少させることで腸漏れに寄与し、代謝性エンドトキセミアの特徴である[375]。 |
| コリンセラ、プロテオバクテリア、腸内細菌科など、炎症に関連する特定の病原細菌の蔓延率は、ヒ素曝露下で増加することが観察されています。一方で、プロバイオティクスとみなされるビフィドバクテリウム属細菌の減少も報告されています。注目すべきことに、ビフィドバクテリウム属細菌群へのこの悪影響は、同時の亜鉛曝露によって回復する可能性があります[369]。関連研究では、新生児の尿中ヒ素濃度は、フィルミクテス属細菌と正相関し、バクテロイデス属細菌と逆相関することが示されています。これら2つの主要な腸内細菌門は、肥満やがんなどの疾患とも密接に関連しています[376]。 |
| 鉛への曝露も同様に悪影響を及ぼし、善玉菌のビフィドバクテリウム・ビフィダムとロンガム、真菌のペニシリウム属の減少を引き起こします。同時に、ビロフィラ、コリンセラ、プロテオバクテリア、バークホルデリアレスなどの病原性菌群、およびマラセチア・レストリクタやグロボーサなどの病原性真菌の増殖を促進します。マラセチアの一部の種は、脂漏性皮膚炎、白癬菌、毛包炎などの症状の一因となることが知られており、アトピー性皮膚炎を悪化させる可能性があります [377]。また、鉛は腸管バリアの完全性を損ない、胆汁酸や短鎖脂肪酸などの微生物代謝物が肝内循環に入りやすくし、その結果、動物とヒトの両方で全身障害を引き起こす可能性があります [378]。 |
| 水銀への曝露、特に米と比較して魚などの食物源を介した曝露は、3つの特定の細菌分類群、すなわち放線菌、デスルフォビブリオ、メタン生成菌の増加と関連付けられています。広範囲にわたる水質汚染のため、魚の摂取は依然としてヒトにおける水銀曝露の主な経路となっています[379]。これらの細菌のうち、デスルフォビブリオは腸管関連疾患だけでなく、パーキンソン病などの神経変性疾患にも関与する病原性細菌として機能しています[380]。一方、メタン生成菌は、脳および筋肉の膿瘍形成、腸内細菌叢の乱れ、代謝異常、大腸がんとの関連が指摘されています[381]。 |
| カドミウムは腸内細菌叢に顕著な悪影響を及ぼし、構造破壊、透過性亢進、胆汁酸、短鎖脂肪酸、アミノ酸の生合成阻害などを引き起こす[382]。他の毒素と結合すると、カドミウムは腸内細菌叢の不均衡を悪化させ、複数の臓器系に機能障害を引き起こす[383]。同様の影響はニッケルについても報告されている[384]。 |
| 重金属への曝露が腸内細菌叢と健康全般に及ぼすこれらの有害な影響を打ち消すために、いくつかの食事介入が提案されている。これには、食物繊維(特に全粒穀物由来のペクチン)、抗酸化物質を豊富に含む食品、腸内バイオモジュレーターの摂取増加が含まれる。動物由来の脂肪とタンパク質の適度な摂取も推奨されている[385]。さらに、必須栄養素、ビタミン、高品質タンパク質、生理活性ペプチド、抗酸化物質を豊富に含む植物化学物質を豊富に含む食事は、重金属誘発性の毒性と腸内細菌叢の異常を軽減する効果的な戦略となる可能性がある[386]。 |
| 8.4. マイクロプラスチックおよびナノプラスチックによる腸内細菌叢の乱れ |
| プラスチックは、化粧品、台所用品、食品包装などの消費財から、医療機器や建設などの先端分野に至るまで、その汎用性と多様な用途により、現代社会において不可欠な役割を果たしています。使い捨てプラスチックの段階的廃止や、リサイクル可能またはプラスチックフリーの代替品の推進に向けた世界的な取り組みが高まっているにもかかわらず、プラスチック廃棄物は依然として環境の持続可能性に対する重大な脅威となっています。土壌および海洋生態系におけるプラスチックの蓄積はかつてないレベルに達しており、一部の専門家は現在の時代を「プラスチセン(プラスチシン)」と呼んでいます[387]。予測によると、2050年までにさらに330億トンのプラスチックが環境に放出される可能性があります[388]。 |
| 自然生態系において、プラスチックは物理的、化学的、生物学的メカニズム、あるいはそれらの組み合わせによって生分解される[389]。これらの分解プロセスによって生成される粒子は、マクロプラスチック(> 25 mm)、メソプラスチック(5~25 mm)、マイクロプラスチック(< 5 mm)、ナノプラスチック(< 1 μm または < 100 nm)の4つのサイズに分類される[390]。マイクロプラスチックとナノプラスチックの区別は依然として議論の余地があるが、これらはしばしば総称してマイクロプラスチックおよびナノプラスチック(MNP)と呼ばれる。プラスチックとナノプラスチックは、金属や残留性有機汚染物質を吸収することができる[391]。さらに、疎水性、耐久性、浮力を有するため、ナノプラスチックは様々な病原体の潜在的なキャリアとなる可能性がある[392]。環境中のナノプラスチックに関する重大な懸念は、食物連鎖に入り込み、最終的には食生活に影響を与え、食品の安全性と人の健康の両方にリスクをもたらすことである。近年の研究では、プラスチック、環境微生物、マイクロバイオームとの相互作用が検討されているが、ナノプラスチックが腸内マイクロバイオームとどのように相互作用するか、あるいはこれらの相互作用がヒトの生理機能や健康にどのような影響を与えるかについては、限られた研究しか行われていない[393]。ヒトのナノプラスチックへの曝露は、主に経口摂取によって起こり、次いで吸入と経皮吸収が続く。 |
| ナノプラスチックは体積に比べて表面積が大きいため、有機物の吸着が促進され、「プラスチスフィア」と総称される微生物種の新しい生息地が形成されます [389]。このプラスチスフィア内の多くの微生物は、ナノプラスチックを消費して環境に優しい炭素化合物に変換できます [399]。環境中のマイクロバイオームの他に、腸内細菌叢も ナノプラスチックを分解する役割を果たしています [400]。昆虫の腸内細菌が ナノプラスチックを分解できることについてはかなりの証拠がありますが、哺乳類におけるこれらのメカニズムについてはほとんどわかっていません。人間の腸内環境のシミュレーションでは、人間の糞便微生物叢によるマイクロプラスチックの生体内変換をサポートする可能性のあるバイオフィルムの形成が示されており、腸内細菌叢がプラスチックを生分解する可能性を示唆しています [401]。これらの知見は、食事中のマイクロプラスチックが消化器系内でナノサイズの粒子に縮小され、一時的にそこに留まる可能性があることを示唆しています。腸内細菌叢の一部、特にプロテオバクテリアなどの病原性細菌やその他の病原性細菌は、腸内におけるプラスチックの蓄積によって引き起こされる環境変化に適応している可能性があります。これらの細菌は生存するだけでなく、ナノプラスチックを新たな炭素源として利用する可能性があります。さらに、このような代謝プロセスにはナノプラスチックをモノマーに分解する過程が関与している可能性があり、他の微生物群がそれを同化し、さらに分解する可能性があります。しかし、ヒトにおけるこれらの能力の直接的な証拠は依然として不足しています。現在、ヒト腸内におけるナノプラスチックの生分解に関与する酵素活性、微生物機能、またはプラスチック代謝物については、明確な理解が得られていません。最近の研究では、成人および乳児の糞便中に、ポリエチレンテレフタレート(PET)のモノマーであるテレフタル酸(TPA)と、ポリカーボネート(PC)のモノマーであるビスフェノールA(BPA)が含まれていることが確認されています。この知見は、プラスチック由来の代謝物と腸内細菌叢によるポリエチレンテレフタレートおよびポリカーボネートポリマーの生分解との潜在的な関連性を示唆しています[402]。 |
| 合成ポリマー以外にも、プラスチックには様々な商業用途に必要な特定の物理的・化学的特性を付与するために設計された数多くの添加剤が組み込まれています。そのため、プラスチックから生じる多様な分解生成物を考慮することが極めて重要です。分解生成物は、ポリマーの種類、添加剤、分解条件によって変化するからです。これらの生成物の多くは、特にホルムアルデヒド、ベンゼン、フランのように発がん性および変異原性があることが知られており、人体の健康に有害な影響を与える可能性があります[403]。マイクロプラスチックおよびナノプラスチックの分解副生成物は、腸内細菌叢によって腸内で特に高いバイオアベイラビリティを示し、ヒトおよび動物の健康にとって重大な懸念を引き起こしています。例えば、最も広く研究されているプラスチック分解化合物の一つであるパラノニルフェノールは、複数の生物における細胞増殖および生理機能に対する阻害作用により、様々な病態への関与が示唆されています[404]。ヒト腸内細菌叢による環境化学物質の代謝は、そのような添加物を体内に放出する上で極めて重要な役割を果たしている[405]。腸内微生物による変換によって副産物が生じ、それらは全身循環に吸収されるか、消化管上皮細胞に局所的な影響を及ぼす可能性がある。これらの相互作用は、宿主生理と微生物生態の両方に影響を及ぼす可能性がある[406]。さらなる研究が必要であるものの、新たなin vitroおよびin vivoのエビデンスは、腸内細菌叢がナノプラスチックへの曝露とヒトの健康への影響を結びつける生物学的導管であることを強調している。この関連性は結果として環境保健にも及び、それが人為的活動に依存していることを浮き彫りにしている。 |
| 9. 結論 |
| ヒトの消化管は、腸内細菌叢と呼ばれる複雑かつ動的な微生物集団の生息地であり、宿主と複雑な生化学的相互作用を通じて相互に有益な関係を築いています。宿主と微生物叢のこの共生関係は、微生物間および微生物叢と宿主間の動的な相互作用から生じます。バランスのとれた多様な微生物群集は、ユービオシス(優生共生)と呼ばれ、宿主の免疫系および代謝系の安定を維持するために不可欠です。このバランスは、病原菌の増殖を抑制するのにも役立ちます。実際、ユービオシスの条件下では、微生物叢は複雑かつ緻密に調整されたメカニズムを通じて、様々な臓器系や生理機能に調節的な影響を与えます。一方、微生物叢の構成の乱れは、ディスバイオシス(腸内細菌叢の乱れ)と呼ばれ、多くの疾患の発症との関連性がますます高まっています。 「オミクス」などの分野でのさらなる進歩が必要である一方で、プロバイオティクス、サイコバイオティクス、プレバイオティクス、シンバイオティクス、パラプロバイオティクス、メタバイオティクス、ポストバイオティクスなどのバイオモジュレーターを通じて腸内微生物集団に影響を与える能力は、ユーバイオシスを回復または維持するための興味深い機会を提供します。 |
| 腸内微生物叢を、局所的および全身的に重要な機能を持つ「細菌器官」と位置付ける根拠となる科学的証拠は豊富にあります。実際、腸内常在微生物は免疫応答の調節において重要な役割を果たしており、微生物バランスの乱れに対処することで、関連疾患を軽減、あるいは予防することが理論的には可能です。この複雑な統合により、人体は真核細胞と多数の微生物からなる「超生物」、すなわちホロバイオントへと変容します。ヘンダーソンとウィルソンが「ホモ・バクテリエンス」という用語を用いて適切に提唱したように、この概念はヒトと常在微生物との相利共生関係を捉えています[21]。 |
| 乳幼児期は免疫代謝プログラミングにとって極めて重要な時期であり、母乳栄養を受けていない乳児にとって、腸内細菌叢を標的としたカスタマイズされたバイオモジュレーターを調合乳に補充することは、母乳がもたらす効果を再現するための貴重な一歩となり得ます。このアプローチには大きな可能性が秘められていますが、このような戦略を臨床現場に広く導入するには、さらなる科学的検証が必要です。 |
| 腸内細菌叢をターゲットとした食事療法は、代謝性疾患や免疫介在性疾患の管理に不可欠なツールとして急速に認知されつつあります。食物繊維を豊富に含む食品、ポリフェノール、発酵食品は、ビフィズス菌や乳酸菌などの有益な細菌群の増殖を促進することが示されています。イヌリンやフラクトオリゴ糖などのプレバイオティクスは、健康増進に寄与する微生物の増殖を選択的に促進し、プロバイオティクスは生きた菌株を腸内生態系に直接導入します。ポストバイオティクス(細菌の副産物)も、抗炎症作用などの治療効果をもたらします。シンバイオティクスは、プレバイオティクスとプロバイオティクスを組み合わせることで、微生物の回復力と機能性を高めます。 |
| 糞弁微生物移植は、クロストリディオイデス・ディフィシル感染症例における腸内細菌叢の再構築において顕著な効果を示しており、メタボリックシンドロームや炎症性腸疾患(IBD)などの疾患の治療選択肢として研究されています。マイクロバイオーム解析に基づく個別化栄養戦略は、個々の微生物プロファイルに応じて食事介入をカスタマイズすることを目指しており、予防と治療の両方の成果を向上させる可能性があります。これらの進歩は、慢性非感染性疾患の管理におけるマイクロバイオーム調節の有望な役割を浮き彫りにしています。 |
| 腸内細菌叢は、アレルギー、肥満、糖尿病、消化器疾患などの発症と管理において重要な因子として浮上しています。腸内細菌叢は、宿主の全体的な健康状態を反映するだけでなく、生理学的プロセスの潜在的な媒介因子としても機能します。腸内細菌叢を治療標的として認識することは、微生物学、栄養科学、免疫学、システム医学などの分野を横断した学際的な連携の必要性を強調するものです。 |
| 食事療法、プレバイオティクス、プロバイオティクス、あるいは糞弁微生物移植のような微生物叢標的療法といった戦略的介入によるユーバイオシスの回復は、慢性非感染性疾患の管理において大きな可能性を秘めています。これらの進歩を達成するには、研究イニシアチブ、臨床応用、そして公衆衛生戦略にわたる協力的な取り組みが必要です。 |
| 上記を踏まえると、微生物叢研究における主要な課題の一つは、個人間でその構成が大きく異なることにあります。このばらつきは、食生活、遺伝、ライフスタイルなど、エクスポソームに含まれる要因の相互作用によって大きく左右されます。こうした多様性は、慢性非感染性疾患と特定の微生物成分との明確な因果関係を確立するための取り組みを複雑化させています。さらに、腸内微生物叢の構成と慢性非感染性疾患の相関関係は現在では十分に文書化されているものの、その根底にある生物学的メカニズムは依然として不明であり、もう一つの大きなハードルとなっています。横断研究から得られる知見が限られていることも、この問題をさらに浮き彫りにしています。なぜなら、これらの研究は、宿主と微生物叢の相互作用の経時的な動的な性質を捉える深みに欠けているからです。微生物叢の変化、疾患進行との関連性、そして微生物叢と宿主のダイナミクスを解明するには、マルチオミクスアプローチを組み込んだ大規模かつ縦断的な研究が必要です。この複雑さに対処するためには、食事、バイオモジュレーターの想定、そしてライフスタイルが腸内細菌叢の構成と関連する疾患の結果にどのような影響を与えるかを研究で優先的に探究する必要がある[407]。これには、治療戦略を変革する可能性を秘めた、腸内細菌叢を標的とした効果的なバイオモジュレーターの開発が含まれる。食生活パターン、生活習慣、そして新たな治療法を調査することで、個々の腸内細菌叢プロファイルに基づいた推奨事項をカスタマイズし、様々な疾患の予防と管理の改善を促進することができる[408]。 |
| 大きな進歩があったにもかかわらず、課題は依然として残っています。遺伝的背景、環境曝露、微生物多様性といった個人差により、「健康な」マイクロバイオームの標準的な定義を確立することは困難です。明確な微生物基準値の欠如や、集団間での知見の不一致も、因果関係の推論をさらに阻害しています。したがって、因果関係をより明確にし、治療効果を評価するために、標準化された方法論と縦断的研究が緊急に必要とされています。メタゲノミクス、メタボロミクス、トランスクリプトミクス、プロテオミクスを網羅するマルチオミクス技術の導入は、微生物の機能とそれらが宿主の生理機能に及ぼす影響の特定において、画期的な前進を意味します。 |
| 同時に、機械学習とシステム生物学の進歩は、複雑な微生物叢-宿主ネットワークをモデル化するための強力なツールを提供し、疾患の進行や治療反応を予測するバイオマーカーの特定を可能にしています。国際的な協力とオープンアクセスのマイクロバイオームデータベースも、画期的な進歩を促進し、臨床応用を加速させるために不可欠です。 |
| 人間の健康は環境やライフスタイルと複雑に絡み合っているため、包括的なアプローチが必要です。エクスポソームを構成するすべての構成要素は動的に相互作用し、相互に影響を与え合い、全体的な健康状態を決定したり、慢性疾患(慢性非感染性疾患)の発症に寄与したりする可能性があります(図5)。より良い健康成果を達成するには、人間と環境の相互作用に関するこの幅広い視点を考慮する必要があります。 |
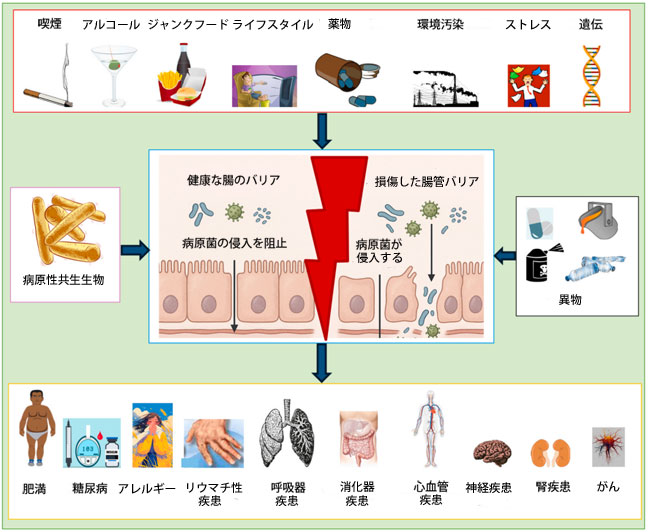 |
| 図5. 腸管バリア障害とそれに伴う全身疾患を決定する外的要因と内的要因 |
| パーソナライズされた栄養、精密なマイクロバイオームの調整、そして次世代プロバイオティクスは、健康成果に革命をもたらす大きな可能性を秘めています。将来的には、マイクロバイオームのプロファイルを個人の遺伝情報、代謝情報、免疫情報と統合し、精密な治療法を開発する戦略が期待されます。マイクロバイオームに基づいた診断と補助ツールは、食事療法から特定の健康課題を標的とした人工微生物コンソーシアムに至るまで、患者に合わせた治療への道を開くでしょう。 |
| 個別化ケアに加え、母乳育児の促進、抗生物質の誤用を最小限に抑えること、食物繊維が豊富で多様性に富んだ食事の推奨など、集団レベルの戦略に焦点を当てた公衆衛生イニシアチブは、微生物の全体的なレジリエンスを高め、慢性非感染性疾患の有病率を低下させる機会を提供します。一方、微生物叢を調節する分子、生きたバイオ医薬品、そして合成生物学の発展に関する研究は、微生物生態系を正確に再設計するための変革的な可能性を秘めています。 |
| マイクロバイオームの潜在能力を最大限に引き出すには、共同研究の取り組み、技術の進歩、そして微生物叢科学を医療と公衆衛生の枠組みに統合することが必要となる。マイクロバイオーム情報に基づいた医療が現実のものとなる時代に移行するにつれ、腸内微生物叢は疾患予防と個別化治療の両方において中心的な役割を果たすようになる。この点で、精密マイクロバイオーム編集や合成生態学といった微生物叢工学技術は、有望な介入手段として際立っている。これらの新たな手法は、微生物叢の構成と機能を操作して疾患を治療し、長期的な健康を促進する大きな可能性を示している[409]。高度なマルチオミクス研究は、微生物叢と宿主の相互作用をより包括的に理解するために不可欠となる。ゲノミクス、トランスクリプトミクス、プロテオミクス、メタボロミクス、マイクロバイオミクスを組み合わせた統合的なアプローチは、慢性非感染性疾患の根底にある重要な微生物バイオマーカー、治療標的、分子メカニズムの解明に役立つだろう。こうした進歩により、個々の微生物叢の特性に合わせた個別化医療の基盤が強化され、予防と治療の革新の新しい時代の到来を告げることになります。 |
| 結論として、腸内マイクロバイオームがヒトの健康に及ぼす重要性は、まだ解明され始めたばかりです。現在の知見は、広大な研究分野の表面的な部分に過ぎません。約800種の細菌とその7000種の異なる菌株のさらなる研究により、慢性非感染性疾患の予防と治療能力は飛躍的に向上すると期待されます。 |
参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
|
この文献は、Microbial Pathogenesis Volume 212, March 2026, 108213に掲載されたGut microbiota: origin or panacea for all ills? Immune and metabolic diseases, nutrition, and microbiota-based interventions.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |


