
Maneeth Mylavarapu et al., |
要約 |
| 本レビューでは、腸内細菌叢と心血管疾患(CVD)の双方向の関係を検証し、微生物のディスバイオシスがアテローム性動脈硬化症、高血圧、心不全などの心血管疾患にどのように寄与するかを解明することを目指します。最近の研究では、腸内細菌叢が短鎖脂肪酸やトリプトファン代謝物を介した免疫調節、腸管バリアの完全性の維持、短鎖脂肪酸(酢酸、プロピオン酸、酪酸)や動脈硬化促進性トリメチルアミンN-オキシド(TMAO)などの代謝物の産生に関与していることが強調されています。食生活、特に地中海式食事と西洋式食事の違いは、腸内細菌叢の構成と心血管疾患リスクに有意な影響を与えます。ポリフェノールと運動は、腸内細菌叢と心血管疾患のアウトカムに良い影響を与えることが示されています。腸内細菌叢と心血管の健康には重要な相互作用が存在します。ディスバイオシスとトリメチルアミンN-オキシドやリポ多糖などの代謝物は心血管疾患に関与しており、短鎖脂肪酸とバランスの取れた腸内細菌叢は心血管疾患の予防に寄与します。今後の研究では、個別化された心血管疾患治療法を特定するために、精密医療、次世代プロバイオティクス、最適化された糞便微生物移植、およびマルチオミクスアプローチに焦点を当てる必要があります。 |
| 目次(クリックして記事にアクセスできます) |
| 1. はじめに |
| 2. 方法 |
| 3. 腸内細菌叢:構成と機能 |
| 3.1. 構成 |
| 3.2. 機能 |
| 3.3. 宿主と微生物の関係 |
| 4. 腸内細菌叢と心血管の健康を結びつけるメカニズム |
| 4.1. 因果関係の実験モデル |
| 4.2. 腸内細菌叢のディスバイオシス |
| 4.3. 免疫調節 |
| 4.4. バリア機能不全 |
| 4.5. 代謝産物の動態 |
| 5. 腸内細菌叢と特定の心血管疾患 |
| 5.1. 動脈硬化 |
| 5.2. 高血圧 |
| 5.3. 不整脈 |
| 5.4. 心不全 |
| 5.5. 脳卒中 |
| 5.6. 肺血栓塞栓症 |
| 6. 食事と生活習慣が腸内細菌叢と心血管疾患の健康に及ぼす影響 |
| 6.1. 地中海食 |
| 6.2. 西洋型食生活 |
| 6.3. ポリフェノールと腸内環境 |
| 6.4. 運動と腸内細菌叢の調節 |
| 7.治療的介入 |
| 7.1. プロバイオティクスとプレバイオティクス |
| 7.2.糞便微生物移植 |
| 7.3. 薬理学的アプローチ |
| 7.4. 新たな治療戦略 |
| 8. 課題 |
| 9.今後の展望 |
| 10.結論 |
| 本文 |
| 1.はじめに |
| 人体は数兆個の微生物と動的な共生関係にあるという概念は、2001年のヒトゲノムプロジェクトの完了以降、注目を集めるようになりました[1]。それ以来、広範な研究により、腸内細菌叢が代謝、免疫、臓器機能など、様々な生理学的プロセスに深く影響を与えていることが明らかになってきました。消化管には推定100兆個の微生物が生息しており、主にフィルミクテス門やバクテロイデス門などの細菌門で構成され、放線菌、プロテオバクテリア、ヴェルコミクロビアなども少数含まれています[2, 3]。分子生物学とシーケンシング技術の進歩は、これらの微生物群集に関する理解に革命をもたらし、それらがヒトの健康に及ぼす影響についてのより深い探求を可能にしました。 |
| 腸内細菌叢は現在、心血管(CV)の健康において重要な役割を果たしていることが認識されており、その代謝副産物は血管機能、脂質代謝、全身性炎症を調節する複数のメカニズムに影響を及ぼしています[4]。心血管疾患は依然として世界的に罹患率と死亡率の主な原因であり、高血圧、脂質異常症、肥満、糖尿病、喫煙などの確立された危険因子があります[5]。しかし、新たなエビデンスは、腸内細菌叢の構成と機能が心血管の健康と疾患に不可欠であることを示唆しています[1、2、6-8]。腸内細菌叢と心血管疾患の相互作用は、主に短鎖脂肪酸、トリメチルアミンNオキシド、胆汁酸、リポ多糖などの微生物代謝物によって媒介されており、炎症、内皮機能、血圧調節、アテローム性動脈硬化に影響を及ぼします[7-10]。 |
| 腸内細菌叢の乱れ、すなわち腸内微生物バランスの乱れは、動脈硬化、高血圧、心不全(HF)などさまざまな心血管疾患の発症に関与していることが指摘されている [9]。腸内細菌叢の構成は、食事、年齢、遺伝、抗生物質の使用、環境曝露など、複数の要因によって形成される。飽和脂肪、加工炭水化物の摂取量が多く、食物繊維の摂取量が少ないという特徴を持つ西洋型の食生活は、腸内細菌叢の乱れ、トリメチルアミンNオキシド産生の増加、全身性炎症と関連しており、心血管疾患リスクの上昇に寄与している。一方、食物繊維とポリフェノールが豊富な地中海食や植物性食品中心の食事は、腸内細菌叢の多様性を促進し、短鎖脂肪酸産生を高め、心血管疾患に有益である [10–14]。 |
| 腸内細菌叢が心血管疾患の健康に果たす役割に対する認識が高まるにつれ、腸内細菌叢を標的とした介入が潜在的な治療戦略として検討されています。プロバイオティクス、プレバイオティクス、食生活の改善、そして微生物代謝物を標的とした薬理学的アプローチは、心血管疾患リスクを軽減する可能性について研究されています[13, 14]。マイクロバイオーム研究の分野は急速に発展しており、個別化されたマイクロバイオームに基づく治療法に焦点を当てた今後の研究は、心血管疾患の予防と管理の進歩に有望視されています[15–17]。 |
| 本レビューは、腸内細菌叢が心血管疾患の健康に及ぼす影響について包括的な概要を提供することを目的としています。主要な微生物代謝物、その根底にある病態生理学的メカニズム、そして潜在的な治療戦略を解明することにより、心血管疾患のアウトカム改善のためにマイクロバイオームに基づく介入を組み込んだプレシジョン・メディシン(精密医療)アプローチの必要性を強調します。 |
| 2. 方法 |
| 2000年から2024年の間に発表された論文について、PubMedとGoogle Scholarを用いて、「腸内細菌叢」「心血管疾患」「腸内毒素症」「トリメチルアミンNオキシド」「短鎖脂肪酸」「腸-心軸」をキーワードに包括的な文献検索を実施した。関連性は、研究デザインの質と腸心軸のメカニズム理解への貢献度に基づいて評価した。 |
| 3. 腸内細菌叢:構成と機能 |
| ヒト腸内細菌叢は複雑な微生物群であり、宿主の免疫系、代謝、そして健康全般に大きな影響を与えます[18]。この多様な生態系は、細菌、ウイルス、寄生虫、真菌、ファージ、真核生物、古細菌など、数多くの微生物で構成されています[1, 19]。ヒトマイクロバイオームを構成する10兆~100兆個の微生物のうち、細菌が大部分を占めています。これらの細菌の99%以上は、フィルミクテス門、バクテロイデス門、プロテオバクテリア門、放線菌門に属し、健康な人の腸内細菌叢においてフィルミクテス門とバクテロイデス門が最も多く存在します[20]。 |
| 3.1. 構成 |
| ヒトの消化管マイクロバイオームは、消化管に沿って変化する多様な微生物群から構成されています。 |
•食道:遠位食道マイクロバイオームは多様性が低く、レンサ球菌属が優勢です。プレボテラ属、放線菌属、ラクトバチルス属、ブドウ球菌属などの他の属も同定されています[21]。 •胃:胃は歴史的に細菌にとって住みにくい場所と考えられてきましたが、ヘリコバクター・ピロリ属が生息しており、微生物組成に大きな影響を与えています。その他の耐酸性細菌には、レンサ球菌属、ナイセリア属、ラクトバチルス属などがあります。研究では、パスツレラ属、ベイヨネラ属、ロチア属、レンサ球菌属、プレボテラ属などの優勢な属が特定されています[22–24]。 •小腸:十二指腸には主にフィルミクテス門細菌と放線菌が定着し、空腸にはラクトバチルス、エンテロコッカス、レンサ球菌などの通性嫌気性菌が生息する。回腸には大腸の微生物叢に類似した細菌叢が生息し、主に嫌気性菌とグラム陰性菌からなる[21]。 •大腸:フィルミクテス門細菌とバクテロイデス門細菌が優勢であるが、大腸にはバクテロイデス・テタイオタオミクロンやバクテロイデス・フラギリスなどの日和見病原菌も生息する[21]。 |
| 3.2. 機能 |
| 腸内細菌叢は、様々な代謝および免疫プロセスに寄与することで、宿主の健康に重要な役割を果たしています。 |
•食物繊維代謝:腸内細菌叢は食物繊維を短鎖脂肪酸(例:酢酸、プロピオン酸、酪酸)に発酵させ、腸の恒常性と炎症を調節します[1]。 •免疫:腸内細菌叢は、免疫系の形成、腸管関連リンパ組織(GALT)の発達促進、全身性炎症の調節において中心的な役割を果たします[19, 25]。 •脂質代謝:腸内細菌叢は、エネルギーバランス、グルコース代謝、脂質代謝に影響を与え、肥満やメタボリックシンドロームなどの病態に影響を与えます[26]。 •胆汁酸代謝:腸内細菌叢は一次胆汁酸を二次代謝物に変換し、コレステロールの恒常性と脂質吸収を調節します[19]。 •トリプトファン代謝:腸内細菌叢はトリプトファンをインドールなどの生理活性化合物に代謝し、免疫機能や炎症に影響を与えます[19]。 •短鎖脂肪酸:短鎖脂肪酸は、制御性T細胞の機能や粘膜防御に影響を及ぼすことで免疫応答を調節し、腸の完全性を維持します[19, 25–28]。 •コリン代謝:腸内細菌叢はコリンをトリメチルアミン(TMA)に変換し、トリメチルアミンは心血管疾患に関連する化合物であるトリメチルアミンNオキシドに酸化されます[1, 29]。 •腸-脳軸:腸内細菌叢は腸管神経系および中枢神経系と相互作用し、神経発達や認知機能に影響を与えます[30, 31]。 |
| 3.3. 宿主と微生物の関係 |
| 宿主と腸内細菌叢の関係は、主に共生関係ですが、ディスバイオティックな条件下では病原性へと変化する可能性があります。宿主は、免疫調節、微生物の空間的分離、代替栄養素の供給など、フィードバック機構を用いて微生物のバランスを維持しています。腸内細菌叢の構成と機能を理解することは、心血管疾患および全体的な健康状態を改善するための標的介入を開発する上で不可欠です[1]。 |
| 4. 腸内細菌叢と心血管の健康を結びつけるメカニズム |
| 最近の研究では、腸内細菌叢が心血管の健康に重要な役割を果たしていることが強調されており、腸内細菌叢の組成変化が心筋梗塞、高血圧、動脈硬化症などの様々な心血管疾患と関連していることが示されています[32, 33]。腸内細菌叢と心血管機能の複雑な関係は「腸-心軸」と呼ばれ[33]、腸内環境が心血管疾患の転帰に深く影響することを浮き彫りにしています。この双方向の相互作用をより深く理解することは、腸内細菌叢を標的とした心血管の健康改善のための新たな治療戦略を開発する上で不可欠です。 |
| 4.1. 因果関係の実験モデル |
| 糞便微生物移植(FMT)は、自然発生的な生理学的メカニズムではなく、因果関係を確立するための重要な実験モデルとして機能します。無菌動物モデルは、疾患感受性における腸内細菌叢の機能的役割を解明する上で重要な役割を果たしてきました。研究では、高血圧患者から無菌マウスへの糞便微生物移植後に血圧が有意に上昇することが示されており、腸内細菌叢の構成と高血圧との直接的な関連性が確立されています[34, 35]。さらに、特定の細菌種が心血管の健康状態を調節することに関与していることが示唆されています。例えば、酪酸産生細菌であるローズブリア・インテスティナリスを無菌ApoE欠損マウスに定着させると、炎症マーカーが減少し、動脈硬化病変の進行が抑制されることが示されています[36]。さらに、動脈硬化感受性の異なるマウス系統間の糞便微生物移植研究により、腸内細菌叢の構成が疾患発症に重要な役割を果たすことが明らかになりました[37]。これらの知見は、心血管疾患リスクに影響を与える上で、個々の細菌種と微生物群集全体の構造の両方が重要であることを強調しています。 |
| 4.2. 腸内細菌叢のディスバイオシス |
| 微生物群集の不均衡であるディスバイオシスには、普遍的に標準化された定義がなく、複雑な微生物動態を過度に単純化してしまう可能性があります。本レビューでは、ディスバイオシスを、微生物群集構造における不適応的な不均衡と定義します。これは、多様性の喪失、有益な共生菌の減少、病原性共生菌の増加を特徴とし、宿主-微生物間の恒常性を破壊し、疾患の病態に寄与します[38]。健康な腸内細菌叢は、バクテロイデス属とフィルミクテス属のバランスの取れた比率を特徴としており、この比率はpH、酸素レベル、栄養素の利用可能性などの要因により消化管内で変化します[38]。16S rRNA遺伝子配列解析を用いた初期の研究では、冠動脈疾患(CAD)に関連する細菌分類群が特定されました[39]。 |
| 研究によると、冠動脈疾患患者ではラクトバチルス(フィルミクテス)属細菌の増殖が亢進し、バクテロイデス属細菌(バクテロイデスおよびプレボテラ)の増殖が減少することが示されています[40]。さらに、メタゲノム解析により、動脈硬化性心血管疾患患者では腸内細菌科細菌および口腔内細菌の増殖が亢進する一方で、酪酸産生細菌の増殖は低下していることがわかっています[41]。心不全患者では、微生物多様性の低下、コア微生物叢の枯渇、クロストリジウム・ディフィシル感染症に対する感受性の上昇が認められます[42, 43]。さらに、右房圧の上昇は、粘膜バイオフィルム形成の増加、細菌の過剰増殖、カンジダ、カンピロバクター、赤痢菌などの病原菌の定着と関連付けられています[44]。特に、フェカリバクテリウム・プラウスニッツィやラクノスピラ科などの酪酸産生細菌の減少は、心不全患者集団全体で炎症マーカーの上昇と相関している[42, 45]。 |
| 4.3. 免疫調節 |
| 腸内細菌叢が免疫細胞の活性、特にT細胞の機能を調節することで心血管の健康に影響を与えることを示唆するエビデンスが増えています[46, 47]。炎症を起こしやすいマウスから動脈硬化を起こしやすいマウスへの腸内細菌叢の移行は、インターロイキン(IL)-1β、IL-2、インターフェロン(IFN)-γなどの全身性炎症性サイトカインの上昇に起因すると考えられる、動脈硬化性プラーク形成を促進することが示されています[48, 49]。逆に、バクテロイデス・ブルガトゥスおよびバクテロイデス・ドレイの補給は、血漿中の腫瘍壊死因子α(TNF-α)レベルおよび動脈硬化性病変を減少させることが示されています[49]。同様に、ラクトバチルス・プランタラムATCC 14917の投与は、酸化LDL、TNF-α、インターロイキン-1β(IL-1β)のレベルを低下させることで、病変形成を軽減しました。ロゼブリアとブラウティアの存在は、血漿コレステロール、TNF-α、IL-1β、および動脈硬化負荷の低下と関連しています[50, 51]。さらに、食事からの塩分摂取は、腸内細菌叢の変化を介して高血圧と関連付けられています。塩分の過剰摂取はラクトバチルス・ミュリヌスを枯渇させ、血圧の上昇をもたらしますが、サプリメントの摂取はTヘルパー17(TH17)細胞の活性を調節することでバランスを回復させ、高血圧管理のための潜在的な治療法を提供します[52]。 |
| 4.4. バリア機能不全 |
| 腸管バリアは粘液層、タイトジャンクション、免疫防御から構成され、細菌の転座を阻害します。この関係は双方向性です。バリアの破綻はリポ多糖の転座を可能にしますが、グラム陰性細菌の細胞壁の構成成分であるリポ多糖自体はタイトジャンクションタンパク質を直接損傷し、透過性をさらに高め、エンドトキシン血症と炎症の悪循環を引き起こします[53]。心血管疾患患者ではエンドトキシン濃度が上昇しており、肝静脈血中のエンドトキシン濃度は心室血中よりも高くなります[54, 55]。アッケルマンシア・ムシニフィラなどの特定の細菌種は、腸管の完全性を維持するのに役立ちます。A. ムシニフィラによる治療は、ApoE欠損マウスにおいてエンドトキシン血症と大動脈アテローム性動脈硬化を軽減することが示されている[56]。ヒト研究では、低温殺菌したA. ムシニフィラの治療効果がさらに裏付けられており、肥満者の循環リポ多糖レベルを低下させることが明らかになっています[57]。これらの知見は、腸管バリア機能の強化と腸内細菌叢の調整を目的とした戦略が、心血管疾患の予防と治療に有望な道筋となる可能性を示唆しています。 |
| 4.5. 代謝産物の動態 |
| 腸内細菌叢は代謝器官として機能し、宿主の全身循環においてシグナル伝達分子として作用する生理活性物質を産生する。保護的な代謝産物と動脈硬化促進的な代謝産物のバランスは、心血管系の健康状態を決定する主要な要因である。 |
| 短鎖脂肪酸は、主にフェカリバクテリウムやローズブリアなどの細菌による食物繊維の発酵によって生成され(酢酸、プロピオン酸、酪酸を含む)、重要な心臓保護効果を発揮します。メカニズム的には、短鎖脂肪酸はヒストン脱アセチル化酵素(HDAC)阻害剤として機能し、血管内皮における炎症誘発性遺伝子発現を抑制します。さらに、短鎖脂肪酸はGタンパク質共役受容体(GPR41およびGPR43)と相互作用し、レニン分泌制御と血管拡張を介して血圧を調節します[58、59]。逆に、トリメチルアミンNオキサイドは主要な動脈硬化促進代謝物です。腸内細菌は、トリメチルアミン部分を含む食事栄養素、特に赤身肉や卵に含まれるコリン、ホスファチジルコリン、L-カルニチンをトリメチルアミンに代謝します[60]。 トリメチルアミンは肝臓でフラビン含有モノオキシゲナーゼ(FMO3)によって吸収され酸化されてトリメチルアミンNオキサイドを生成する。トリメチルアミンNオキサイドは、(1)逆コレステロール輸送の阻害、(2)マクロファージ上のスカベンジャー受容体(CD36およびSR-A1)のアップレギュレーションによる泡沫細胞の形成、(3)血小板の過剰反応性および血栓症リスクの増強という3つの異なるメカニズムによって心血管病理を促進する[60-63]。 |
| ディスバイオシスによって誘発されるバリア機能障害は、エンドトキシンであるリポ多糖の循環への移行を促進します。リポ多糖は内皮細胞および免疫細胞上のToll様受容体4(TLR4)に結合し、NF-κB炎症カスケードを誘発して全身性炎症を引き起こします[64, 65]。さらに、腸内細菌は胆汁酸プールを調節します。二次胆汁酸はファルネソイドX受容体(FXR)およびTGR5上のシグナル分子として作用し、脂質およびグルコース代謝に影響を与えます[65]。これらの知見を総合すると、腸内細菌叢代謝物が心血管の健康に及ぼす二重の影響が強調され、短鎖脂肪酸は保護効果を発揮する一方、トリメチルアミンNオキサイドおよびリポ多糖は疾患の進行に寄与します。したがって、微生物バランスを維持することは心血管の健康にとって不可欠です[60–65]。図1は腸-心臓軸の統合されたメカニズム経路を探求し、表1は心血管機能に対する微生物の影響の包括的な概要を示しています。 |
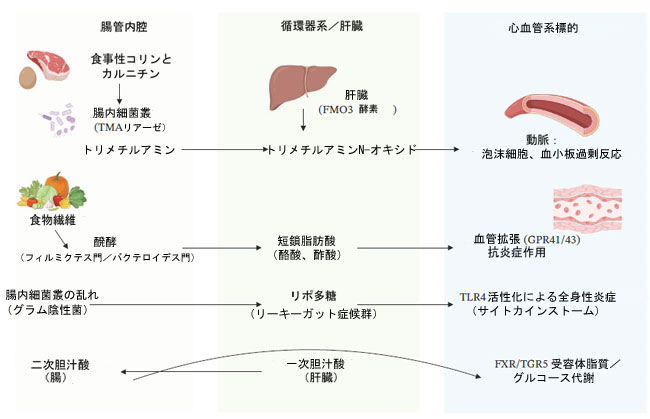 |
| 図1. 腸-心臓軸の統合的なメカニズム経路 |
| 表1.腸内細菌叢が心血管疾患に及ぼす主な影響メカニズム |
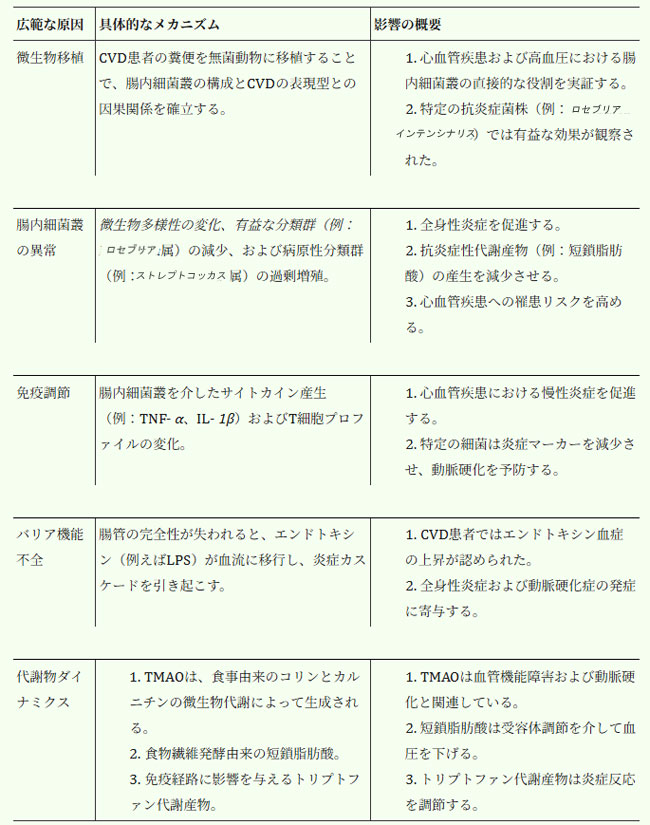 |
| 略語: CVD、心血管疾患; IL-1β、インターロイキン1ベータ; LPS、リポ多糖; SCFAs、短鎖脂肪酸; TMAO、トリメチルアミンN-オキシド; TNF-α、腫瘍壊死因子アルファ。 |
| 5. 腸内細菌叢と特定の心血管疾患 |
| 5.1. 動脈硬化 |
| 動脈硬化は、脂質代謝の異常と不適切な免疫応答によって引き起こされる慢性炎症性疾患であり、動脈壁内にコレステロールを豊富に含むマクロファージが蓄積する[66]。16S rRNA遺伝子パイロシークエンシングを用いた研究により、動脈硬化プラークには腸内細菌叢に一般的に見られる系統型の細菌DNAが含まれていることが明らかになっている。プラーク中の細菌DNA量は炎症と相関しており、微生物の転座の可能性を示唆している[66, 67]。ストレプトコッカス属やベイロネラ属などの特定の細菌はプラークの構成に直接影響を与える可能性があり、シュードモナス属、クレブシエラ属、肺炎クラミジアも動脈硬化病変内で同定されている[68]。しかし、ほとんどの研究では、プラーク微生物叢の構成とプラーク破裂や心血管イベントなどの臨床転帰との間に明確な関連性は確立されていません[68-70]。 |
| 代謝的には、アテローム性動脈硬化症の進行は、第4.5節で説明したトリメチルアミンNオキサイド経路に大きく影響されます。血漿トリメチルアミンNオキサイドレベルの上昇は、ヒトにおけるアテローム性動脈硬化症の負担増加および主要な心血管イベント(MACE)の増加と強く相関しています[71]。動物モデルでは、トリメチルアミン生成の食事による抑制がプラーク形成を弱め、因果関係を裏付けています[72]。逆に、短鎖脂肪酸産生細菌の枯渇は酪酸の利用可能性を低下させ、血管炎症に対する保護的な抑制をなくし、プラークの進行を加速させます[72-74]。 |
| 5.2. 高血圧 |
| 高血圧は心血管疾患の主要な修正可能な危険因子であり、腸内細菌叢の異常と強く関連している[75, 76]。微生物組成の変化としては、フィルミクテス門とバクテロイデス門の比率(F/B比)の増加、短鎖脂肪酸産生菌の減少、乳酸菌の増加、プロテオバクテリア門とシアノバクテリア門の増加などが挙げられる[69]。 |
| メカニズム的には、短鎖脂肪酸の減少は血圧調節を阻害します。セクション4.5で述べたように、短鎖脂肪酸は通常GPR41と相互作用して血管拡張を媒介します。高血圧動物モデルでは、短鎖脂肪酸の利用可能性の低下は末梢血管抵抗の増加と血管リモデリングにつながります[77–80]。さらに、高血圧の既知のリスク因子である高塩分摂取は、ラクトバチルス・ムリヌスを減少させることが示されており、この細菌を補給すると、Tヘルパー17(TH17)細胞の活性を調節することにより、塩感受性高血圧を予防します。逆に、トリメチルアミンNオキサイドレベルの上昇は、アンジオテンシンIIの昇圧効果を延長し、酸化ストレスを介して内皮機能障害を誘発することにより、高血圧に寄与します[81–83]。短鎖脂肪酸産生菌群を回復させることを目的としたプロバイオティクス介入は、これらの血管炎症反応を軽減することにより収縮期血圧を下げるのに有望であることが示されています[84]。 |
| 5.3. 不整脈 |
| 心房細動(AF)は最も一般的な持続性不整脈であり、腸内細菌叢異常によって引き起こされる全身性炎症との関連性がますます指摘されている。心房細動における「腸と心臓」のつながりは、主に炎症性シグナル伝達と心房の構造的リモデリングを介して媒介される[85]。腸内細菌叢異常は、腸管バリア機能を障害し、血中リポ多糖濃度の上昇を引き起こすことで心房細動の進行に寄与する[85-87]。リポ多糖は心房筋細胞内のNLRP3インフラマソームを活性化し、炎症性サイトカインであるIL-1βとIL-18の放出を促進する。この炎症環境は心房線維化を促進し、リエントリー性不整脈の基質となる[86]。さらに、トリメチルアミンNオキサイド濃度の上昇は、心房自律神経リモデリングの促進と心房細動感受性の増加に関与していると考えられている[88-90]。 トリメチルアミンNオキサイドは心房組織へのM1マクロファージの浸潤を促進し、炎症と線維化を悪化させる。逆に、胆汁酸はこのリスクを調節する。二次胆汁酸によるファルネソイドX受容体の活性化は心房細動を引き起こす炎症カスケードを阻害することが示されており、健康な胆汁酸代謝を維持することが不整脈の発症に対する保護となることを示唆している[91-94]。図2は、腸内細菌叢、炎症、および心房細動の関係を示している。 |
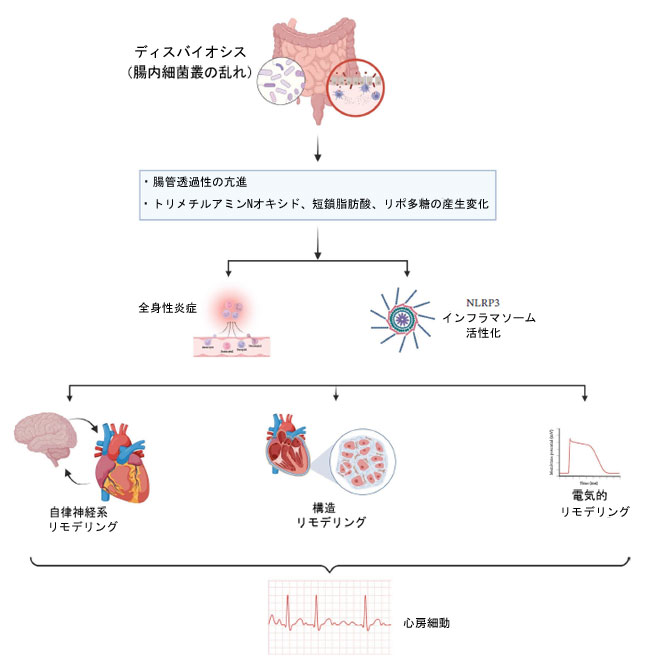 |
| 図2. 腸内細菌叢、炎症、および心房細動の関係 |
| 5.4. 心不全 |
| 心不全(HF)は主に、冠動脈疾患、高血圧、代謝障害などの疾患に起因する心筋機能障害によって引き起こされます[95]。近年の研究により、腸内細菌叢と心不全の間には双方向的な関係があることが明らかになってきています。腸内細菌叢の異常は、全身性炎症、酸化ストレス、代謝異常を引き起こし、心筋機能障害を悪化させます[95, 96]。 |
| 「心不全の腸仮説」によれば、心拍出量の低下、腸浮腫、腸運動の変化によって引き起こされる腸管透過性と腸内細菌叢組成の変化が心不全の転帰を悪化させる[97]。心不全患者はカンピロバクター、シゲラ、サルモネラなどの病原性細菌による腸内コロニー形成が増加し、全身性炎症が増強される[44]。さらに、リポ多糖は心筋細胞、心臓線維芽細胞、マクロファージ上のToll様受容体4(TLR4)に結合し、NLRP3インフラマソームの活性化を介して炎症性サイトカインの放出と心筋損傷を促進する[98, 99]。 |
| 短鎖脂肪酸産生細菌(ユーバクテリウム、フェカリバクテリウム、ルミノコッカスなど)は心不全患者で減少しているのに対し、炎症誘発性プロテオバクテリアの過剰増殖がよく見られる[100, 101]。プロバイオティクスまたはプレバイオティクス介入による腸内細菌叢のバランス回復は、炎症マーカーと臨床転帰の改善を示している[102]。トリメチルアミンNオキサイドはSmad3シグナル伝達を活性化することで心筋肥大と線維化に寄与し、左心室拡張と脳性ナトリウム利尿ペプチドレベルの上昇につながる。さらに、加齢に伴う慢性的な低度炎症状態である炎症性老化は、高齢心不全患者の腸内細菌叢異常と関連付けられている[103–105]。 |
| 5.5. 脳卒中 |
| 腸内細菌叢とその代謝産物は、虚血性脳卒中を含む神経疾患の進行を調節します[106]。腸内細菌叢の異常は腸内環境を変化させ、栄養吸収、免疫恒常性、全身代謝に影響を与え、高血圧や糖尿病などのメカニズムを介して虚血性脳卒中のリスクを高めます[107]。さらに、脳卒中の重症度と予後は、免疫応答、炎症、血栓形成を調節する腸内細菌叢の変化によって影響を受けます[108]。 |
| 腸内細菌叢-腸-脳軸は、神経、内分泌、免疫経路を介して腸と中枢神経系間の双方向コミュニケーションを促進する[109–111]。短鎖脂肪酸などの微生物代謝産物は、脳-腸バリアの完全性に寄与し、酸化ストレスを軽減し、急性虚血性脳卒中(AIS)後の神経炎症を軽減する[112]。さらに、脳卒中後の細菌移行は、自律神経系の過剰活性化と過剰なグルココルチコイド放出により腸内細菌叢の異常と腸管透過性を悪化させ、脳卒中関連感染症に寄与する可能性がある[113]。 |
| 5.6. 肺血栓塞栓症 |
| ディスバイオシスは、特に有益な常在細菌の減少と腸内細菌科などの病原性グラム陰性菌の過剰増殖によって、静脈血栓塞栓症のリスク増加に関与していると考えられています。グラム陰性菌の外膜を構成する糖脂質成分であるリポ多糖は、血管内皮細胞および血小板上のToll様受容体に結合することで凝固カスケードを活性化し、過凝固状態を誘発します。トリメチルアミンNオキサイドは血小板の過剰反応性を高め、血栓形成を促進することで、肺血栓塞栓症の感受性をさらに高めます[114]。 |
| 最近の研究では、腸内細菌叢異常に関連する血栓形成に対抗するためのプレバイオティクスおよびプロバイオティクス介入が検討されており、レスベラトロールは過凝固状態を緩和し、血栓リスクを低減する有望な候補として浮上している[115]。 |
| 6. 食事と生活習慣が腸内細菌叢と心血管疾患の健康に及ぼす影響 |
| 腸内細菌叢の構成と機能は食事によって大きく左右されますが、運動や睡眠といったその他の生活習慣も重要な役割を果たします。食習慣、腸内環境、免疫機能の間の動的な相互作用は十分に研究されており、腸内細菌叢が心血管疾患の健康に及ぼす影響を裏付ける証拠が増えつつあります[116]。食事によって腸内細菌叢が変化すると、感染症や全身性炎症への感受性が高まり、ひいては心血管疾患の転帰に影響を与える可能性があります。 |
| ヒトの消化管には多様な微生物群集が存在し、その大部分は大腸に生息しており、未消化の炭水化物、タンパク質、食物繊維の発酵によって短鎖脂肪酸が生成される[117]。酪酸、酢酸、プロピオン酸などのこれらの短鎖脂肪酸は、免疫応答や代謝経路の調節に不可欠である。大腸に優勢な細菌属には、ビフィドバクテリウム、ラクトバチルス、バクテロイデス、クロストリジウム、エシェリヒア、ストレプトコッカス、ルミノコッカスなどがある。腸内細菌叢と心血管恒常性の間には複雑な関係があるため、腸内微生物組成を変化させる生活習慣の選択は、腸-心臓軸に大きな影響を与える可能性がある[116-118]。 |
| 6.1. 地中海食 |
| 地中海食(MD)は、豆類、全粒穀物、ナッツ類、果物、野菜、エキストラバージンオリーブオイルなどの植物性食品を重視していることから、心血管に対する有益な効果について広く研究されてきました。この食事はオメガ3多価不飽和脂肪酸(PUFA)を豊富に含み、ペルオキシソーム増殖因子活性化受容体γ(PPAR-γ)を活性化し、核因子κB(NF-κB)を阻害することで、抗動脈硬化作用と抗炎症作用を発揮し、TNF-αなどの炎症性サイトカインの産生を抑制します。その結果、地中海食を遵守することで、冠動脈疾患、炎症性腸疾患、その他の慢性炎症性疾患のリスクが低下することが示されています[119, 120]。 |
| 地中海食は直接的な心血管系への効果に加えて、腸内細菌叢の多様性を促進します。食物繊維が豊富なため、バクテロイデス属の細菌の増殖が促進され、腸内酸性化が強化され、バランスの取れた微生物生態系が維持されます[120, 121]。さらに、地中海食に含まれる食物繊維の発酵により、短鎖脂肪酸、特に酪酸が生成されます。酪酸は、心血管疾患や一部のがんの発生率低下と関連付けられています[122]。Kimbleらによる対照試験では、地中海食の摂取により、ポリフェノール代謝に関与する細菌であるアドラークロイツィア ・エクオリファシエンスと、強力な抗炎症作用を持つ酪酸産生菌であるF. プラウスニッツィーの存在量が増加することが実証されました[121–123]。 |
| 6.2. 西洋型食生活 |
| 一方、飽和脂肪酸、精製炭水化物、糖類、加工食品、赤身肉の摂取量が多いことを特徴とする西洋型食生活(WD)は、腸内細菌叢の異常や心血管疾患の悪化と関連付けられています[121, 122]。西洋型食生活を長期間続けると、リポ多糖の分泌とカイロミクロン(訳者注:カイロミクロン(Chylomicron)は、食事で摂取した脂質を小腸から全身へ運ぶ、最大かつ最も低密度なリポタンパク質(脂質とタンパク質の複合体)です。主成分はトリアシルグリセロール(中性脂肪)で、リンパ管を通って血液に入り、脂肪細胞や筋肉へエネルギーを運びます)の蓄積が促進され、アリステプス属やバクテロイデス属などのグラム陰性菌の増殖が促されます。この変化は腸管タイトジャンクションの完全性を損ない、リポ多糖の血流への移行を促進し、TNF-α、インターフェロンγ(IFN-γ)、IL-1βの上昇を介して全身性炎症を引き起こします。この慢性炎症状態は、時間の経過とともに内皮機能障害、高血圧、動脈硬化症につながります[120, 124, 125]。 |
| Tangらによる3年間の研究では、高濃度の食事性ホスファチジルコリン(西洋型食生活に豊富に含まれる成分)が、動脈硬化のリスク増加と強く関連する腸由来代謝物であるトリメチルアミンNオキサイドの産生につながることがわかった[126]。さらに、座りがちな生活習慣と砂糖入り飲料やアルコールの過剰摂取の組み合わせは、腸管バリアの破壊をさらに悪化させる。Leclercq博士による60人の患者を対象とした研究では、アルコール摂取が腸内微生物バランスを大きく変化させ、長期的な心臓および代謝機能障害につながることが示された[127]。 |
| 6.3. ポリフェノールと腸内環境 |
| 果物、野菜、お茶、ココア、ワインなどの植物性食品に含まれる食事性ポリフェノールは、抗酸化作用や心臓保護作用について広く研究されています[128, 129]。これらの化合物は、ビフィズス菌や乳酸菌などの有益な細菌の増殖を促進することで、腸内細菌叢の多様性を高めます。特に赤ワインに含まれるポリフェノールは、代謝の健康に有益な効果をもたらすバクテロイデス属の細菌の増加と関連付けられています[128, 129]。 |
| ポリフェノールを豊富に含む食事はプレバイオティクスとして働き、有益な微生物の活動を促進し、栄養素の吸収を改善します [128–130]。一般的なプロバイオティクスであるビフィドバクテリウムは、免疫機能をサポートし、炎症性腸疾患から保護し、がんのリスクを低減することが示されています。さらに、ココア由来のポリフェノールは、高密度リポタンパク質 (HDL) レベルの上昇、血漿トリグリセリドおよび炎症マーカーの減少と関連付けられています [129、130]。さらに、ポリフェノールは、黄色ブドウ球菌やサルモネラなどの有害な病原体に対して抗菌活性を発揮し、病原性クロストリジウム種の増殖を抑制します [130]。ポリフェノールのサブタイプであるヒドロキシケイ皮酸は、肝保護作用、抗肥満作用、および心血管系への有益性を示しています [129–131]。さらに、ポリフェノールを豊富に含む食品に含まれるフラボノイドは、フリーラジカルスカベンジャーとして働き、血中脂質レベルとコレステロールを低下させる[132]。 |
| 6.4. 運動と腸内細菌叢の調節 |
| 身体活動は、腸内細菌叢の構成を調節するもう一つの重要な因子です。定期的な運動は微生物の多様性を高め、バクテロイデス門とファーミキューテス門の比率を改善します。これは、体重管理や代謝の健康状態の改善につながります。運動は、腸管バリアの完全性と粘膜免疫を強化する有益な微生物の増殖を促進します[133]。 |
| 運動中、骨格筋の収縮はインターロイキン-6(IL-6)などのマイオカインの放出を刺激し、その結果、グルコース代謝の重要な調節因子であるグルカゴン様ペプチド-1(GLP-1)の分泌が促進されます[133, 134]。運動はまた、短鎖脂肪酸の産生を増加させ、腸管の健全性の向上、全身性炎症の軽減、代謝機能の向上につながります[134, 135]。Zhongらによる無作為化比較試験(RCT)では、女性における有酸素運動が腸内細菌叢の多様性を大幅に改善し、有益な微生物の変化が心血管リスク因子の減少と関連していることが実証されました。16S rRNAシーケンスを使用して、この研究では健康増進細菌属の増加が特定され、身体活動、腸の健康、心血管の健康の間のつながりが強化されました[136]。 |
| 7.治療的介入 |
| 消化管に生息する複雑な微生物群集である腸内細菌叢は、心血管疾患を含む全身の健康において極めて重要な役割を果たしています。このことから、心血管疾患の予防と管理を目的とした腸内細菌叢を標的とした治療的介入への関心が高まっています。現在の戦略としては、プロバイオティクス、プレバイオティクス、糞便微生物移植、および薬物療法などが挙げられます。 |
| 7.1. プロバイオティクスとプレバイオティクス |
| プロバイオティクス(健康に有益な効果をもたらす生きた微生物)とプレバイオティクス(有益な細菌の増殖を促進する消化されない食品成分)は、心血管保護効果について広く研究されてきました。臨床試験では、心血管リスク因子の調節における有効性が実証されています。例えば、2型糖尿病(T2DM)患者を対象とした試験では、6週間のプロバイオティクス補給により、血圧とフラミンガムリスクスコアが有意に低下することが示されました[137]。同様に、メタアナリシスでは、血圧、総コレステロール、LDLコレステロール、血糖値、HbA1c、BMIの有意な低下とHDLコレステロール値の上昇が確認されました[138]。これらの効果は、長期にわたる介入、高用量、および代謝障害のある患者において特に顕著でした。 |
| プロバイオティクスの利点は菌株によって異なります。ラクトバチルス・アシドフィルス、L.プランタルム、L.ファーメンタム、L.ガセリなどの菌株は、血圧と脂質プロファイルの改善を示しています。さらに、L.ラムノサス GR-1とリモシラクトバチルス・ロイテリRC-14は女性の泌尿生殖器の健康に貢献し、間接的に全体的な健康をサポートします[139]。複数の菌株からなるプロバイオティクス製剤は、単一菌株による介入と比較して優れた有効性を示すことが多く、心血管の健康アウトカムをより効果的に向上させます。リモシラクトバチルス・ロイテリTF-7、エンテロコッカス・フェシウムTF-18、ビフィドバクテリウム・アニマルス TA-1などの特定の菌株は、コレステロール低下作用を示し、相乗的に脂質プロファイルと腸内細菌叢の構成を改善します[140、141]。これらの利点の根底にあるメカニズムには、短鎖脂肪酸の生成、胆汁酸加水分解酵素活性、脂質代謝調節、全身性炎症の調節などがあり、これらすべてが心血管の健康の改善に貢献しています[141]。 |
| 7.2.糞便微生物移植 |
| 糞便微生物移植(FMT)とは、健康なドナーからレシピエントへ腸内細菌叢を移植するプロセスであり、主にクロストリジオイデス・ディフィシル感染症の治療に用いられる新たな治療法として注目されています。心血管疾患に対するその可能性は現在研究中です。前臨床研究では、糞便微生物移植が腸内細菌叢の構成を変化させ、全身性炎症を軽減することで、動脈硬化の発症に影響を与える可能性が示唆されています[111]。しかしながら、ヒトを対象とした研究はまだ限られています。 |
| 糞便微生物移植の潜在的な心血管系への効果としては、代謝プロファイルの改善、腸由来の炎症の調節、メタボリックシンドロームに関連する炎症マーカーの減少などが挙げられます。糞便微生物移植は有望視されているものの、心血管疾患に対する直接的なエビデンスが限られていること、感染伝播のリスク、結果のばらつき、倫理的および規制上の懸念など、いくつかの課題があります。心血管系への応用における有効性と安全性を確立するためには、標準化されたプロトコルと大規模な臨床試験によるさらなる研究が必要です[142]。 |
| 7.3. 薬理学的アプローチ |
| 腸内微生物代謝産物を標的とすることは、心血管疾患介入の新たな道筋となる。最も研究が進んでいる微生物代謝産物の一つがトリメチルアミンNオキサイドであり、これは腸内細菌による食事由来のコリンとカルニチンの代謝によって生成される。トリメチルアミンNオキサイド濃度の上昇は、動脈硬化や心血管疾患の有害事象と関連付けられている[143]。トリメチルアミンNオキサイドを減少させるための薬理学的戦略には、以下のようなものがある[144]。 |
1. トリメチルアミン生成に関与する微生物酵素を標的とすることでトリメチルアミン産生を阻害する、 2. トリメチルアミンからトリメチルアミンNオキサイドへの肝臓での変換を阻害する、 3. 腸内細菌叢全体のバランスを崩すことなく、トリメチルアミン産生経路を選択的に抑制する非致死性阻害剤を使用する。 |
| トリメチルアミンNオキサイドレベルを低下させることは、血小板反応性や血栓症リスクなどの心血管リスク因子を低下させる可能性を示している。短鎖脂肪酸や胆汁酸などの他の腸由来代謝物も心血管の健康に重要な役割を果たしており、食事、プロバイオティクス、薬理学的薬剤による追加の治療機会を提供している[144-146]。 |
| 7.4. 新たな治療戦略 |
| 腸-心軸は、宿主の代謝、炎症、免疫応答の調節における腸内細菌叢の役割を強調している。新たな治療戦略は、細菌代謝産物を標的とし、腸管バリア機能を強化し、炎症経路を調節することを目的としている[147]。 |
| 次世代プロバイオティクス(NGP)は、安定性の向上と標的疾患管理のために設計されており、微生物叢に基づく治療における有望な進歩を表しています。合成生物学とバイオインフォマティクスの統合により、より精密な介入が可能になっています[148、149]。今後の方向性としては[147–149]が挙げられます。 |
・個々の腸内細菌叢プロファイルに合わせた個別化マイクロバイオーム療法、 ・心血管系への効果を最適化した複数菌株プロバイオティクス製剤、 ・より高い有効性を確保する先進的なプロバイオティクス送達システム、 ・腸内細菌叢の調節を最大化するプレバイオティクスとプロバイオティクスの併用療法。 |
| 8. 課題 |
| 腸内細菌叢が心血管疾患の健康に果たす役割がますます認識されるようになっているにもかかわらず、いくつかの重要な課題が依然として残っています。最も大きな課題の一つは、因果関係と相関関係を区別することです。多くの研究で腸内細菌叢の異常と心血管疾患との関連性が確立されていますが、腸内細菌叢の変化が心血管疾患の発症や進行に直接的に寄与するという決定的な証拠はまだ得られていません。因果関係を明らかにするためには、腸内細菌叢の調節を目的とした大規模な縦断研究や介入型ランダム化比較試験が必要です。この臨床応用におけるギャップを明確にするため、表2では、マウスモデルで確立された因果メカニズムと、ヒトを対象とした研究で観察された臨床的関連性を比較しています。 |
| 表2.動物モデルとヒト臨床試験における主要な知見の比較 |
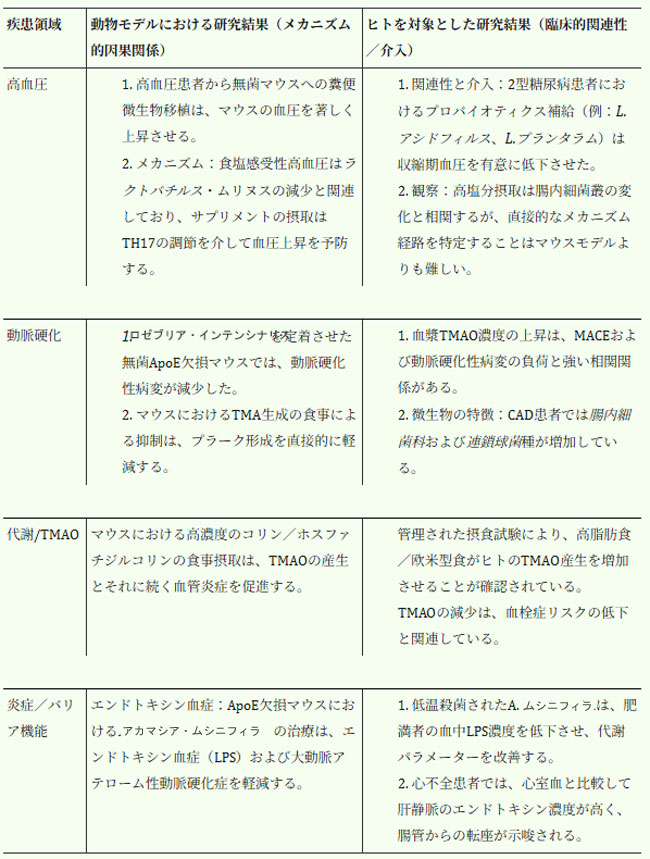 |
| 略語: ApoE、アポリポタンパク質E; BP、血圧; CAD、冠動脈疾患; FMT、糞便微生物移植; LPS、リポ多糖; MACE、主要心血管イベント; T2DM、2型糖尿病; TH17、Tヘルパー17細胞; TMA、トリメチルアミン; TMAO、トリメチルアミンN-オキシド。 |
| もう一つの大きな課題は、腸-心軸の根底にある正確なメカニズムを解明することです。トリメチルアミンNオキサイド産生、短鎖脂肪酸、炎症などの経路が重要な役割を果たしていると考えられていますが、それらの相互作用や相対的な寄与は依然として不明です。ゲノミクス、メタボロミクス、プロテオミクスを統合したマルチオミクスアプローチは、腸内細菌叢、宿主代謝、心血管機能の複雑な相互作用を解明するために不可欠です。主要な微生物種とその代謝産物を特定することは、治療標的の絞り込みにおいて極めて重要となるでしょう。 |
| 腸内細菌叢の構成における個人差は、普遍的な介入策の開発をさらに複雑にしています。遺伝、食事、ライフスタイル、環境曝露などの要因が大きな異質性をもたらし、より個別化されたアプローチが必要となります。腸内細菌叢プロファイルに基づいて個人を層別化することで介入効果を高めることができますが、そのためには高度なプロファイリング技術と堅牢なデータ分析手法が必要です。さらに、研究デザイン、サンプル収集、シーケンス技術、データ解釈における不一致が再現性を阻害しています。腸内細菌叢研究のための標準化されたプロトコル、特に腸管バリア機能と全身性炎症を評価するための統一された方法論を確立することは、信頼性が高く比較可能なデータを生成するために不可欠です。 |
| 腸内細菌叢研究を効果的な臨床治療へと応用することには、大きな課題が伴います。最適なプロバイオティクス株、プレバイオティクス、腸内細菌叢調節戦略の特定、そして効率的な送達システムの開発は、現在もなお継続的な取り組みです。長期的な安全性と有効性は、潜在的な副作用を慎重に考慮した上で、大規模なランダム化比較試験によって確立されなければなりません。さらに、食事、生活習慣、腸内細菌叢の複雑な相互作用により、腸内細菌叢の変化が心血管疾患の転帰に及ぼす具体的な影響を特定することは困難です。 |
| 最後に、腸内細菌叢の調節が心血管疾患の健康に及ぼす長期的な影響は、ほとんど解明されていません。短期的な研究では有望な結果が示されていますが、介入の効果の持続性や、心血管疾患の発症、進行、予後への影響を評価するには、長期的な研究が必要です。これらの課題に取り組むことは、心血管疾患の予防と治療における腸内細菌叢に基づく戦略の可能性を最大限に引き出す上で極めて重要となります。図3に、主な課題をまとめました。 |
 |
| 図3. 腸内細菌叢と心血管疾患に関する研究における主要な課題 |
| 9.今後の展望 |
| 腸内細菌叢が心血管疾患の健康に果たす役割についての理解を深めるには、最新技術と革新的な治療戦略を統合した多面的なアプローチが必要です。精密医療は、腸内細菌叢のプロファイリングを臨床データやマルチオミクスデータと組み合わせることで中心的な役割を果たし、心血管疾患の予防と管理のための個別化された介入を可能にするでしょう。 |
| 機能性と標的送達メカニズムを強化した次世代プロバイオティクスの開発は、治療効果の向上に有望である。特定の代謝産物を産生したり、標的となる腸管部位に定着したりできる遺伝子操作されたプロバイオティクスは、より精密な介入を可能にするかもしれない。同様に、心血管疾患への応用に向けて糞便微生物移植プロトコルを最適化する必要があり、有益な微生物群集の特定、安全性の確保、ドナーの選択と便処理の標準化に重点を置く必要がある。 |
| 有害な微生物代謝産物を標的とする薬理学的戦略や、腸内細菌叢の構成を調節する戦略は、有望な新たな道筋となる。新規の薬剤標的と選択的阻害剤を特定することで、ディスバイオシスに伴う心血管系への悪影響を軽減できる可能性がある。マルチオミクスデータと計算モデリングを統合したシステム生物学的手法は、腸内細菌叢、宿主代謝、および心血管系間の複雑な相互作用を解明し、最終的に重要な治療経路の特定を促進する上で極めて重要となるだろう。 |
| これらの進歩を臨床現場に活かすためには、腸内細菌叢を調節する介入の安全性と有効性を評価するための大規模なランダム化比較試験が不可欠です。腸と心臓の相互作用に関するさらなる研究は、特に血圧調節、炎症、その他の心血管系プロセスに関連する根本的なメカニズムと新たな治療標的を解明する上で極めて重要となるでしょう。 |
| 最後に、健康な腸内細菌叢を促進するための幼少期の介入に焦点を当てた予防的アプローチは、長期的な心血管疾患の健康に大きな影響を与える可能性があります。心血管疾患の発症における腸内細菌叢の役割を調査し、幼少期から腸内環境を最適化するための戦略を特定することは、後の人生における心血管疾患リスクを低減するための重要な一歩となるでしょう。 |
| 10.結論 |
| 腸内細菌叢はもはや単なる共生生態系としてではなく、心血管疾患の病態を左右する修飾可能な因子として捉えられている。「腸-心軸」は、保護的な短鎖脂肪酸と、トリメチルアミンNオキサイドやリポ多糖などの動脈硬化促進性メディエーターとのバランスといった、明確な分子経路を介して機能する。これらの微生物シグナルは、動脈硬化、高血圧、不整脈の発症機序に不可欠であり、重要な治療領域を切り開くものである。 |
| しかし、これらのメカニズムに関する知見を臨床応用につなげるには、大きな制約を克服する必要がある。現在のパラダイムは、ヒトの心血管生理やマイクロバイオームの複雑さを完全に再現できないマウスモデルに大きく依存している。今後の研究では、(1)再現性を確保するための「ディスバイオシス」の定義の標準化、(2)横断的関連研究から因果関係を確立できる縦断的介入ヒト試験への移行、(3)個体間のばらつきを考慮するためのマルチオミクスの適用を優先する必要がある。 |
| 最終的に、心血管疾患医療の進化は、微生物生態系を機能的な臓器として扱うことを必要とするでしょう。マイクロバイオームプロファイリングをリスク層別化に統合することで、腸と心臓の軸を標的とした次世代プロバイオティクスから選択的代謝阻害剤に至るまで、長期的な心血管疾患の転帰を改善する精密医療へと前進できる可能性があります。今後、精密医療、次世代プロバイオティクス、およびシステム生物学アプローチの進歩は、腸-心臓軸に関する理解を深める可能性を秘めています。これらの知見を臨床診療に統合することで、研究者と臨床医は、心血管疾患の転帰と全体的な健康を改善する、より効果的で個別化された介入を開発できます。この分野が進化し続けるにつれて、腸内細菌叢の治療の可能性を最大限に引き出すことは、心血管疾患と闘い、長期的な健康を向上させる革新的な戦略への道を開く可能性があります。 |
| 参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
| この文献は、Cardiology ResearchandPractice, 2026;2026:9920016に掲載されたThe Gut–Heart Axis: A Comprehensive Review of Microbiota's Role in Cardiovascular Health and Disease and Emerging Therapeutic Strategies.を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |