
Carolina Beatrice D'Anniballe De Salles et al., |
要約 |
| アルツハイマー病、パーキンソン病、軽度認知障害などの加齢に伴う神経変性疾患は、世界的な健康課題として深刻化している。現在の治療薬は症状緩和にとどまり、疾患修飾効果は乏しい。近年の研究により、腸-脳軸と食生活が加齢に伴う認知機能低下に大きく関与していることが示唆されている。本レビューではまず、腸内細菌叢の異常と神経変性のメカニズム的関連性に焦点を当てた。さらに、プロバイオティクスや栄養補助食品が高齢者の脳機能改善に有効であることを示す前臨床研究および臨床研究について考察した。また、ランダム化比較試験およびメタアナリシスでは、プロバイオティクスや特定の栄養補助食品が、軽度ながらも一貫した認知機能改善効果をもたらすことが示唆されており、特に疾患発症初期段階で治療を受けた患者においてその効果が顕著である。これらの効果は、特定の標的アプローチによるものではなく、腸内細菌叢、免疫シグナル伝達、神経保護経路の複合的な影響によるものと考えられる。したがって、今回のレビューでは、プロバイオティクスや栄養補助食品が加齢に伴う神経変性に対する効果的かつ安全な治療法となる可能性を示唆する報告に焦点を当てている。 |
| 目次(クリックして記事にアクセスできます) |
| 1. はじめに |
| 2. 方法 |
| 3. メカニズム的インターフェース:加齢、腸内細菌叢異常、および神経変性 |
| 4.様々な神経変性疾患に基づく介入 |
| 4.1. アルツハイマー病(AD) |
| 4.1.1. 前臨床的証拠 |
| 4.1.2. 臨床的エビデンス |
| 4.2. パーキンソン病(PD) |
| 4.2.1. 前臨床的証拠 |
| 4.2.2. 臨床的エビデンス |
| 4.3. 軽度認知障害(MCI)および加齢性認知機能低下(ARCD) |
| 4.3.1. 前臨床的証拠 |
| 4.3.2. 臨床的エビデンス |
| 5. 限界 |
| 6. 課題と今後の方向性 |
| 7. 結論 |
| 本文 |
| 1.はじめに |
| アルツハイマー病(AD)、パーキンソン病(PD)、軽度認知障害(MCI)などの神経変性疾患による世界的な健康危機は、高齢者の罹患率の上昇に伴い深刻化しています[1,2,3]。予測によると、世界の認知症患者数は2050年までに1億3100万人に達し、アルツハイマー病は診断された認知症症例全体の60~80%を占め続けるとされています[4,5]。パーキンソン病の発症者数も増加の一途をたどっており、患者とその介護者、そして医療機関にとって、身体的、精神的、経済的に大きな負担となっています[6,7]。現在利用可能なこれらの疾患の治療法は限られており、主に症状管理に重点を置いています[8]。さらに、これらの治療法は疾患の進行を止めることはできず、しばしば副作用を伴います。したがって、疾患修飾効果があり、副作用が最小限に抑えられる代替治療戦略の開発が求められています[5,9]。 |
| 近年、いくつかの前臨床および臨床研究において、神経変性疾患の管理におけるプロバイオティクスおよび栄養補助食品の有効性が示されています[10,11,12,,13]。そこで、本レビューでは、神経変性疾患の治療戦略としてプロバイオティクスおよび栄養補助食品が有効であることを示す証拠を詳しく解説しました。 |
| 腸内細菌叢は、加齢に伴い有益な共生細菌が失われ、病原性細菌が増殖するため、ディスバイオシス(腸内細菌叢異常)を引き起こす一連の変化を経る[14]。その結果、腸管透過性、酸化ストレス、炎症が増加し、一般的に炎症性老化として知られている[10,15,16,17]。腸管透過性の増加は、病原性共生細菌と炎症性メディエーターの全身循環への移行を促進する。循環する炎症性サイトカインはその後脳に到達し、神経炎症、アミロイドβ(Aβ)およびタウ病理を促進する可能性がある[7,18,19,20,21]。 |
| さらに、腸内細菌叢と食事の変化は新たな炎症状態を引き起こし、それが神経免疫シグナル伝達、シナプス可塑性、代謝機能を変化させます[15,18,22,23]。微生物群集構造と短鎖脂肪酸(SCFA)およびトリプトファン由来インドールの代謝出力の両方に影響を与える微生物の変化は、ミクログリアの活性化につながり、神経伝達物質の安定性と血液-脳関門(BBB)機能に影響を与えます[21,24,25,26]。これらの相互作用は、加齢に伴う認知機能の維持における腸-脳軸の中心的な役割を強調しています。 |
| 研究者たちは現在、栄養介入が加齢に伴う精神機能の維持に役立つ重要な保護措置として機能することを理解している[27,28]。例えば、プロバイオティクスは短鎖脂肪酸などの神経活性代謝物を生成することで腸の完全性と免疫応答を回復させる[16,19,20]。したがって、加齢に伴う認知機能低下の予防には、腸内細菌叢の異常と栄養欠乏を調査する必要がある。これらの状態は、神経変性を遅らせたり予防したりするための効果的で手頃な方法を提供するからである。研究証拠は、プロバイオティクスと栄養補助食品が、医療従事者が脳細胞を保護しながら既存の薬をサポートするために使用できる安全な治療オプションであることを示している[19,28,29]。 |
| したがって、このレビューでは、入手可能な前臨床および臨床の証拠を統合して、アルツハイマー病、パーキンソン病、および軽度認知障害におけるプロバイオティクスと栄養補助食品の治療可能性を評価します。これらの介入が、微生物組成、免疫機能、および栄養状態を調節することによって、高齢者の脳の健康をどのように総合的にサポートするかを強調します(図1)。図1は、腸内マイクロバイオームの加齢に伴う変化と、腸-全身-脳軸を介して媒介されるプロバイオティクスおよび栄養介入の神経保護効果との間の重要なつながりを示しています。 |
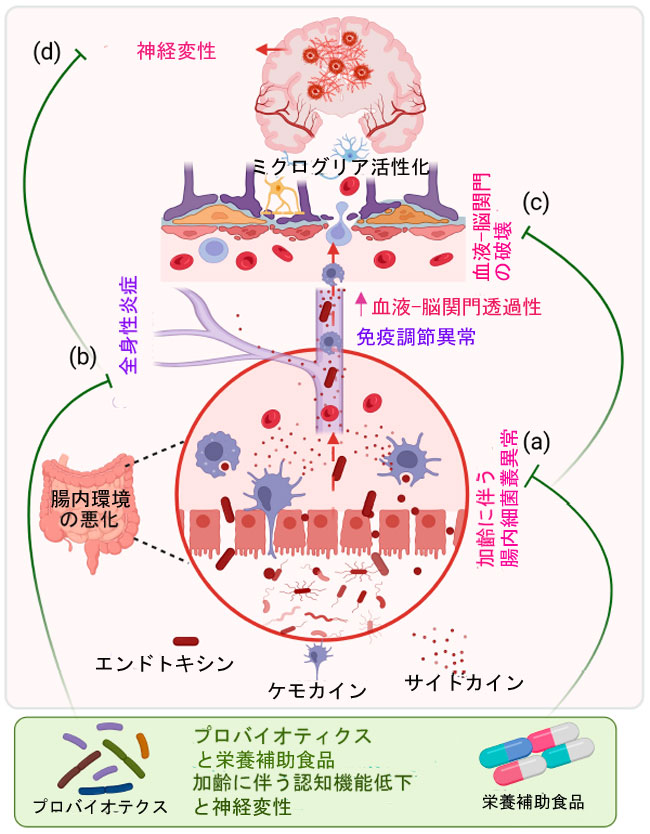 |
図1. 不健康な加齢に伴う腸-脳軸の機能障害と栄養介入によるその調節。 不健康な加齢中、微生物多様性の低下は腸内細菌叢の異常(a)を促進し、腸管透過性の増加とエンドトキシンの移行を引き起こします。これにより、循環サイトカインとケモカインの上昇を特徴とする全身性炎症が引き起こされます(b)。持続的な炎症シグナル伝達は血液-脳関門の完全性を損ない、グリア細胞の活性化を誘導し(c)、最終的に神経変性と認知機能低下(d)につながります。プロバイオティクスと栄養補助食品は腸内細菌叢の構成を調節し、加齢に伴う腸内細菌叢の異常、全身性炎症、血液脳関門透過性、および神経変性リスクを軽減します。 |
| 2. 方法 |
| 腸-脳-免疫軸に関連するメカニズム研究、動物モデル、ヒト臨床試験など、多様なエビデンスを統合的に評価するために、ナラティブアプローチを採用した。さらに、臨床効果と認知機能に関するアウトカムを考察する際には、ヒトを対象としたランダム化比較試験を優先した。関連文献は、PubMed/MEDLINE、Scopus、Web of Scienceの検索によって特定し、Google Scholarや主要なレビュー論文および影響力のある原著論文の参考文献リストの手動スクリーニングによって追加の研究を収集した。査読済みで英語で出版され、加齢、アルツハイマー病、パーキンソン病、軽度認知障害における認知機能、神経変性、神経炎症、または腸-脳軸メカニズムとの関連でプロバイオティクスおよび/または栄養補助食品を検討した研究を対象とした。 |
| 3. メカニズム的インターフェース:加齢、腸内細菌叢異常、および神経変性 |
| 腸-脳軸(GBA)は、中枢神経系(CNS)と腸管神経系(ENS)、免疫シグナル、および微生物代謝産物を結びつける双方向のコミュニケーションネットワークです[30,31]。迷走神経を介した神経経路は、腸と脳間の主要なコミュニケーション経路となっています[32]。加齢に伴う腸管神経系の変性および迷走神経緊張の低下は、シグナル伝達を阻害し、消化管運動および炎症の中枢制御に影響を与える可能性があります[10]。さらに、腸内細菌叢異常は、IL-6やTNF-αなどの炎症性サイトカインの血中濃度を上昇させる免疫応答を刺激します。これらのサイトカインは脳内のミクログリアを活性化し、アルツハイマー病およびパーキンソン病における神経炎症に寄与します[16,33]。研究によると、免疫調節異常に加えて、視床下部-下垂体-副腎(HPA)軸も加齢に伴って調節異常を起こす[34,35]。視床下部-下垂体-副腎軸の長期活性化はコルチゾール放出の増加をもたらし、神経炎症を悪化させ、アルツハイマー病やパーキンソン病などの疾患における神経変性に対する脆弱性を高める[35]。さらに、代謝調節異常は、腸機能障害と神経変性疾患の進行を結びつけるもう1つの重要な経路である[36]。さらに、微生物代謝と宿主エネルギー恒常性の加齢に伴う変化は、短鎖脂肪酸産生、ミトコンドリア機能、グルコースおよび脂質代謝を損ない、酸化ストレスの増加と持続的な神経炎症につながる[22,37,38]。これらの代謝障害は、神経細胞のエネルギー供給を損ない、血液-脳関門(BBB)の完全性を破壊し、アルツハイマー病および パーキンソン病におけるタンパク質ミスフォールディングとシナプス機能障害を悪化させます。加齢は短鎖脂肪酸の産生を減少させ、トリプトファン代謝を変化させ、セロトニンレベルの低下とキノリン酸などの神経毒性代謝産物の産生増加につながります [7]。したがって、腸内細菌叢の異常、炎症性老化、および腸-脳軸の変化は、脳損傷と認知機能低下を加速させます。したがって、プロバイオティクスと栄養補助食品を使用することで、これらの関連する経路のバランスを回復できる可能性があります。さらに、研究では、ビフィドバクテリウムやフェカリバクテリウムなどの健康増進共生細菌の減少と、潜在的に病原性のある分類群 (腸内細菌科) の増加が示されています [10,16]。さらに、ビフィドバクテリウムのレベルが低い高齢者は、軽度認知障害を示す可能性が高いことが実証されています [39]。さらに、認知症患者では非認知症患者よりもフィルミクテス/バクテロイデス(F/B)比が高かった[39]。他の研究では、アルツハイマー病患者では抗炎症性メディエーターの減少と炎症促進性グループの増加を特徴とする異なる微生物シグネチャーが報告されている[40]。これらのデータは、腸内細菌叢の構成がマーカーとして機能し、認知老化に影響を与えるという仮説を裏付けている。これらの戦略を総合すると、加齢に伴うディスバイオシスの悪影響に対抗するのに役立つ可能性がある。 |
| プロバイオティクスや栄養補助食品で腸-脳軸を標的にすることは、加齢に伴う神経変性を軽減する有望な方法です。プロバイオティクスは、微生物の多様性を改善し、有害な細菌の増殖を遅らせ、抗炎症作用と神経保護作用を持つ短鎖脂肪酸を生成することで、健康な腸を回復するのに役立ちます[14,16,19]。FAO/WHOの定義によれば、プロバイオティクスは、適切な量を摂取すると宿主に健康上の利益をもたらす生きた微生物です[41]。最も研究されている属は、ラクトバチルス属(例:L.アシドフィルス、L.プランタルム、L.カゼイ)とビフィドバクテリウム属(例:B.ロンガム、B.ブレーベ、B.ビフィダム)です[42]。しかし、ストレプトコッカス・サ-モフィルス、バチルス・ズブチルス、クロストリジューム・ブチリカム、エシェリシャ・コリ・ニッスル1917などの他の菌株も治療効果について検討されている[16,19,43]。これらの菌株は消化管内で生存し、腸細胞に付着し、宿主の免疫と代謝に影響を与えることができる。これらのよく知られたタイプに加えて、アッカーマンシア・ムシニフィラとフェカリバクテリウム・プラウスニッツィイなどの新しいプロバイオティクスが、炎症への影響や腸の健康をサポートする方法に関して注目を集めている[41,44]。これらのプロバイオティクスは、宿主の免疫、代謝、セロトニンやγ-アミノ酪酸などの神経伝達物質の産生を調節し、それによって認知と気分に影響を与える[45]。ラクトバチルスとビフィドバクテリウムは、腸内細菌叢のバランスを整え、セロトニンやγ-アミノ酪酸などの気分調節や認知機能向上に関わる神経伝達物質の産生を促進します[16,45]。さらに、プロバイオティクスは血液-脳関門の完全性を改善します。これにより、有害なサイトカインや毒素の中枢神経系への侵入が減少します[46]。臨床研究と前臨床研究の両方で、全身性炎症の軽減、神経栄養因子の増加、認知機能の向上といった効果が確認されています[19,29]。 |
| さらに、加齢に伴い、循環系に入る微生物由来の代謝産物も、腸の状態と全身および脳の生理機能を結びつける重要なメッセンジャーとして認識されています。これらの物質の中には、食物繊維の発酵中に生成される短鎖脂肪酸(酢酸、プロピオン酸、酪酸)やトリプトファン由来のインドールがあります。短鎖脂肪酸は免疫トーンを変化させ、上皮細胞と血液-脳関門のタイトジャンクションを強化し、脳に到達してミクログリアの状態に影響を与えることができます[24,47]。神経変性モデルでは、プロバイオティクスまたは複数株のサプリメントは循環中の短鎖脂肪酸を増加させ、末梢サイトカインの減少と関連しています[18]。インドール誘導体、特にインドール-3-プロピオン酸は、アリール炭化水素受容体シグナル伝達を介して抗酸化作用を発揮し、アストロサイトとミクログリアの炎症を抑制し、それによって血液-脳関門の完全性を保護し、認知機能低下に関連する神経炎症カスケードを軽減します[25,26,48,49]。 |
| さらに、短鎖脂肪酸は末梢免疫恒常性および免疫代謝の重要な調節因子です。酪酸とプロピオン酸は、Foxp3遺伝子座でのヒストン脱アセチル化酵素阻害を介して制御性T細胞(Treg)の分化を促進し、免疫寛容を促進し、炎症性老化を軽減します[47,50,51]。短鎖脂肪酸は恒常性条件下で制御性T細胞の増殖をサポートする一方で、免疫活性化中にエフェクターT細胞の代謝とサイトカイン産生も促進し、その状況依存的な免疫調節的役割を強調しています[52]。プロバイオティクス由来の代謝産物は、Th17応答を抑制し、全身のIL-6およびTNF-αレベルを低下させることにより、免疫バランスにさらに貢献します[19,51,53]。Treg/Th17バランスは加齢において重要であり、慢性的な低度炎症(炎症性老化)は神経変性のリスクを高める可能性があります[15]。 |
| 同時に、プレバイオティクス、ポリフェノール、食物繊維などの栄養補助食品は、有益な細菌に栄養を与え、短鎖脂肪酸の産生を促進し、腸と脳のつながりに影響を与えることができます [28]。さらに、ポリフェノールが豊富な食事は、腸内細菌叢をより健康的なプロファイルに変化させ、酸化ストレスも低下させることが示されています [54]。スーベネイドなどのマルチ栄養素製剤の使用も臨床試験で研究されています。これらの試験では、アルツハイマー病患者の記憶パフォーマンスにわずかな改善が見られました [55]。オメガ 3 多価不飽和脂肪酸 (PUFA)、ビタミン B 複合体、ビタミン D、ビタミン E、ポリフェノール、プレバイオティクスなどの栄養補助食品は、抗炎症、抗酸化、腸内細菌叢調節メカニズムを介して神経保護をサポートします [27,28,47]。 オメガ 3 多価不飽和脂肪酸、特にドコサヘキサエン酸(DHA)とエイコサテトラエン酸(EPA)は神経細胞に豊富に存在し、シナプスの柔軟性をサポートし、神経炎症を軽減します[28]。これらは神経細胞膜に入り込み、シナプス可塑性の維持を助け、ミクログリアの過活動を減少させます[28]。ポリフェノールは、フラボノイド(ベリー、茶、ココア由来)やクルクミンなどの植物由来化合物で、抗酸化作用を持ち、細胞内シグナル伝達経路(MAPK、NF-κBなど)を調節し、腸内細菌叢の構成を変化させます[28]。プレバイオティクスは、消化されない食物繊維(イヌリン、フラクトオリゴ糖など)で、有益な細菌の増殖と活動を選択的に刺激し、短鎖脂肪酸の産生と腸-脳軸機能を促進します[10]。臨床研究およびメカニズム研究によると、ビタミンB群は認知機能低下の既知のリスク因子である血漿ホモシステインを減少させ、神経保護をサポートすることが示されています[56]。オメガ3脂肪酸は炎症を軽減するだけでなく、海馬のシナプス形成と神経新生も促進します[57]。ポリフェノールの中では、レスベラトロールが高齢者の海馬の機能的結合と記憶を改善することが実証されています[58]。プレバイオティクス補給は、短鎖脂肪酸レベルを高めることで、ミクログリアの成熟と機能に役割を果たし、マイクロバイオームと神経保護をさらに結びつけています[24]。これらの介入は総合的に相乗的に作用し、加齢に伴う腸管バリアの完全性、免疫バランス、および認知回復力をサポートします。 |
| 栄養補助食品は免疫および代謝シグナル伝達も形成し、ビタミンDは制御性T細胞の分極を促進し、Th17の活性を抑制します[59,60,61]。しかし、オメガ3 多価不飽和脂肪酸は、炎症を積極的に解消し、マクロファージのエフェロサイトーシスを強化し、ミクログリアの活性化を減少させる特殊なプロレゾルビンメディエーター(SPM)に変換されます[62,63,64]。プロレゾルビンメディエーターは炎症を積極的に解消し、酸化ストレスを減少させ、デブリの貪食を刺激します[64]。臨床研究では、オメガ3の状態が高いほど、高齢者の全身性炎症が軽減され、認知機能が向上することが示されています[65,66]。したがって、これらの介入は、抗酸化防御の強化、神経伝達物質系の調節、および神経栄養因子のサポートを通じて神経保護を促進します[19,28]。このように、食事療法と微生物療法は、既存の治療法を補完し、加齢に伴う神経変性疾患の進行を遅らせる可能性のある、低コストで利用しやすい補助手段となります。プロバイオティクスと標的栄養介入を組み合わせることで、バリア機能の完全性が強化され、サイトカインプロファイルが調節され、酸化還元バランスが改善され、ミクログリアの恒常性が維持され、炎症性老化が軽減され、加齢に伴う認知機能低下のリスクが低減されます[29,54,67]。これらの知見は、プロバイオティクスと標的サプリメントによる腸内細菌叢の調節が、高齢者の炎症性老化を軽減し、認知機能の健康を維持するのに役立つという、多領域アプローチを支持しています。 |
| 4.様々な神経変性疾患に基づく介入 |
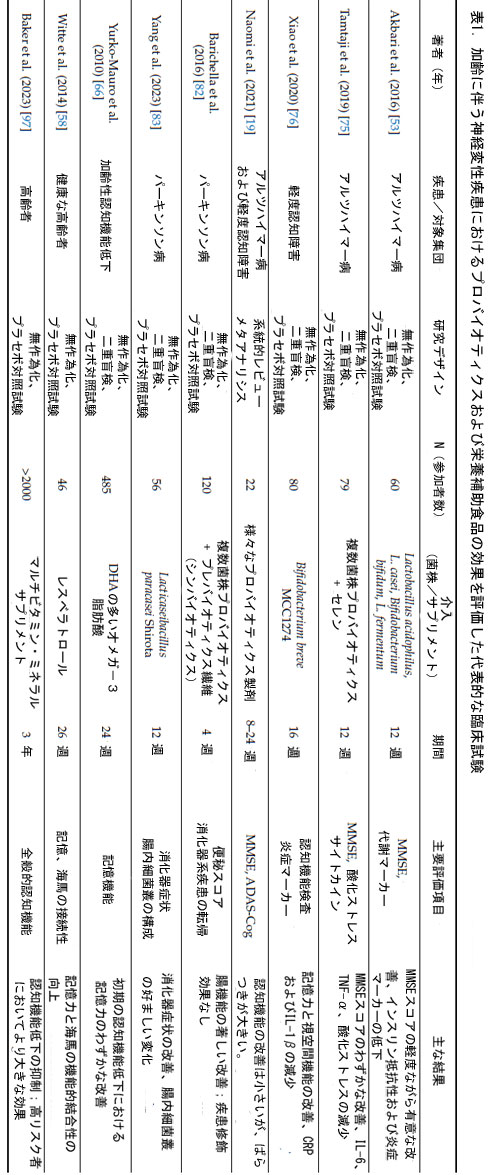
| 図2は、プロバイオティクスと栄養補助食品による介入を比較した概要を示しています。アルツハイマー病、パーキンソン病、軽度認知障害に関連する作用機序、バイオマーカー、臨床転帰を詳細に示しています。さらに、表1は、加齢に伴う神経変性疾患におけるプロバイオティクスと栄養補助食品の効果を評価した臨床試験を示しています。 |
 |
| 図2. アルツハイマー病、パーキンソン病、軽度認知障害におけるプロバイオティクスおよび栄養補助食品介入の概要。 これらの疾患全体を通して、プロバイオティクスおよび特定のサプリメントは、腸内細菌叢、炎症性および代謝性バイオマーカー、神経保護経路の調節と関連している。矢印↑は増加、↓は減少を表す。 |
| 4.1. アルツハイマー病(AD) |
| アルツハイマー病は、神経病理学的に細胞外アミロイドβ(Aβ)沈着、タウタンパク質の過剰リン酸化と神経原線維変化の形成、シナプスおよび神経細胞の喪失、酸化ストレス、慢性神経炎症を特徴とする疾患である[68,69,70]。これらの特徴的なプロセスは、全身性代謝機能障害、免疫老化、腸内細菌叢の異常によって調節されるという証拠が増えつつある。 |
| 4.1.1. 前臨床的証拠 |
| 前臨床研究では、腸内細菌叢を標的とした栄養介入がアルツハイマー病関連病理を軽減できることが一貫して示されています。3xTg-アルツハイマー病マウスでは、ラクトバチルス・ プランタルムKY1032とL. クルバタスHY7601の補給により、ミクログリアの活性化が抑制され、海馬ニューロンの完全性が維持され、空間記憶が改善されました[29]。タウオパチーモデルでは、プロバイオティクスの投与により神経炎症が軽減され、グリコーゲンシンターゼキナーゼ-3β(GSK-3β)活性が阻害され、タウタンパク質の過リン酸化が抑制され、認知機能が改善しました[46]。これらの効果は、血液-脳関門の完全性を高め、脳由来神経栄養因子(BDNF)などの神経栄養因子の発現を促進する循環短鎖脂肪酸の増加と関連付けられています[16,24,45,51]。プロバイオティクス以外にも、食事由来の生理活性物質が相乗効果を発揮することが示されています。レスベラトロールやクルクミンなどのポリフェノールは、APP/PS1マウスモデルにおいてアミロイド蓄積、酸化ストレス、神経炎症を軽減しました[71,72]。一方、オメガ3脂肪酸はシナプスの回復力を高め、脳由来神経栄養因子の発現を増加させました[73,74]。これらの前臨床研究結果は、初期のアルツハイマー病様病態において、腸内細菌叢の調節と栄養戦略が疾患修飾効果を持つ可能性を示唆しています。 |
| 4.1.2. 臨床的エビデンス |
| 臨床研究は、プロバイオティクスおよび特定の栄養補助食品がアルツハイマー病の初期段階において測定可能な効果を発揮するという、複数のエビデンスを統合的に示している。画期的な無作為化比較試験において、Akbariらは、ラクトバチルス・アシドフィルス、ラクトバチルス・カゼイ、ビフィドバクテリウム・ビフィダム、およびラクトバチルス・フェルメンタムを含むプロバイオティクスミルクを12週間摂取することで、アルツハイマー病患者のミニメンタルステート検査(MMSE)スコアが有意に改善したと報告している[53]。同様に、Tamtajiらは、プロバイオティクスとセレンの併用摂取がミニメンタルステート検査スコアの改善、抗酸化酵素活性の向上、および炎症性サイトカイン(IL-6、TNF-α)の減少をもたらすことを実証した[75]。軽度認知障害のある人では、ビフィドバクテリウム・ブレーベMCC1274の補給により、C反応性タンパク質とIL-1βレベルが低下しながら、記憶と視空間パフォーマンスが改善しました[76]。栄養介入も同様の効果を示しています。オメガ3脂肪酸の補給は、軽度認知障害およびアルツハイマー病の人の認知機能を改善しました[65,66]。さらに、ビタミンDの補給は、制御性T細胞の誘導とTh17応答の抑制による免疫分極の改善と関連付けられています[61]。しかし、ビタミンB群(B6、B12、葉酸)は、海馬萎縮と認知機能低下に関連するホモシステイン関連神経毒性を軽減します[56]。レスベラトロールなどのポリフェノールは、高齢者の記憶パフォーマンスと海馬の機能的結合を改善しました[58]。さらに、オメガ3脂肪酸、ウリジン、コリン、補因子を組み合わせたスーベネイドなどの多栄養素製剤は、前駆期および軽度のアルツハイマー病患者の記憶能力を一貫して改善し、進行期では効果が減弱しました[55]。 |
| メタ分析は、臨床的エビデンス基盤をさらに強化する。Naomi らは、23 のランダム化比較試験を分析し、ミニメンタルステート検査スコアの小さながらも有意な改善と、インスリン代謝および酸化ストレス バイオマーカーへの好ましい効果を報告した [19]。さらに、Tripathi らは、認知機能の改善は記憶領域で最も顕著であり、介入期間が長く、複数の菌株を含むプロバイオティクス製剤の場合にその効果が大きいことを観察した [77]。Xiao らによる包括的なメタ分析では、ミニメンタルステート検査および ADAS-Cog スコアの再現性のある改善、ならびにインスリン抵抗性の低下や脂質プロファイルの改善などの心血管代謝上の利点が確認され、プロバイオティクスは低リスクの補助的介入であると結論付けた [78]。追加の統合分析では、腸内細菌叢の回復、全身性炎症の軽減、グルコース代謝の改善、および酸化ストレスの軽減が、臨床的利益の根底にある収束メカニズムであると強調した [79,80]。 |
| 要約すると、前臨床研究と臨床研究の両方からの証拠は、プロバイオティクスと特定の栄養補助食品がアルツハイマー病に対して、控えめながらも再現性のある効果を発揮し、特に前駆期および疾患初期段階で最も強い効果が観察されることを示している。これらの介入は、全身性炎症、代謝調節、およびアルツハイマー病の発症機序に関連する微生物叢依存性シグナル伝達経路を調節することにより、既存の治療法を補完する補助療法として最も効果的であると考えられる。 |
| 4.2. パーキンソン病(PD) |
| パーキンソン病は、黒質におけるドーパミン作動性ニューロンの進行性喪失を特徴とする疾患である[81]。この神経変性により、震え、硬直、運動緩慢といった典型的な運動症状が現れる。パーキンソン病の腸管仮説を支持する証拠が増えつつあり、α-シヌクレイン病理が腸管で始まる可能性が示唆されている。腸管神経系から、この病理は迷走神経を介して脳に広がると考えられている[22,82,83]。 |
| 4.2.1. 前臨床的証拠 |
| パーキンソン病の動物モデルは、腸内細菌叢を標的とした介入や栄養介入のメカニズム的根拠を提供している。ロテノン誘発パーキンソン病ラットモデルでは、ラクトバチルス・プランタルムの補給により運動機能が改善し、酸化ストレスと神経損傷が有意に減少した[84]。さらに、XieとPrasadは、ラクチカゼイバチルス・ラムノサスHA-114による治療が、6-OHDA誘発パーキンソン病様症状を示すげっ歯類において、海馬依存性の認知機能障害を選択的に改善することを実証した[85]。また、Hsiehらは、プロバイオティクスの長期投与が、MitoPark パーキンソン病マウスにおいてドーパミンニューロンを保護し、運動機能障害の悪化を軽減することを示した[86]。同様に、オメガ3脂肪酸は、MPTP誘発マウスモデルにおいて、神経細胞膜の安定化と神経炎症の解消を介して、黒質線条体変性を抑制し、運動機能を改善した[87]。ビタミンDは、ドーパミン作動性ニューロンのアポトーシスを減少させ、炎症シグナル伝達を抑制することによってパーキンソン病モデルにおいて神経保護効果を示し[88]、線条体ドーパミン放出と黒質ドーパミン含有量を増加させた[89]。さらに、Prajapatiらは、補酵素Q10の投与がミトコンドリア機能を促進し、げっ歯類における6-OHDA誘発性ドーパミン作動性毒性を予防することを実証した[81]。総合すると、前臨床研究は、プロバイオティクスと栄養補助食品がパーキンソン病関連モデルにおいてα-シヌクレイン関連病理、酸化ストレス、ミトコンドリア機能障害、およびドーパミン作動性完全性を調節できることを示している。 |
| 4.2.2. 臨床的エビデンス |
| 臨床的エビデンスは、パーキンソン病に伴う消化器機能障害、特に便秘の管理においてプロバイオティクスの使用を最も強く支持しています。初期の臨床研究では、ラクトバチルス・カゼイ・シロタを含む発酵乳が、便秘を伴うパーキンソン病患者の排便回数を有意に増加させ、便の硬さを改善することが示されました[90]。これらの知見は、その後、より大規模なランダム化比較試験で確認されました。BarichellaらによるクラスI試験では、シンバイオティクス治療(複数の菌株からなるプロバイオティクスとプレバイオティクス繊維の組み合わせ)を4週間行うことで、プラセボと比較して完全な排便回数が有意に増加し、便秘の重症度が改善することが示されました[82]。さらに最近の試験では、ラクトバチルス・パラカゼイ・シロタの補給が消化器症状を緩和するだけでなく、腸内細菌叢の構成を短鎖脂肪酸産生菌の増加へと好ましい方向に変化させることも示されました[83]。さらに、系統的レビューとメタ分析では、プロバイオティクスはパーキンソン病の消化器系の転帰を確実に改善し、運動症状と非運動症状に対する効果は控えめで変動があり、研究の異質性とサンプルサイズの小ささによって部分的に制限されているという結論が一貫して出ています[19]。 |
| 栄養補助食品は主に全身および非運動効果について評価されてきました。オメガ3脂肪酸の補給は、ランダム化比較試験で実証されているように、パーキンソン病患者の気分と生活の質をわずかに改善することが示されています[91]。二重盲検プラセボ対照試験では、オメガ3とビタミンEの組み合わせにより、統一パーキンソン病評価尺度(UPDRS)の合計スコアが改善し、抗酸化能が強化され(総抗酸化能とグルタチオンの増加、マロンジアルデヒドの減少)、全身性炎症(hs-CRP)が減少しました[92]。ビタミンDの補給は、姿勢の安定性の改善と転倒リスクの減少に関連しており、特定のビタミンD受容体(VDR)遺伝子型を持つパーキンソン病患者で最大の効果が観察されています[93]。対照的に、初期の有望性にもかかわらず、コエンザイムQ10を評価する大規模な第III相試験(QE3試験)は、疾患修飾効果を実証できず、QE3試験の否定的な結果がパーキンソン病に対するこの化合物のさらなる開発を中止させた[9,94]。 |
| 要約すると、臨床および前臨床の証拠は、プロバイオティクスがパーキンソン病の消化器症状に対して一貫性のある再現可能な効果をもたらすことを示しており、これはこの疾患における微生物叢標的療法の最も強力な応用例と言える。オメガ3脂肪酸やビタミンDなどの栄養補助食品は、気分、酸化ストレス、転倒予防など、非運動症状や全身症状の選択において補助的な効果をもたらす可能性があるが、これまでのところ、パーキンソン病の進行に対する明確な疾患修飾効果を示した介入はない。 |
| 4.3. 軽度認知障害(MCI)および加齢性認知機能低下(ARCD) |
| 軽度認知障害は、正常な加齢と認知症の中間段階であり、年間約10~15%がアルツハイマー病に移行します。加齢性認知機能低下は、記憶力や実行機能における、より軽微で臨床症状を伴わない障害を指し、血管機能障害、微量栄養素欠乏、代謝異常、および腸内細菌叢の加齢に伴う変化と関連していることが多い。認知機能の連続体において比較的初期段階に位置することから、軽度認知障害と加齢性認知機能低下はともに、腸内細菌叢および栄養に基づく介入による予防および治療の可能性が高い段階と言えます。 |
| 4.3.1. 前臨床的証拠 |
| 加齢および認知機能障害モデルにおける前臨床研究は、マイクロバイオームを標的とした介入および栄養介入の強力なメカニズム的根拠を提供している。高齢げっ歯類へのプロバイオティクス投与は、海馬における脳由来神経栄養因子の発現を増強し、学習および記憶能力を向上させる。一方、短鎖脂肪酸などの微生物代謝産物は、免疫、エピジェネティクス、およびシナプス可塑性に関連する経路を調節する[18,51,52]。ブルーベリー、ブドウ、およびその他の植物由来のポリフェノールは、加齢モデルにおいて酸化ストレスを軽減し、神経細胞の回復力を促進する[71,72,95]。オメガ3脂肪酸は、樹状突起の完全性、シナプス可塑性、および認知の柔軟性をサポートする[73,74]。ビタミンB群は、海馬変性や血管機能障害の主な原因であるホモシステイン値を低下させることで神経保護効果を発揮する[56,88,96]。これらの動物実験は、腸内細菌叢の調節と標的を絞った栄養サポートが、加齢に伴うシナプス維持と認知機能回復力に関連する経路に収束することを示している。 |
| 4.3.2. 臨床的エビデンス |
| 軽度認知障害患者を対象とした臨床試験では、軽度ながら再現性のある認知機能改善効果が一貫して認められています。複数のランダム化比較試験では、プロバイオティクス補給後にミニメンタルステート検査スコア、言語学習、記憶領域の改善が報告されており、炎症マーカーおよび代謝マーカーの減少も伴っていました[77]。さらに、系統的レビューでは、プロバイオティクスは軽度認知障害患者の認知機能と気分に小さながらも一貫した効果をもたらし、その効果は菌株特異性、介入期間、ベースラインのリスクプロファイルによって左右されると結論付けられています[19]。ビタミンB群(B6、B12、葉酸)の補給は、軽度認知障害患者を対象とした磁気共鳴画像法(MRI)を用いた研究において、ホモシステイン値を低下させ、海馬萎縮を著しく遅らせることが示されています[56]。レスベラトロール、ココアフラバノール、ベリー由来化合物などのポリフェノールベースの介入は、小規模なランダム化比較試験で記憶力、実行機能、処理速度を改善することが示されています[54,58]。オメガ3のサプリメント、特にDHAが豊富な製剤は、主観的認知機能低下または軽度認知障害の高齢者の学習および記憶能力の改善と関連しています[65,66]。 |
| 軽度認知障害におけるプロバイオティクスの直接的な証拠は、ビフィドバクテリウム・ブレーベMCC1274の16週間の補給が即時記憶と視空間/構成能力を改善し、循環炎症マーカーを減少させたことを示す無作為化二重盲検プラセボ対照試験によってさらに裏付けられています[76]。これらの知見は、プロバイオティクス介入が軽度認知障害および初期の神経変性段階全体にわたって小さくても確実な認知上の利点をもたらすことを示すより広範なメタ分析と一致しています[19]。 |
| 加齢性認知機能低下および認知機能が正常な高齢者集団の臨床データは、これらの観察を裏付けています。加齢性認知機能低下の高齢者では、レスベラトロール補給により記憶力が向上し、海馬の機能的結合が強化され、グルコース代謝が最適化されました [58]。ココアフラバノールとベリー抽出物介入のレビューでは、実行機能と処理速度に一貫して利点があると報告されています [54]。しかし、オメガ 3 補給は、高齢者集団における記憶力と学習成果の改善と関連付けられています [66]。大規模な試験は、標的を絞った補給戦略をさらに支持しています。COSMOS-Mind 試験では、3 年間にわたる毎日のマルチビタミン・ミネラル補給により、全般的認知機能の低下が有意に遅くなり、特に心血管疾患のある参加者においてエピソード記憶と実行機能が改善しました [97]。地域在住の高齢者を対象としたプロバイオティクス試験では、精神的柔軟性、ストレス耐性、腸内細菌叢の構成の改善も報告されており、より広範な総合的研究により、言語学習、気分、実行機能に対する菌株および用量依存的な効果が裏付けられています[19,54,98]。機能的神経画像研究では、ココアフラバノールが歯状回機能とパターン分離記憶を選択的に強化し、食事による調節に対する海馬のサブ領域特異的な感受性を強調することがさらに実証されています[99]。 |
| 要約すると、前臨床および臨床研究の収束的な証拠は、プロバイオティクス、ビタミンB群、オメガ3脂肪酸、ポリフェノールが、軽度認知障害および加齢性認知機能低下において相補的かつ段階的な認知機能改善効果をもたらすことを示している。効果の大きさは控えめではあるものの、これらの介入は一貫して記憶力と実行機能を改善し、全身性炎症を軽減し、海馬の健全性を維持する。早期に開始し、長期にわたって継続することで、腸内細菌叢と栄養に基づく戦略は、軽度認知障害または加齢性認知機能低下から顕性認知症への進行を遅らせるのに役立つ可能性がある。 |
 |
| 5. 限界 |
| 有望な結果が見られるにもかかわらず、認知機能の老化におけるプロバイオティクスと栄養補助食品に関する現在の文献には、いくつかの重要な限界がある。ほとんどのランダム化臨床試験は検出力が不足しており、被験者数が少ない(通常30~120人)ため、統計的検出力と一般化可能性が制限される[53]。介入期間が短い(8~24週間)ため、長期的な認知機能の軌跡、疾患の進行、または軽度認知障害から認知症への移行の評価が制限される[58,75]。研究間の大きな異質性、特にプロバイオティクス株の組成、投与レジメン、投与形態、サプリメントの製剤および生物学的利用能における異質性は、研究間の比較とメタアナリシスによる統合をさらに複雑にし、標準化された臨床推奨事項を妨げている[16]。海馬萎縮率、持続的な生活の質の改善、または認知症の発症率など、臨床的に意義のある長期的なアウトカムを評価する試験はほとんどない。例えば、VITACOG試験では軽度認知障害患者におけるビタミンB群補給による脳萎縮の軽減が実証されたものの[96]、ほとんどの研究の追跡期間は6ヶ月以下であり、COSMOS-Mindのような大規模試験でさえ認知症の発症率を評価していない[97]。複数のランダム化試験とメタアナリシスでは統計的に有意な認知機能改善効果が報告されているが、効果の大きさは一般的に小さく、異質で、短期的であり、持続的または疾患修飾効果の証拠は限られているため、これらの介入は単独療法ではなく補助療法として検討されるべきである。最後に、腸内細菌叢の変化は一貫して神経変性疾患と関連付けられているが、ヒトのデータは主に相関関係を示しているため因果関係は不明であり、プロバイオティクスは一般的に忍容性が高いものの、免疫不全患者ではまれに菌血症や敗血症が報告されており、慎重な患者選択と安全性のモニタリングが必要であることを強調している。 |
| 6. 課題と今後の方向性 |
| マイクロバイオームと栄養に基づく介入を臨床現場に導入する際の大きな課題の一つは、菌株や栄養素に特化した推奨事項が必要であることです。ビフィドバクテリウム・ブレーベMCC1274やラクティカゼイバチルス・パラカゼイ・シロタなどの特定のプロバイオティクス菌株は、認知機能や消化器系への有益な効果を示していますが[76,83]、その効果は菌株、投与量、製剤、投与形態によって大きく異なります[19,77]。同様に、すべてのオメガ3脂肪酸やポリフェノールが同等の効果を示すわけではなく、DHAはEPAよりも一貫して記憶力向上効果を示し[66,73]、ココアフラバノールは実行機能や海馬記憶において領域特異的な改善をもたらします[99]。これらの知見は、腸内細菌叢のベースライン組成、日常的な食事、遺伝的背景など、宿主固有の要因を考慮した精密栄養フレームワークへと、広範な介入カテゴリーを超えて移行する必要性を強調しています。 パーキンソン病ではビタミンD受容体遺伝子型に基づくサプリメントへの反応の差異がすでに観察されており[93]、アルツハイマー病ではオメガ3脂肪酸によるリスク調節においてAPOE(訳者注:APOE(アポリポタンパクE)は、脂質(コレステロール)の運搬に関わるタンパク質で、特にアルツハイマー型認知症の主要な遺伝的リスク因子として知られています。3つの遺伝子型(ε2, ε3, ε4)があり、特にε4型を持つ人は認知症リスクが3〜12倍高まる一方、必ず発症するわけではなく、生活習慣でリスク軽減が可能です)遺伝子型に基づく反応の差異が観察されている[65]。マイクロバイオームシーケンス、メタボロミクス、バイオインフォマティクスの進歩により、個人を予測される反応者と非反応者に層別化することが可能になり、試験の異質性を低減し、翻訳精度を向上させることができるようになった[18,24]。新たなエビデンスは、パーキンソン病の便秘と生活の質を改善したシンバイオティクス[82]、より安定した薬理作用を提供する短鎖脂肪酸やインドール誘導体などのポストバイオティクス[25,26]、前駆期アルツハイマー病に効果を示したスーベネイドやLipiDiDietなどの多栄養素製剤[55,100]を含む、複合的かつ多面的な戦略を支持している。メタゲノミクス、メタボロミクス、プロテオミクス、免疫表現型解析、宿主ゲノミクスなどのマルチオミクスアプローチの統合は、神経変性に関与する微生物-代謝-免疫ネットワークをこれらのデータセットが捉えるため、メカニズムの解明と精密誘導介入設計に向けた重要なステップとなります [7,18,24,25,47,64]。システムレベルのバイオインフォマティクス、ネットワーク解析、機械学習モデルは、疾患の進行と治療反応性を予測する微生物-宿主シグネチャの特定に有望であることが示されています [78,97]。人工知能の応用により、マイクロバイオーム、食事、代謝、遺伝子、臨床結果にわたる複雑な非線形相互作用のモデリングが可能になり、最適な菌株選択、栄養素の組み合わせ、投与戦略、バイオマーカー強化試験設計が促進されます [18,24,78]。総合的に見て、マルチオミクス、計算モデリング、およびAI駆動型分析の統合は、再現性の向上、異質性の最小化、そしてマイクロバイオームベースおよび栄養介入を、加齢および神経変性疾患に対する臨床的に実行可能な個別化戦略へと発展させるために不可欠である。 |
| 7. 結論 |
| 近年の科学的発見により、プロバイオティクスや栄養補助食品が認知機能の老化や低下に対抗する上で大きな可能性を秘めていることを示す重要な前臨床および臨床データが得られています。前臨床モデルとヒトを対象とした研究の両方において、様々なプロバイオティクス株、オメガ3脂肪酸、ビタミンB群、ポリフェノールが、シナプス可塑性および回復力、神経炎症、代謝バランスに好影響を与えることが示されています。臨床レベルでは、これらのサプリメントは認知機能と健康状態の改善にわずかではあるものの意義のある効果をもたらし、臨床応用への可能性を示しています。アルツハイマー病、パーキンソン病、軽度認知障害を対象としたランダム化比較試験およびメタアナリシスによるエビデンスは最も進んでおり、これらの介入が、これらの疾患において一般的に用いられる認知機能評価指標(MMSE、ADAS-Cog、RBANS)に対して、再現性のある小さな効果を示すことが一貫して示されています。これらの研究には、認知機能に対する菌株および栄養素特異的な影響、宿主および臨床的特徴による調節、サンプルサイズが小さく期間が短いことによる他の環境への一般化可能性の制限が共通しており、これらのアプローチが疾患の経過や認知症への移行にどのような影響を与えるかを判断するために、大規模で多施設共同、十分な検出力を持つ、より長期の追跡調査試験が重要であることが強調されています。将来的には、腸-脳軸の操作と栄養欠乏が、加齢に伴う神経変性疾患や脳の老化に対する重要な補助治療標的として浮上する可能性があります。プレバイオティクスとプロバイオティクス、シンバイオティクス、ポストバイオティクスを、現在のエビデンスに基づく栄養素ベースの介入(マルチビタミン、オメガ3、ビタミンB)のアプローチと組み合わせたマルチモーダル介入の開発は、安全で拡張性があり、個別に標的を絞ることができる可能性があります。 |
| 参考文献(本文中の文献No.は原論文の文献No.と一致していますので、下記の論文名をクリックして、原論文に記載されている文献を参考にしてください) |
| この文献は、Microorganisms. 2026 Jan 27;14(2):290.に掲載されたProbiotic and Dietary Supplements Intervention in Age-Related Neurodegenerative Disorders. を日本語に訳したものです。タイトルをクリックして原文を読むことが出来ます。 |