
Sehee Park et al.
Biochemical and Biophysical
Research Communications 440 (2013) 14–19
要約
インフルエンザウイルスは世界中の人間集団に非常に伝染性があり、年間約250,000〜500,000人が死亡しています。ワクチンや抗ウイルス薬は、感受性の高い個人を保護するために一般的に使用されます。しかし、ワクチンの抗原ミスマッチと現在利用可能な抗ウイルス薬に対する耐性株の出現により、新しい広域スペクトルの抗インフルエンザ薬を開発することが急務となっています。
ここでは、いくつかのポリフェノール成分を含む多年生低木種の果実であるAronia melanocarpa(ブラックチョークベリー、アロニア)が、オセルタミビル耐性株を含むインフルエンザウイルスのさまざまなサブタイプに対してin vitroおよびin vivoで有効であることを報告します。
アロニアのこれらの抗インフルエンザ特性は、2つの成分、エラグ酸とミリセチンに起因していました。生体内治療マウスモデルでは、アロニア、エラグ酸、ミリセチンがマウスを致命的な攻撃から保護しました。これらの結果に基づいて、アロニアは抗ウイルス剤の貴重な供給源であり、エラグ酸とミリセチンはインフルエンザ治療薬としての可能性があることを示唆しています。
訳者注:オセルタミビルは、スイスのロシュ社により商品名「タミフル」(tamiflu)で販売されています。
はじめに
インフルエンザウイルスはヒトに急性呼吸窮迫を引き起こします[1]。感染が始まると、これらのウイルスは呼吸器症状を引き起こしてから、個々の免疫システムによって排除されます。二次細菌感染などのさまざまな種類の合併症を伴う場合、インフルエンザウイルスは深刻な後遺症を引き起こし、世界中で年間最大250,000〜500,000人の死亡の原因となっています[1]。パンデミックはさまざまな死亡率推定値をもたらします。1918年から19年の間に、4,000万人以上がH1N1インフルエンザの大流行に見舞われました[2]。最近では、推定570,000人の死亡が2009年のパンデミックH1N1(pH1N1)感染に関連していることが判明しました[3]。繰り返し発生する断続的なインフルエンザ感染は、これらの呼吸器病原体に対する効果的な介入方法を組織する必要性を強調しています。
ワクチンはインフルエンザ感染に対して選択する主要な管理手段と考えられています。しかしながら、失望するワクチンの有効性は非常に若い患者と非常に古い患者の両方に懸念を引き起こし[4,5]、不活性化された3価インフルエンザワクチン(TIV)は、健康なレシピエントであっても常に適切な体液性反応をもたらすとは限りません[6]。これらの技術的ハードルを克服するために、効果的なアジュバント補充[7]またはワクチン投与のための代替経路[8]が、他の方法論的ブレークスルー[9]とともに調査されました。抗ウイルス薬もインフルエンザ患者の治療に利用できます[10]。しかしながら、抗ウイルス耐性株の出現により、医師は臨床状況において適切な薬剤を選択することが困難になっている[11]。
さらに、オセルタミビル感受性の対応物に対するオセルタミビル耐性株の病原性の強化[12]と性能過剰の可能性[13]は、新しい抗インフルエンザ薬を開発する緊急の必要性を強調しています。ポリフェノール剤が代替となり得る。さまざまなポリフェノールは、1990年代から抗インフルエンザ療法としての潜在的な使用が調査されており、インフルエンザの感染性を抑制することにより、in vitroおよび/またはin vivoでの有効性が実証されています[14、15]。
アロニアメラノカルパ(Aronia)は、北米のネイティブブラックチョークベリーで、ポリフェノールが豊富な多年生低木で、その薬効の可能性について集中的に研究されています[16]。アロニアの化学成分のいくつかはウイルス性疾患に対してテストされています[17]。特に、イソケルセチン[18]、ケンフェロール[19]、フェルラ酸[20]、カフェイン酸[21]、およびヒドロキシ安息香酸[22]は、それらの抗インフルエンザ活性に基づく評価が提案されています。エラグ酸の場合、H3N2ウイルス複製に対する相乗効果は、オセルタミビルと同時に適用すると、Madin–Darbyイヌ腎臓(MDCK)細胞で見られました[23]。ただし、アロニアポリフェノールのin vivoでの有効性はまだ解明されていません。
この研究では、インフルエンザウイルスに対するアロニアとその化学成分のin vitroおよびin vivoでの可能性をテストしました。殺ウイルス性試験、表面糖タンパク質阻害アッセイ、複製阻害アッセイ、およびin vivo治療評価の結果に基づいて、アロニア、エラグ酸、ミリセチンは抗ウイルス治療薬として開発される可能性があると結論付けています。
結果
季節性、オセルタミビル耐性、およびH5N1インフルエンザウイルスに対するアロニアの有効性
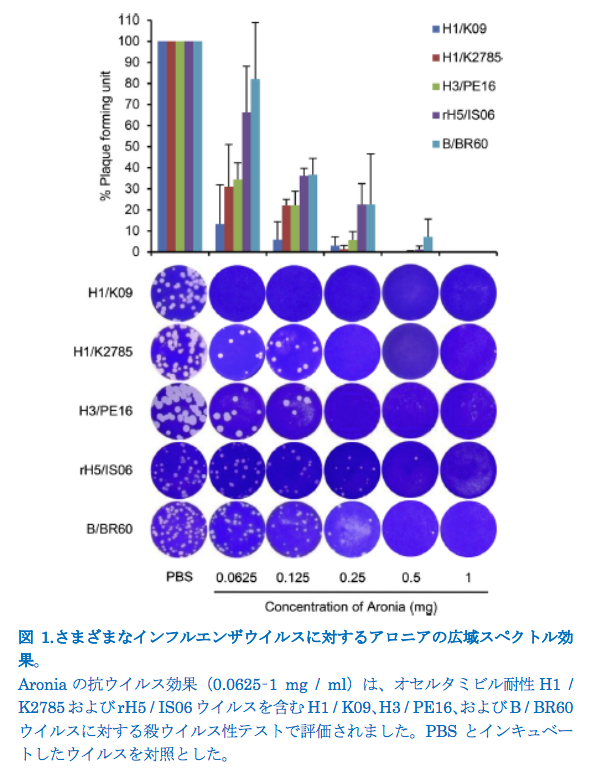
アロニアの抗インフルエンザ効果は、オセルタミビル耐性H1 / K2785株とHPAI rH5 / IS06ウイルスを含む季節性インフルエンザウイルス(H1 / K09、H3 / PE16、およびB / BR60)に対する殺ウイルス性テストで評価されました。
このアッセイでは、0.0625–0.5 mgのアロニアがすべてのテスト済みウイルスに対して交差反応性を示しました。H5およびヒトBサブタイプには比較的高い濃度が必要でしたが、0.0625 mgのアロニアは、オセルタミビル耐性H1 / K2785ウイルスを含むH1およびH3ウイルスに対してほぼ70%のウイルス斑を抑制しました(図1)。アロニアの濃度が増加すると反応性が向上し、0.125 mgはテストしたすべてのウイルスに対して60%以上の有効性を示しました(図1)。これらの発見は、アロニアが様々なインフルエンザウイルス株に対して幅広い抗ウイルス効果を持っていることを示唆しています。
H1 / K09ウイルスに対するアロニアのin vitro効果
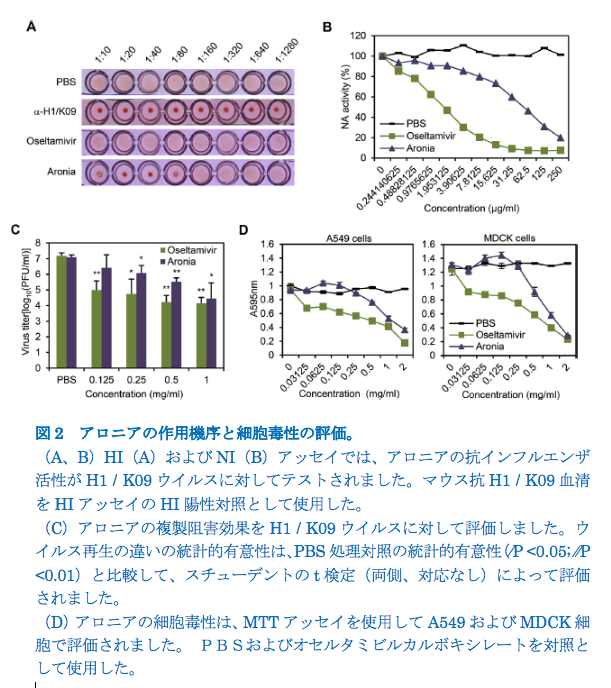
先に述べたように[24]、殺ウイルス性アッセイは、薬剤がウイルス外皮の生化学的組成物を破壊できるかどうかを評価します。したがって、インフルエンザウイルスの表面糖タンパク質、主にHAおよび/またはNAが、アロニアの暫定的な標的タンパク質である可能性があると考えました。アロニアがウイルス感染性をどのように抑制したかを決定するために、H1 / K09 HAおよびNAタンパク質に対するアロニアの阻害効果を評価しました。
まず、アロニアのHI反応性をテストしました。 HIアッセイでは、2.5 lgのアロニアがtRBCのHAとシアル酸間の結合相互作用を阻害し、H1 / K09ウイルスのHAに対して80 HIの力価が得られました(図2A)。その後の蛍光NA阻害(NI)アッセイでは、約1.95 lg / mlのオセルタミビルカルボキシレートが、PBS処理対照と比較してH1 / K09ウイルスのNA活性を50%以上低下させ、62.5 lg / mlがNAを完全に廃止しました酵素活性(図2B)。しかし、AroniaはH1 / K09 NA活性を1.95 lg / mlの濃度で約10%だけ減少させました(図2B)。テストされた濃度のAroniaでは、完全なNA阻害は達成されませんでした。 次に、アロニアのウイルス複製阻害効果とオセルタミビルのウイルス複製阻害効果を比較しました。オセルタミビルと比較してアロニアの有効性は低いですが、アロニアはH1 / K09ウイルスの複製を用量依存的に阻害することもわかりました(図2C)。 MTTアッセイの結果に基づいて、Aroniaは培養細胞(MDCKおよびA549細胞)に対する細胞毒性がオセルタミビルカルボキシレートよりも低いこともわかりました(図2D)。これらの結果は、アロニアが主にHAタンパク質を標的とすることでインフルエンザウイルスの複製を阻害することを示しています。
アロニアの化学成分
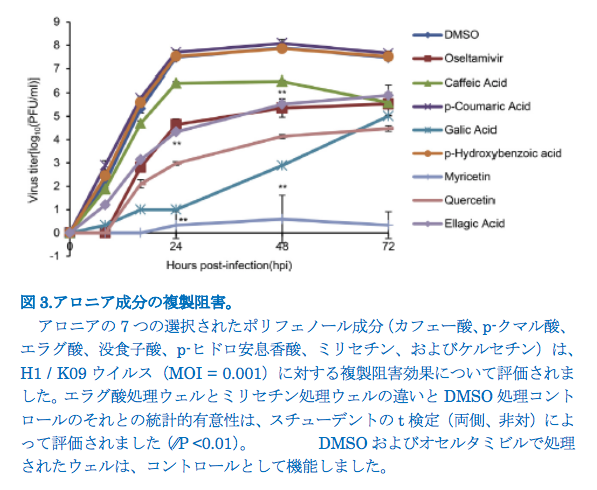
この研究では、A.melanocarpaの粗果実から調製したアロニアを使用しました。 アロニアの有効成分が非特定の化学物質と混合された可能性があります。したがって、以前に報告されたアロニアの組成指数[27]を調べ、アロニアの選択した7つのポリフェノール成分(カフェー酸、p-クマル酸、エラグ酸、没食子酸、p-ヒドロキシ安息香酸、ミリセチン、およびケルセチン)の抗ウイルス効果を評価しました。MDCK細胞の複製阻害アッセイでは、エラグ酸、没食子酸、ミリセチン、およびケルセチンがH1 / K09ウイルスの複製を効果的に抑制しました(図3)。それらは、オセルタミビルカルボキシレートと同様またはより優れた効果を示した。ただし、処理された細胞のほとんどが細胞プレートから分離されたため、没食子酸は細胞毒性を示し、ケルセチンとその誘導体は他の多くの研究で評価されました。したがって、さらにin vivoで調査するために、2つのアロニア成分、エラグ酸とミリセチンのみを選択しました。
マウスモデルにおけるアロニア、エラグ酸、ミリセチンのin vivo治療効果
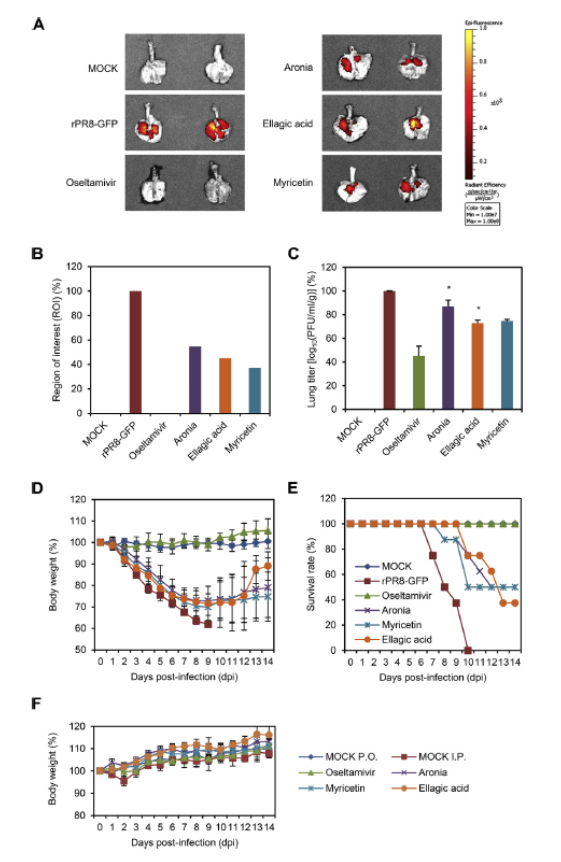
アロニア、エラグ酸、ミリセチンは、抗インフルエンザ治療薬としての使用について評価されました。rPR8-GFPウイルスを使用して[26,28]、ウイルスの侵入の重症度とウイルスの病原性からの治療的回復は、マウスモデルで最初に決定されました。 感染したマウスの抽出された肺からのGFP信号を検出することにより、rPR8-GFPウイルスが感染した肺の表面のほとんどで強いGFP信号を生成することを確認しました(図4A)。アロニア、エラグ酸、ミリセチンで治療すると、感染マウスの肺では、未治療マウスの肺と比較して、GFPの発現が50%以上減少しました(図4AおよびB)。GFP減少率がリン酸オセルタミビル治療で観察されたものに達しなかったとしても、アロニアとその2つの成分はウイルスの侵入を制限し、ウイルス複製を15〜30%減少させました(図4C)。
次に、アロニア、エラグ酸、ミリセチンがマウスを致命的な攻撃から保護できるかどうかを調べました。マウスをrPR8-GFPウイルスでチャレンジし、上記と同じ手順で5日間処理しました。 治療を行わなかった場合、感染したマウスはすべて10 dpiで死亡したため、rPR8-GFPウイルスは100%の致死率でした(図4E)。しかし、リン酸オセルタミビル処理により、感染したマウスは14 dpiまで生存できました(図4DおよびE)。アロニア、エラグ酸、ミリセチンも治療効果を示しました。それらはウイルスの罹患率のレベルを低下させ(図4D)、一部のマウス(それぞれ50、50、および37.5%の生存率)を毒性の兆候のない致死的な攻撃から保護しました(図4EおよびF)。まとめると、これらの結果は、アロニア、エラグ酸、ミリセチンが抗インフルエンザ治療薬としての可能性を秘めていることを示唆しています。
議論
現在、インフルエンザ感染に対して人間が利用できる医療オプションは限られています。ワクチンと抗ウイルス薬は2つの主要な対策です。ただし、ワクチンのミスマッチと抗ウイルス耐性変異株の出現は、新しい医療介入法の開発を要求しています。代替または自然療法として、ポリフェノール化合物は、がん、心血管疾患、神経変性障害などの慢性疾患の予防のために集中的に研究されてきました[29]。さらに、ポリフェノールの抗菌活性は、食品保存料の開発[30]や多くの感染症の治療のための新しい治療法[31]に適用されています。インフルエンザウイルスについては、さまざまなポリフェノールが阻害効果を持つことが報告されています。ただし、提案されたポリフェノール化合物では、広域スペクトルの有効性は確認されていません。
この研究では、アロニアはオセルタミビル耐性H1N1ウイルスやrH5 / IS06ウイルス(図1)などのインフルエンザウイルスに対して交差反応性を示した可能性があります(図2A)。異なるサブタイプのHAは通常、球状の頭部ドメインに異なる抗原シグネチャーを発現します[32]。したがって、さまざまなインフルエンザウイルスに対するAroniaの一般的な効果は、HA頭部の非特異的マスキングによって達成する必要があります。アロニアの阻害機能は、ウイルス表面タンパク質の結合以外のメカニズムによっても媒介される可能性があります。
最近、ミリセチンはウイルス酵素阻害剤としての効能が注目されています[33]。
細胞性シグナル伝達経路の遮断によるウイルスタンパク質輸送または成熟の阻害は、ポリフェノール性クルクミンまたはレスベラトロールの誘導体の作用機序についても提案されている[34]。 細胞ベースのアッセイでは、アロニア、エラグ酸、またはミリセチンでの処理によりウイルス感染は減少しましたが(図1–3)、これらの薬剤の作用の正確なメカニズムを広域抗ウイルス剤としてさらに発展させるために特定する必要があります。
耐性変異株の出現を減らすことは、新しい抗ウイルス薬候補にも必要です。インフルエンザウイルスのNA球状頭部内の触媒部位を標的とするオセルタミビルは、非常に強力で広く処方されている抗インフルエンザ薬です[35]。しかし、オセルタミビル治療の結果に関係なく、2007〜2009年のオセルタミビル耐性H1N1ウイルスの蔓延が、新しい抗ウイルス薬開発の動機となっています。耐性変異体の発生率を下げるには、細胞経路を標的とする抗ウイルス剤の開発が、ウイルスタンパク質を直接標的とするよりも優れた方法である可能性があります。これは、普遍的な細胞経路を遮断することにより、ウイルス自体を化学圧力から免れることができるためです。この研究で特定された有効性に加えて、アロニア、エラグ酸、ミリセチンの未知のメカニズムを解明する必要があります。特に、細胞シグナル伝達経路に対する化合物の影響に焦点を当てています。
Aroniaは、ポリフェノールの豊富なリポジトリです。テストされたインフルエンザウイルスに対するin vitroの有効性に加えて、この研究の結果は、アロニア、エラグ酸、ミリセチンのin vivoでの治療効果を示唆しています。したがって、これらの候補の根底にある責任のあるメカニズムを明らかにすることは、広域スペクトルの抗ウイルス剤の発見を促進し、最終的にインフルエンザウイルスに共通する病因の進行に関する理解を深めることができます。

この文献は、Biochemical and Biophysical Research Communications 440 (2013) 14–19に掲載された Aronia melanocarpa and its components demonstrate antiviral activity against influenza viruseswoを一部省略して日本語に訳しました。タイトルをクリックして原論文の全文を英文で読むことが出来ます。